JAR│郑州烟草院&南开大学:时序转录组与代谢组谱分析揭示WRKY6和WRKY23是烟草应对假单胞菌感染的关键调控因子
- 2026-05-28 13:31:18
 点击蓝字↑↑↑“转录组”,轻松关注不迷路
点击蓝字↑↑↑“转录组”,轻松关注不迷路
 生科云网址:https://www.bioincloud.tech
生科云网址:https://www.bioincloud.tech引言:丁香假单胞杆菌烟草致病变种(Pseudomonas syringae pv. tabaci)是一种革兰氏阴性植物病原细菌,引起极具破坏性的烟草野火病,造成全球范围的经济影响。尽管其致病机理已被充分研究,但烟草应对该病原菌感染的动态防御机制仍不清楚。
目的:本研究旨在通过多组学整合分析,解析烟草应对丁香假单胞杆菌感染的分阶段防御机制,重点阐明转录重编程与代谢重塑之间的时空协调关系,并对关键调控模块进行功能验证。
方法:研究者整合时间序列转录组学和代谢组学数据,重构烟草的动态响应模式。通过时序基因共表达网络(TO-GCN)和加权基因共表达网络分析(WGCNA)探索阶段特异性调控模块,并通过构建转基因株系验证WRKY6和WRKY23在抗病性中的作用。
结果:侵染早期(12–24小时)优先激活胁迫信号和激素(水杨酸/茉莉酸)通路,随后在侵染后期(48–60小时)转向细胞稳态调控。WRKY、ERF和NAC转录因子家族协同调控阶段特异性基因表达。值得注意的是,WRKY6和WRKY23被证实为负调控因子,沉默这两个基因可导致病斑面积减少42–58%,病原菌载量降低3.2–4.5倍。代谢组学分析揭示了苯丙烷代谢的持续激活,特别是对L-苯丙氨酸稳态及其防御衍生物黄苷生物合成的调控。此外,还鉴定出参与鞘脂代谢、光响应和激素交互作用的核心模块。
结论:本研究表明,WRKY介导的转录重编程协调了植物激素信号、鞘脂动态和光响应,从而在时空上调控次生代谢产物的生成。所鉴定的WRKY6和WRKY23调控模块为抗病性工程改造提供了分子框架;提出的两阶段防御模型(早期信号转导 → 后期代谢重塑)增进了对植物-病原菌互作的理解,并为精准育种提供了潜在靶点。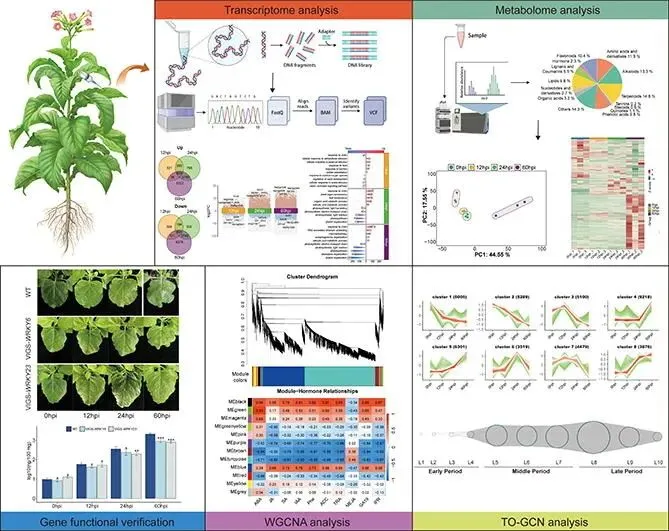
论文ID
实验设计
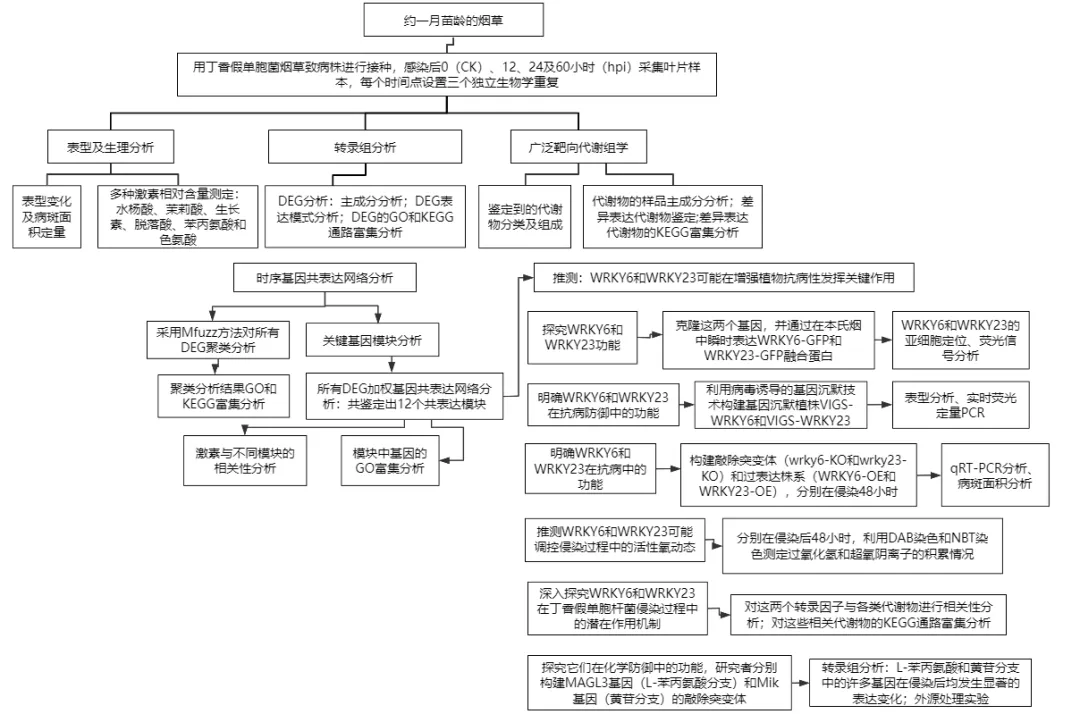
结果
1 烟草对丁香假单胞杆菌感染的表型及生理响应
为评估丁香假单胞杆菌感染对烟草生长的影响,研究者对约一月苗龄的烟草接种了丁香假单胞杆菌烟草致病变种菌株。接种后12小时,侵染点周围未见明显病害症状。接种后24小时,侵染点周围开始出现浅褐色斑点,至接种后60小时,斑点颜色开始加深。与这些观察结果一致,病斑面积的定量分析显示,侵染区域的尺寸随时间逐渐增加,表明侵染期间病害严重程度逐步扩展(图1A)。此外,研究者在丁香假单胞杆菌侵染过程中的0、12、24和60小时分别测定了不同激素的水平。具体而言,水杨酸、茉莉酸和生长素(IAA)的含量在侵染期间稳步增加,其中水杨酸是最丰富的激素(图1B)。作为激素生物合成的必需氨基酸,L-色氨酸和L-苯丙氨酸也观察到相似的变化趋势。相比之下,脱落酸(ABA)的含量表现出不同的模式,在侵染后12小时内略有下降,随后从24小时开始逐渐增加。这些发现表明,烟草对丁香假单胞杆菌的响应可能源于植物激素信号通路的激活。
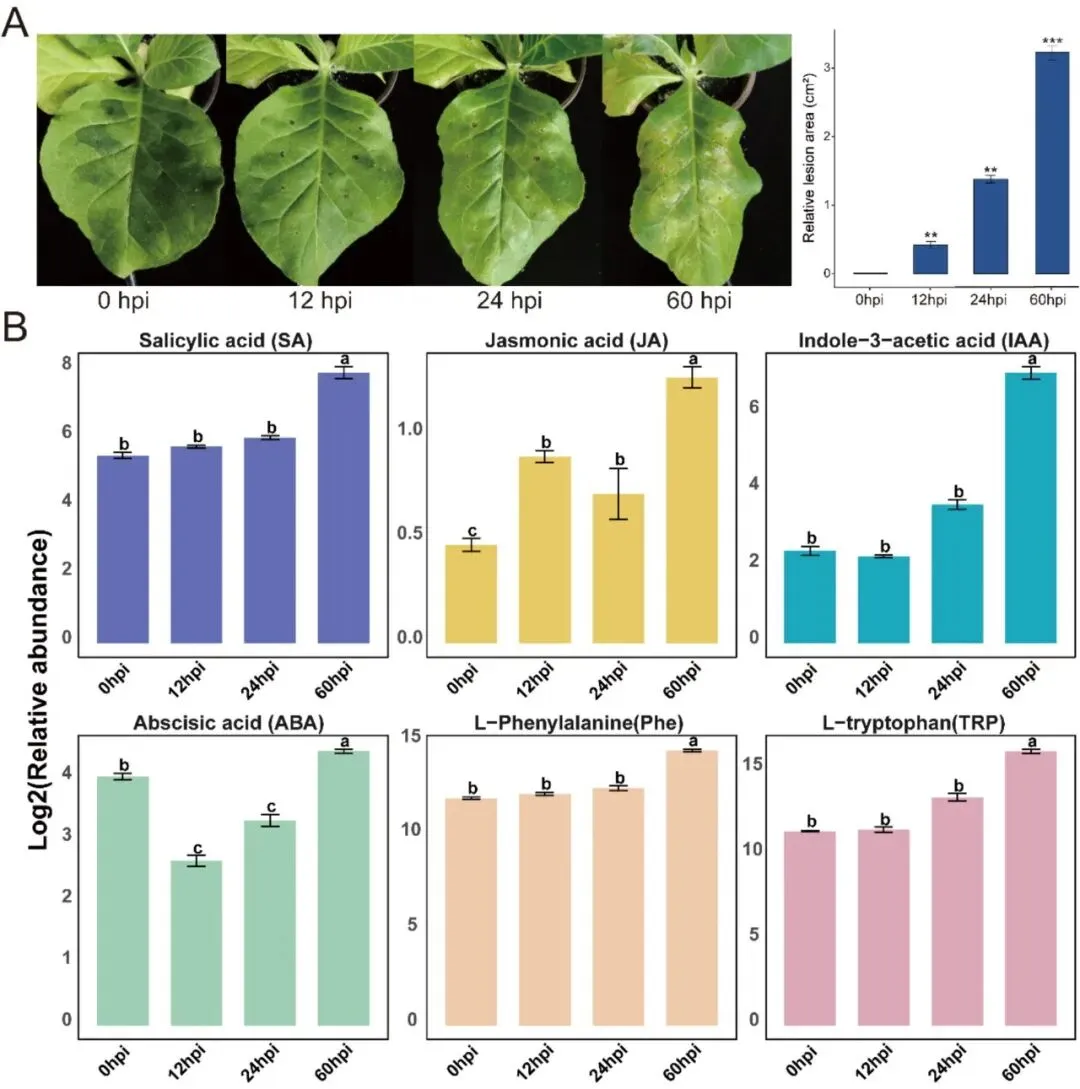
图1. 烟草受丁香假单胞杆菌侵染过程中的表型及生理特性。(A) 丁香假单胞杆菌侵染后0、12、24和60小时(hpi)烟草叶片的表型变化及病斑面积定量。(B) 丁香假单胞杆菌侵染过程中烟草叶片内多种激素的相对含量,包括水杨酸、茉莉酸、生长素、脱落酸、苯丙氨酸和色氨酸。数据为三次独立生物学重复的平均值±标准误(N=3)。(A) 图的统计学显著性采用双尾Student t检验进行评估(P<0.05 (*),P<0.01 (**),P<0.001 (***);NS,无显著差异)。对于(B)图中的多组比较,使用单因素方差分析 followed by Tukey–Kramer检验;柱上不同小写字母表示在P<0.05水平差异显著。
2 烟草响应丁香假单胞杆菌感染的时间序列转录组分析
为阐明烟草在丁香假单胞杆菌侵染过程中防御响应的潜在机制,研究者在侵染后0、12、24和60小时进行了RNA测序,每个样品设置三个生物学重复。过滤低质量读数后,共获得191.02 GB的干净测序读数。Q30碱基比例和GC含量范围分别为95.56%至96.06%和41.93%至44.20%(附表S2)。各样本的比对率均很高,平均值达到95%。为验证RNA-seq结果的准确性,研究者选取12个基因进行RT-qPCR验证,观察到RNA-seq结果与RT-qPCR分析之间存在高度相关性(附图S1)。
相关性分析表明,不同样本的生物学重复间具有良好的重现性,证实了测序数据的可靠性(附图S2A)。主成分分析也显示,不同样本在组内具有较高水平的重复性,并且不同处理组之间也存在显著差异(图2A)。通过转录组分析,研究者共鉴定到42,805个表达蛋白编码基因。为筛选参与丁香假单胞杆菌侵染的候选基因,研究者鉴定了处理样本(12、24、60小时)与对照样本(0小时)之间的差异表达基因。最终,在12小时鉴定到3,031个差异表达基因(1,427个上调,1,559个下调),在24小时鉴定到10,722个差异表达基因(5,500个上调,5,222个下调)。在60小时,差异表达基因数量显著增加至20,295个(10,181个上调,10,114个下调)。在所有侵染时间点均观察到的差异表达基因共有1,624个(633个上调,991个下调),表明侵染对烟草基因表达产生了显著影响(图2B和附图S2B)。通常,植物激素信号通路和植物免疫信号在病原菌侵染过程中发挥重要作用。在已知的植物激素信号通路相关基因中,与水杨酸、茉莉酸和生长素等激素相关的基因在丁香假单胞杆菌侵染期间显著上调。同样,许多已知的植物免疫信号相关基因和病程相关基因也被发现差异表达(附表S3-5)。总体而言,这些发现证实了研究者实验结果的可靠性(附图S2C和D)。
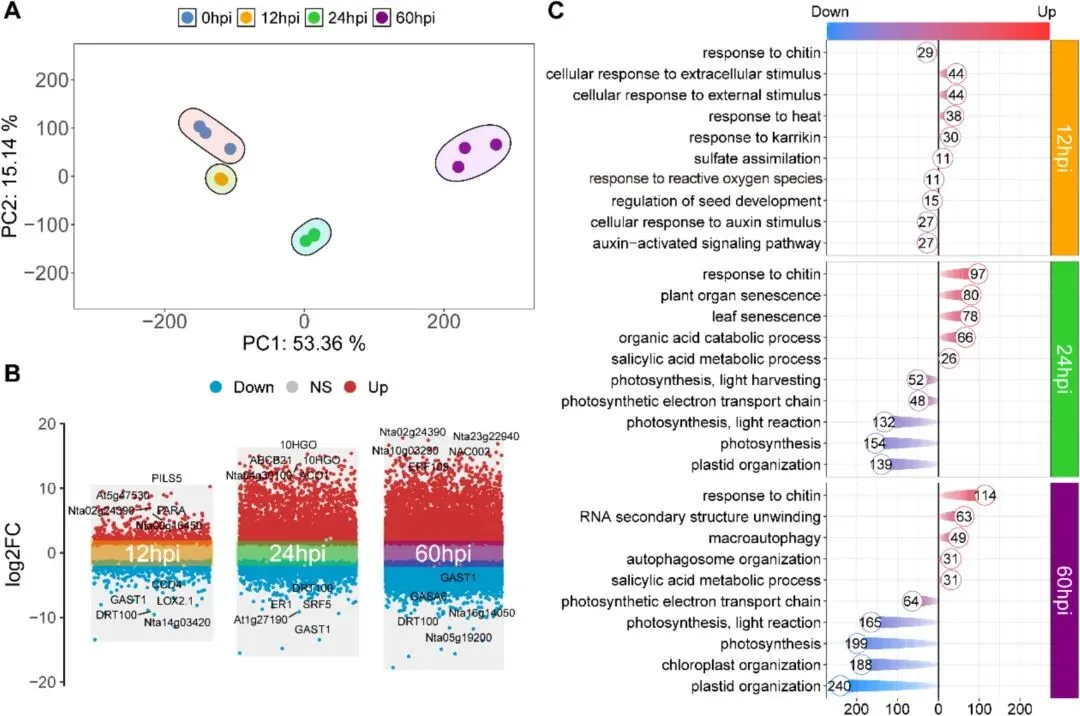
图2. 丁香假单胞杆菌侵染不同时间点的差异表达基因分析。(A) 不同样品基因表达谱的主成分分析。 (B) 火山图显示相对于0 hpi,12 hpi、24 hpi和60 hpi的差异表达基因,其中红色、蓝色和灰色点分别表示上调基因、下调基因和无显著差异基因。 (C) 对12 hpi、24 hpi和60 hpi的差异表达基因进行GO富集分析,展示每个时间点上调和下调基因富集的生物学过程条目。
为鉴定响应丁香假单胞杆菌侵染的通路,研究者利用各时间点的差异表达基因进行了GO和KEGG通路富集分析。GO富集分析显示,上调基因的功能主要富集在胁迫响应和激素调节方面,这些过程在侵染早期(12小时和24小时)迅速激活。在早期阶段,植物通过激活如细胞对细胞外刺激的响应和水杨酸代谢过程等,快速感知并响应病原菌侵染。在侵染后期(60小时),植物通过一系列复杂的分子机制维持细胞稳态和生存,包括激活对几丁质的响应和转录负调控等,共同构成后期防御响应。从侵染早期(12小时和24小时)开始,与光合作用、光反应和光捕获相关的基因显著下调,表明植物主动降低光合作用的能量消耗,将能量重新分配至防御相关的生物学过程。到60小时阶段,光合作用的抑制作用加剧,整体转录活性降低,表明植物在胁迫后期已进入节能的自我保护状态(图2C和附表S6)。KEGG分析也发现了类似结果。此外,在12小时和24小时,KEGG富集分析显示氨基酸代谢和某些次生代谢物的生物合成高度活跃,包括缬氨酸、亮氨酸和异亮氨酸的降解,色氨酸代谢,萜类骨架生物合成,以及二苯乙烯类、二芳基庚烷类和姜酚类的生物合成。在此阶段,植物通过增强氨基酸代谢和昼夜节律相关通路来调整生理状态,使其能够适应病原侵染引起的昼夜变化,并合成防御相关的激素和次生代谢物。在60小时,半胱氨酸和蛋氨酸代谢、淀粉和蔗糖代谢通路显著富集,这些代谢通路的激活可能与增强的抗氧化能力、防御相关基因表达的调控以及防御分子的合成有关(附图S2E和附表S7)。
3 烟草响应丁香假单胞杆菌侵染的时序基因共表达网络分析
通常,表达模式相似的基因在相同的生物学通路中倾向于执行相似的功能。为阐明丁香假单胞杆菌侵染过程中烟草叶片基因表达的时序动态变化,研究者采用Mfuzz聚类方法将所有转录本分为八个簇(图3A)。受丁香假单胞杆菌侵染后,簇1、2和3中的基因表达总体呈下降趋势,而簇4中的基因在侵染后24小时显著上调。簇6和7中的基因表达总体呈先升后降趋势,其中簇6在24小时达到表达峰值,簇7在12小时达到峰值。此外,簇5和簇8中的基因表达持续上调。
为进一步研究丁香假单胞杆菌侵染响应的调控网络,研究者对差异表达基因进行了时序基因共表达网络分析,并选取bZIP12基因作为起始节点(附图S3A)。据此,差异表达基因被划分为10个时间顺序层级(L1–L10),反映了从侵染后0至60小时的渐进式转录程序。基于每个层级内基因的整体表达趋势,这10个层级进一步归并为三个与侵染相关的时期,即早期(L1–L4)、中期(L5–L7)和晚期(L8–L10),代表了侵染过程中转录调控的相继阶段(图3B)。研究者观察到,这10个层级的基因表达峰值与聚类分析中的表达模式精确对应,这与丁香假单胞杆菌侵染的时间进程相符(附图S3B)。具体而言,对于L8-L10层级,基因表达水平的趋势与丁香假单胞杆菌侵染后观察到的趋势高度相似,表现为持续上调。对这些层级的深入分析揭示了几关键转录因子家族,包括WRKY、C2H2、ERF和NAC,它们在调控网络中占据核心位置(附图S2C)。这些转录因子家族的激活可能在侵染响应的快速启动和调控中发挥关键作用。除转录因子外,研究者还发现与免疫和激素信号相关的基因,如WRKY23、CML19、RPP8L2和RLK5,在网络中高度富集。这些结果表明,这些基因可能在应对丁香假单胞杆菌侵染的防御反应中发挥重要作用(附图S3C)。
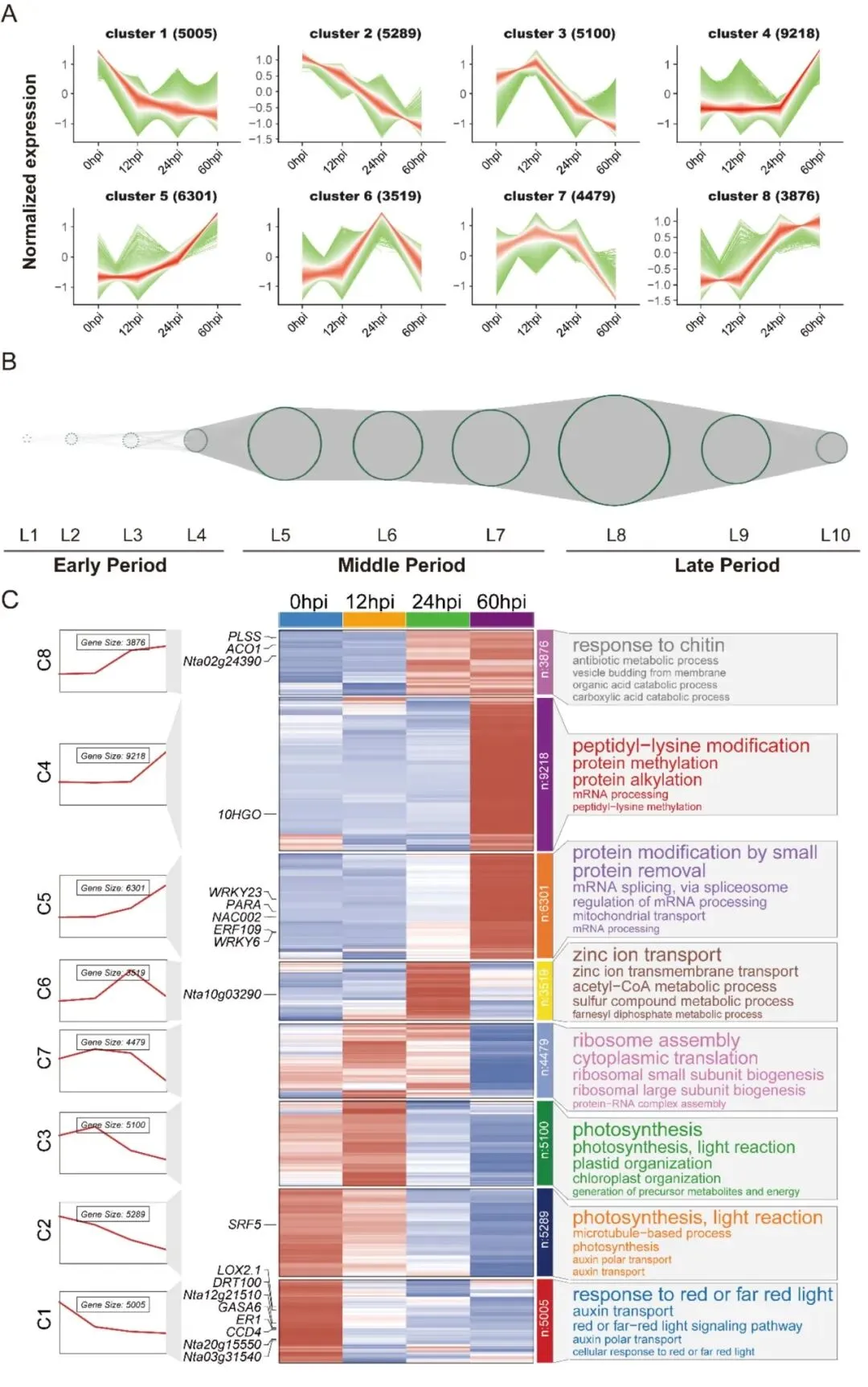
图3. 响应丁香假单胞杆菌侵染的时间顺序基因共表达网络。(A) 采用Mfuzz方法对所有差异表达基因的聚类结果,显示了在0、12、24和60 hpi的标准化表达模式。(B) 预测的烟草响应丁香假单胞杆菌侵染的时序基因共表达网络,其中差异表达基因被组织成10个时间层级(L1–L10),并根据表达动态分为早期、中期和晚期。(C) 时间簇中动态基因表达变化的热图及其GO富集分析,展示了代表性基因及与每个时间簇相关的富集生物学过程条目。
随后,研究者对聚类分析结果进行了GO和KEGG富集分析(图3C)。簇1、2和3中的基因(包括CCD4、ER1、SRF5等)主要在侵染早期高表达,涉及生长素运输和光合作用的光反应,表明植物在侵染早期通过快速调整光合作用和生长平衡来响应病原菌。簇6和7中的基因在侵染中期高表达,主要与锌离子转运和核糖体组装相关,表明植物在侵染中期通过调节能量产生和蛋白质合成来维持生理功能。簇4、5和8中的基因(如WRKY6、PARA、WRKY23等)在侵染晚期激活,主要参与翻译后蛋白修饰和免疫应答相关通路,表明植物防御机制在侵染后期显著激活。这些结果与差异表达基因分析一致,进一步验证了聚类分析的准确性(图3C和附表S8)。综上所述,植物通过基因表达的阶段特异性精细调控其应对丁香假单胞杆菌侵染的响应。同时,KEGG富集分析显示,与卟啉代谢、淀粉和蔗糖代谢以及光合作用通路相关的基因在早期响应阶段(簇1、2和3)显著富集,表明植物在早期通过调控氨基酸降解和糖代谢来快速响应病原菌侵染。在中期响应阶段(簇6和7),结果显示基因富集于苯丙氨酸代谢通路,这与GO分析中关于能量代谢调控的结果一致。在晚期响应阶段(簇4、5和8),KEGG富集分析结果也显示基因富集于谷胱甘肽代谢以及缬氨酸和异亮氨酸降解通路。这些发现表明,在侵染后期,植物通过调整能量代谢和信号转导来维持基本的细胞功能(附图S3D和附表S9)。
4 烟草响应丁香假单胞杆菌侵染的代谢组学分析
为阐明丁香假单胞杆菌侵染过程中烟草的代谢变化,研究者进行了广泛靶向代谢组学和激素代谢组学分析,共鉴定到2,768种代谢物,分为13个不同的类别。其中,丰度最高的前三类分别是生物碱、氨基酸及其衍生物,以及黄酮类化合物(图4A)。主成分分析显示,不同组别间代谢物的变异主要受丁香假单胞杆菌侵染后时间差异的驱动(图4B)。为进一步研究侵染后的代谢变化,研究者对差异表达代谢物进行了统计分析。结果显示,有372种差异表达代谢物在侵染后三个时间点均差异表达,表明它们在植物响应丁香假单胞杆菌侵染中发挥基础且持续的作用(图4C)。
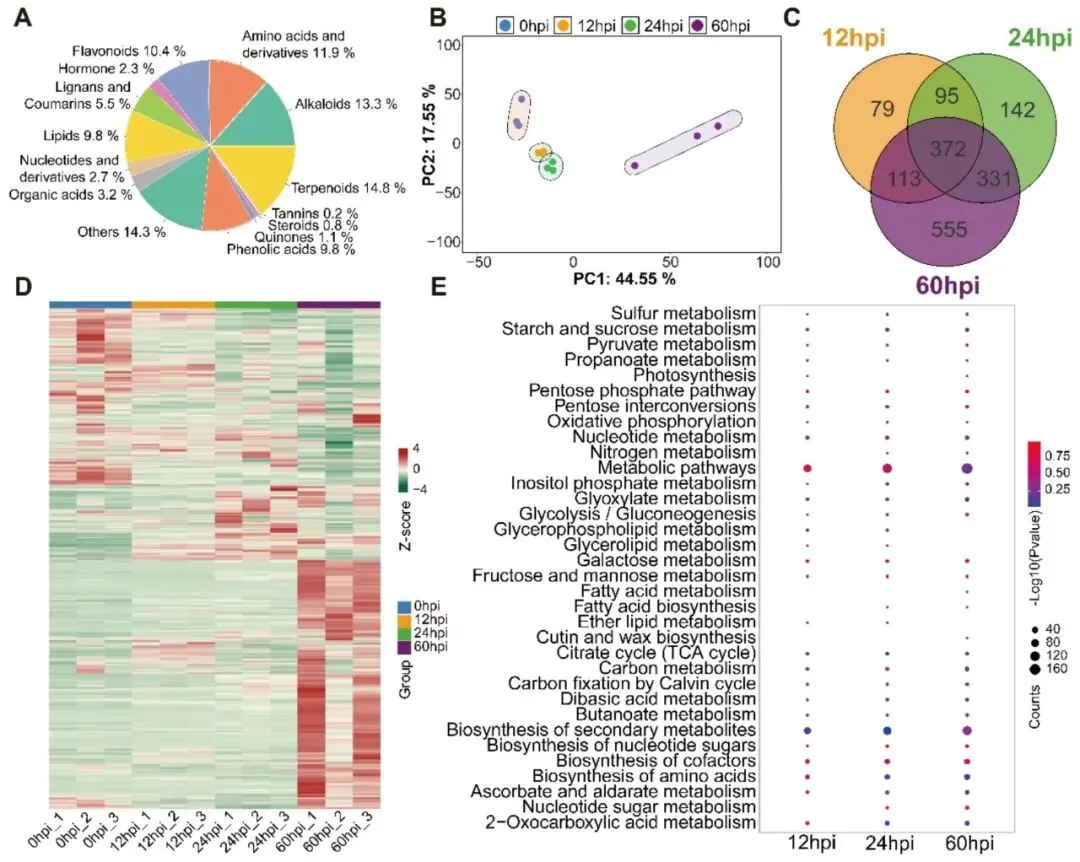
图4. 代谢物分类及差异表达代谢物的鉴定。(A) 鉴定到的代谢物分类及组成。(B) 基于所鉴定代谢物的样品主成分分析。(C) 丁香假单胞杆菌侵染后差异表达代谢物的维恩图。(D) 不同侵染后时间点所有差异表达代谢物的热图。(E) 不同侵染后时间点差异表达代谢物的KEGG富集分析,点大小表示代谢物数量,颜色代表富集显著性。
研究者进一步分析显示,大量差异表达代谢物随侵染时间呈逐渐增加的模式(图4D)。在侵染后期,代谢物表达发生显著变化,许多代谢物呈上调趋势。这些发现表明,植物可能采取逐渐增强的防御策略,即随着丁香假单胞杆菌的持续存在,代谢物的合成和积累增加(图4D)。差异表达代谢物的KEGG富集分析显示,次生代谢物的生物合成、碳代谢以及2-氧代羧酸代谢等几个通路在侵染后三个时间点均被共同富集(附表S10)。此外,在侵染早期至中期(12小时和24小时),甘油磷脂代谢、甘油脂代谢和醚脂代谢等通路出现特异性富集(图4E)。
这些通路可能参与了抵御丁香假单胞杆菌侵染初期所需的快速代谢调整。与这一观点一致,转录组和代谢组数据的整合相关性分析显示,在侵染后12小时,部分代谢通路在基因表达和代谢物积累水平上同时富集(附图S4A和B)。这些共享通路主要包括初级和次生代谢过程,表明侵染后不久即发生早期协调的转录调控,驱动代谢重编程。在侵染中后期(24小时和60小时),特异性富集的通路包括氮代谢、脂肪酸生物合成以及氨基糖和核苷酸糖代谢。在这些后期时间点,差异表达基因和差异表达代谢物中共同检测到的通路数量增加(附图S4A和B),表明转录调控与代谢输出之间的一致性逐渐增强。这表明烟草在侵染早期进行特异性代谢调整,而在中后期则转向涉及防御性化合物合成的通路,以支持更持久的防御机制。此外,转录组和代谢组来源的通路在时间上的重叠和一致的富集模式强调了丁香假单胞杆菌侵染过程中基因表达变化与代谢重编程之间的紧密耦合,且这些通路大多与代谢组学分析得到的差异表达代谢物和转录组分析得到的差异表达基因共享。
总之,从整体时间角度来看,烟草的防御代谢策略似乎是从最初的快速响应转变为更复杂和持久的代谢调整,从而有效应对病原菌的长期存在(图4E和附表S10)。
5 响应丁香假单胞杆菌侵染的关键模块鉴定
为更深入地理解烟草响应丁香假单胞杆菌侵染的机制,研究者对所有差异表达基因进行了加权基因共表达网络分析,以鉴定响应丁香假单胞杆菌侵染的潜在关键模块。基于相似的表达模式,共鉴定出12个共表达模块(图5A)。考虑到激素在丁香假单胞杆菌侵染过程中的重要作用,研究者探究了激素与不同模块的相关性。结果显示,大多数激素与黑色、绿色和蓝色模块呈显著正相关,而与紫色、棕色和青绿色模块呈显著负相关(图5B)。鉴于黑色、绿色和蓝色模块与多种激素的高度相关性,研究者进一步分析了这三个模块中基因的表达模式。这些模块中的基因在丁香假单胞杆菌侵染期间表现出显著的表达变化(附图S5A-C)。GO富集结果显示,黑色模块中的基因显著富集于鞘脂代谢过程、多元醇生物合成过程以及对活性氧的响应等生物学过程(附图S5D)。绿色模块中的基因显著富集于对光照强度的响应、乙烯激活的信号通路以及细胞分裂素激活的信号通路等关键生物学过程(附图S5E和附表S11)。蓝色模块中的基因显著富集于赤霉素介导的信号通路、细胞对水杨酸刺激的响应、脱落酸激活的信号通路以及蛋白去磷酸化等生物学过程(图5C)。类似地,KEGG分析也揭示了黑色、蓝色和绿色模块在植物代谢调控和信号转导中的功能特异性和潜在作用(附图S6A和附表S12)。这些发现表明,这三个模块的功能与植物激素的调控及对丁香假单胞杆菌侵染的响应密切相关。
为进一步探究上述三个模块内部基因间的互作关系并挖掘关键基因的核心调控作用,研究者分别构建了基因调控网络。黑色和绿色模块的网络分析显示,vps13A、AFC2、UGT80B1、PRR95、COL9及LUX等核心调控因子与模块内基因呈现高度相关性(附图S6B)。蓝色模块的网络分析则表明,CML36、CIPK7、RPP8L2、PLL5、WRKY23和WRKY6等基因处于网络核心位置,可能作为关键调控因子发挥作用(图5D)。鉴于蓝色模块与水杨酸、茉莉酸和生长素呈现较高的正相关性,研究者推测这些候选核心基因可能与该类激素协同调控。此外,这些鉴定的核心基因大多与已知的植物激素及免疫调控密切相关,这不但印证了WGCNA分析结果的可靠性,也为后续研究提供了重要的候选靶点。
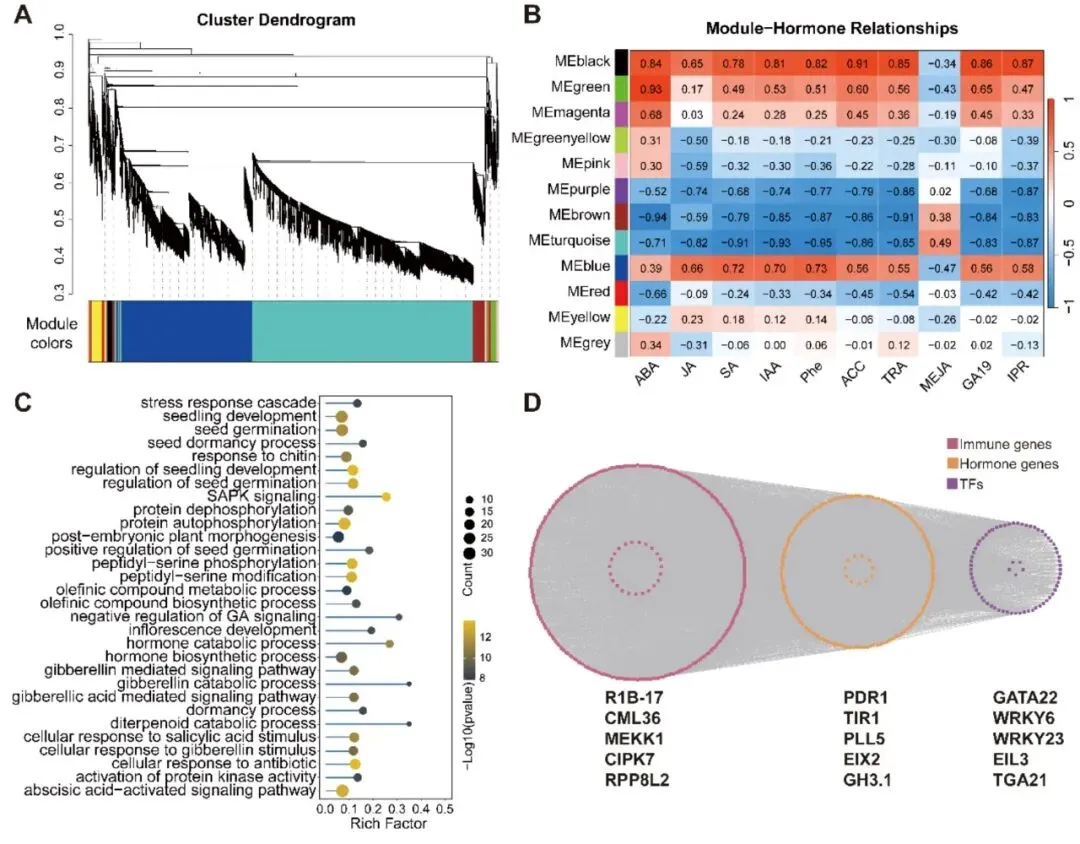
图5. 烟草受丁香假单胞杆菌侵染后的基因模块分析。(A) 聚类树状图显示12个共表达基因模块。(B) 模块与不同激素相关性的热图(颜色刻度表示相关性强度)。(C) 蓝色模块中基因的GO富集分析,显示显著富集的生物学过程条目。(D) 蓝色模块中的基因调控网络,突出显示免疫相关基因、激素相关基因和转录因子。
6 WRKY6与WRKY23负向调控烟草对丁香假单胞杆菌的抗性
前述TO-GCN和WGCNA分析已表明,核心基因尤其是WRKY6和WRKY23转录因子可能在侵染过程中与水杨酸、茉莉酸和生长素协同调控,且在丁香假单胞杆菌侵染后显著诱导表达。因此,研究者推测WRKY6和WRKY23可能在增强植物抗病性中发挥关键作用。为深入探究其功能,首先克隆了这两个基因,并通过在本氏烟中瞬时表达WRKY6-GFP和WRKY23-GFP融合蛋白对其亚细胞定位进行了检测。荧光信号分析显示,WRKY6和WRKY23均特异性定位于细胞核(图6A)。
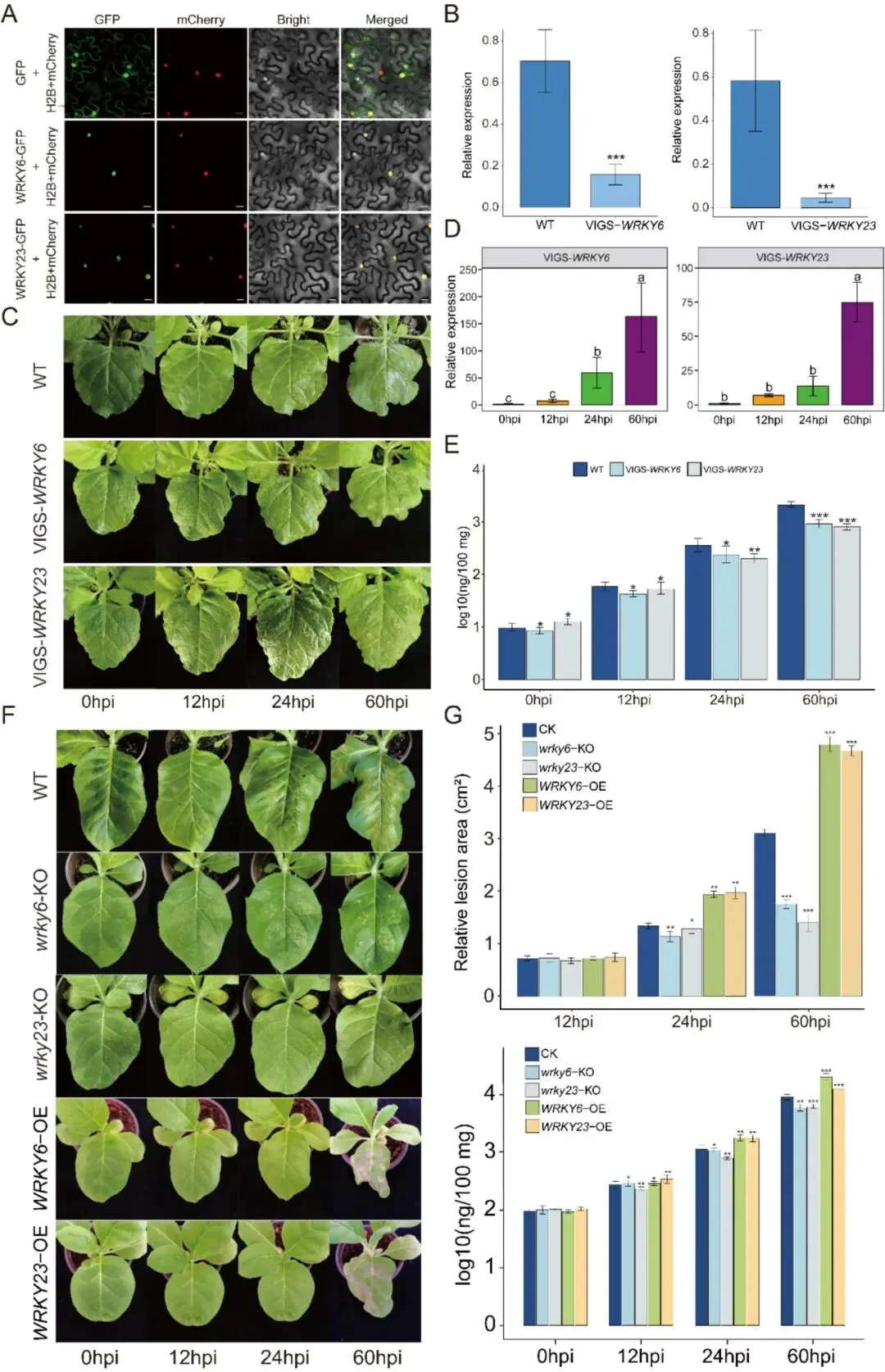
图6. WRKY6和WRKY23通过活性氧信号介导核定位的防御反应以应对丁香假单胞杆菌侵染。(A) WRKY6和WRKY23的亚细胞定位。用融合构建体(WRKY6-GFP 和 WRKY23-GFP)和核标记物H2B-mCherry瞬时转化本氏烟叶片。(B) WRKY6和WRKY23在野生型和VIGS-WRKY6/VIGS-WRKY23沉默植株中的相对表达水平。(C) 野生型与VIGS-WRKY6/VIGS-WRKY23沉默植株在丁香假单胞杆菌侵染后的表型分析。(D) 丁香假单胞杆菌侵染过程中,WRKY6和WRKY23在VIGS-WRKY6/VIGS-WRKY23沉默植株中的时序表达模式。(E) 使用种特异性引物对通过实时荧光定量PCR对侵染叶片中丁香假单胞杆菌DNA进行定量。(F) 野生型、wrky6-KO、wrky23-KO、WRKY6-OE和WRKY23-OE植株在丁香假单胞杆菌接种后0、12、24和60 hpi的表型分析。(G) 野生型、敲除突变体和过表达株系在0、12、24和60 hpi的相对病斑面积和丁香假单胞杆菌DNA水平的定量。数据为三次独立生物学重复的平均值±标准误(N=3)。(B)和(E)图的统计学显著性采用双尾Student t检验进行评估(P<0.05 (*),P<0.01 (**),P<0.001 (***);NS,无显著差异)。对于(D)图中的多组比较,使用单因素方差分析 followed by Tukey–Kramer检验;柱上不同小写字母表示在P<0.05水平差异显著。
为明确WRKY6和WRKY23在抗病防御中的功能,研究者首先利用病毒诱导的基因沉默技术构建了基因沉默植株VIGS-WRKY6和VIGS-WRKY23。与野生型植株相比,沉默植株中WRKY6和WRKY23的表达水平均显著降低(图6B)。值得注意的是,在本氏烟中,丁香假单胞杆菌侵染并未诱导产生明显病斑,而是引起萎蔫症状(图6C)。与野生型植株相比,VIGS-WRKY6和VIGS-WRKY23植株在病原菌侵染后表现出更为严重的萎蔫。同时,接种后四个时间点的时序表达模式与转录组数据趋势一致(图6D)。随后,研究者利用种特异性引物通过实时荧光定量PCR对侵染叶片中的病原菌生物量进行了定量。结果表明,VIGS-WRKY6和VIGS-WRKY23植株中丁香假单胞杆菌的生物量显著低于野生型植株(图6E),提示沉默这两个基因可增强植株对病原菌的抗性。
为进一步明确WRKY6和WRKY23在抗病中的功能,研究者构建了敲除突变体(wrky6-KO和wrky23-KO)和过表达株系(WRKY6-OE和WRKY23-OE)(附图S7A)。qRT-PCR分析证实了各基因型中相应基因的有效敲除和过表达(附图S7B)。接种丁香假单胞杆菌后,敲除株系和过表达株系相较于野生型表现出相反的抗感病表型(图6F)。wrky6-KO和wrky23-KO植株的病害症状均有所减轻,而WRKY6-OE和WRKY23-OE植株则表现出更明显的褪绿和病斑扩展。病斑面积分析进一步证实了这一趋势:在侵染后12、24和60小时,敲除株系的病斑面积显著减小,而过表达株系的病斑面积则显著增大(图6G)。与此一致,各时间点的病原菌生物量定量结果显示,敲除植株中细菌积累量较低,而过表达植株中则较高(图6G)。综上所述,这些结果支持WRKY6和WRKY23在防御反应中发挥负调控因子的作用:在丁香假单胞杆菌侵染过程中,基因敲除增强了抗病性,而过表达则导致了感病性增强。
7 WRKY6与WRKY23通过调控ROS及代谢物介导烟草抗病性
鉴于功能缺失株系抗性增强以及氧化进发在植物免疫中的核心作用,研究者推测WRKY6和WRKY23可能调控侵染过程中的活性氧动态。为此,研究者分别在侵染后48小时,利用DAB染色和NBT染色测定了过氧化氢和超氧阴离子的积累情况。DAB染色显示,侵染后48小时,VIGS-WRKY6和VIGS-WRKY23叶片中的过氧化氢积累强于野生型植株(图7A)。同样,NBT染色显示,同一时间点沉默植株中超氧阴离子积累也增强(图7A)。沉默植株中活性氧积累的增加可能有效限制了病害发展,这与在VIGS沉默植株和突变体株系中观察到的抗性增强表型一致。
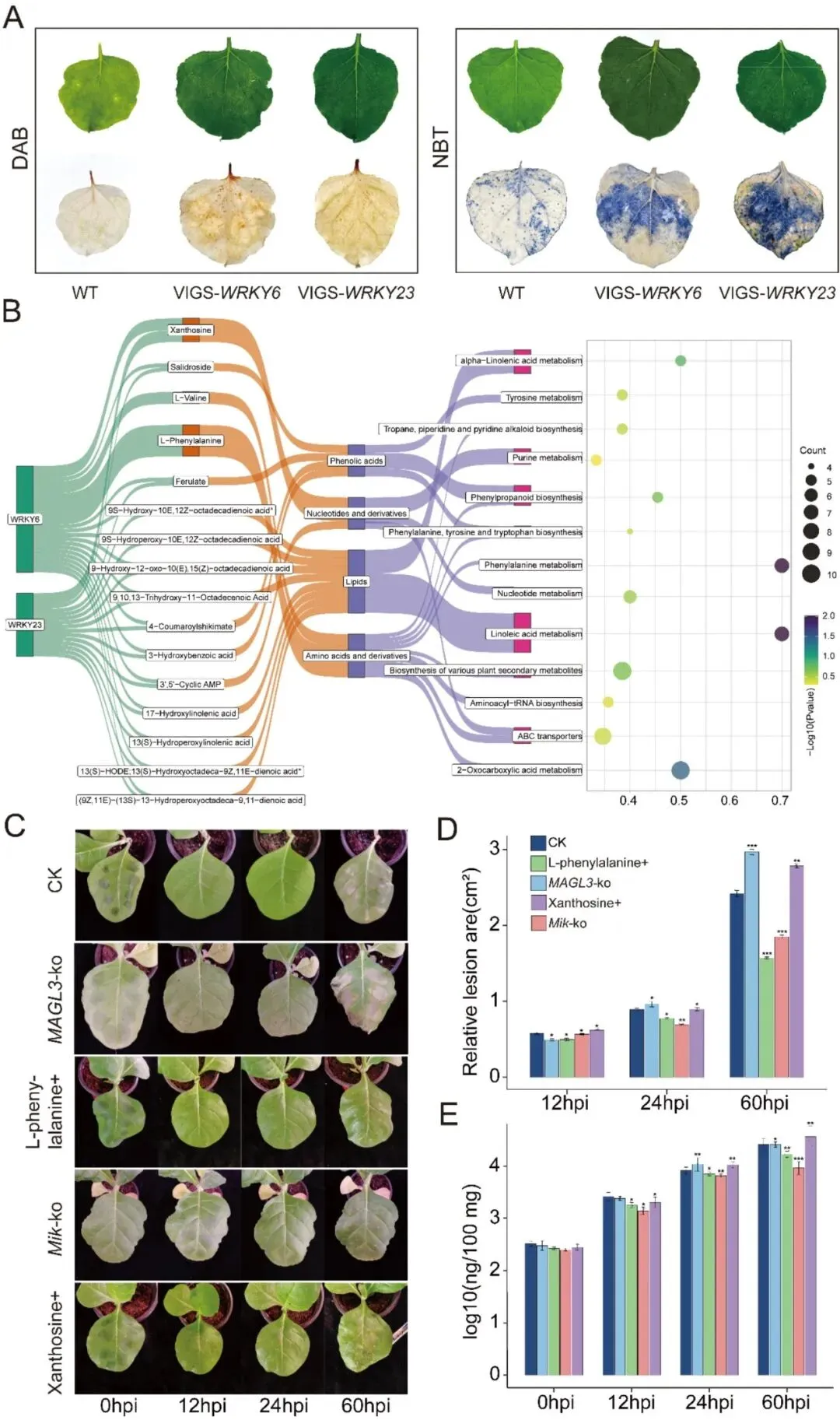
图7. WRKY6和WRKY23敲除突变体对丁香假单胞杆菌的感病性及时间基因表达谱。(A) 丁香假单胞杆菌侵染后48小时,野生型与VIGS-WRKY6/VIGS-WRKY23沉默植株离体叶片中H2O2(DAB染色)和O2⁻(NBT染色)的组织化学检测。(B) 与WRKY6和WRKY23相关代谢物的KEGG分析。(C) 野生型、MAGL3敲除、Mik敲除以及代谢物预处理(L-苯丙氨酸+ 和黄苷+)的烟草叶片在丁香假单胞杆菌侵染后0、12、24和60小时的代表性表型。(D) 野生型、敲除突变体和代谢物预处理植株在12、24和60 hpi的相对病斑面积定量。(E) 各基因型和处理在0、12、24和60 hpi时侵染叶片中的细菌群体定量。数据为三次独立生物学重复的平均值±标准误(N=3)。所有统计学比较均使用双尾Student t检验进行;显著性表示为P<0.05 (*),P<0.01 (**),P<0.001 (***);NS,无显著差异。
为深入探究WRKY6和WRKY23在丁香假单胞杆菌侵染过程中的潜在作用机制,研究者对这两个转录因子与各类代谢物进行了相关性分析。相关性图谱显示,氨基酸及其衍生物是与WRKY6和WRKY23显著相关的主要代谢物类别(附图S7C)。研究者对这些相关代谢物的KEGG通路富集分析表明,WRKY6和WRKY23可能特别调控亚油酸代谢、苯丙氨酸代谢以及托品烷、哌啶和吡啶生物碱的生物合成等通路。值得注意的是,苯丙烷途径中的L-苯丙氨酸及其下游防御化合物黄苷与WRKY6/23的表达水平呈现出极强的正相关性(图7B)。
此外,转录组分析显示,L-苯丙氨酸和黄苷分支中的许多基因在侵染后均发生显著的表达变化,表明它们积极响应丁香假单胞杆菌侵染,且与WRKY6/23的表达相关(附图S7D和S7E)。为探究它们在化学防御中的功能,研究者分别构建了MAGL3基因(L-苯丙氨酸分支)和Mik基因(黄苷分支)的敲除突变体。接种丁香假单胞杆菌后,MAGL3-ko植株的病斑面积和病原菌载量均有所增加,而Mik-ko植株的病斑扩展和病原菌积累则减少(图7C–E)。外源处理实验进一步证实了这些结果:L-苯丙氨酸处理减小了野生型叶片的病斑面积和病原菌数量,而黄苷处理则增大了两者(图7C–E)。综上所述,这些遗传学和代谢学研究结果证明,L-苯丙氨酸分支促进了感病性,而黄苷分支则赋予抗病性,从而将WRKY介导的转录调控与植物防御中的代谢重编程联系起来。
讨论
随着高通量测序技术的快速发展,组学分析已成为研究植物-病原菌互作机制不可或缺的工具。整合转录组学和代谢组学数据有助于更全面地理解病原菌侵染过程中植物的分子调控网络,从而揭示关键调控模块在植物防御反应中的重要作用。本研究通过多组学整合分析阐明了烟草抵御丁香假单胞杆菌的动态防御机制,揭示了侵染早期阶段特异性激素信号(水杨酸、茉莉酸、生长素)的激活和光合作用的抑制,随后由WRKY、ERF和NAC转录因子介导的转录重编程以维持生物碱和类黄酮的生物合成。功能验证表明,WRKY6和WRKY23负向调控烟草抗性。沉默这些基因增强了活性氧积累和特异性代谢物的产生,从而将它们确定为抗病作物育种的关键靶点(附图S8)。
1 植物响应丁香假单胞杆菌侵染的激素信号转导通路
转录组和代谢组分析显示,丁香假单胞杆菌侵染显著改变了烟草中众多基因和代谢物的表达水平,其中上调的候选基因主要富集于与植物防御相关的通路,如苯丙烷代谢、植物激素信号转导和MAPK信号通路。关于丁香假单胞杆菌致病机制的研究,不仅在理解细菌病原体如何利用III型效应子抑制植物免疫、促进感病性方面取得了概念性进展,也促进了气孔免疫和茉莉酸信号关键组分的发现。与茉莉酸信号不同,植物激素水杨酸以其在抵御昆虫取食和死体营养型病原菌中的关键作用而闻名,通常通过水杨酸和茉莉酸信号之间的拮抗相互作用来促进丁香假单胞杆菌的侵染。本研究的结果也证实了水杨酸和茉莉酸在响应丁香假单胞杆菌侵染中的重要作用。此外,还观察到其他激素(包括生长素和脱落酸)相关基因/代谢物的富集,这表明其他植物激素可能在调控植物对丁香假单胞杆菌的抗性中也发挥着不可或缺的作用。特别地,敲除一个重要的生长素生物合成基因CAT2,显著增加了病斑面积和细菌增殖,证实了生长素稳态有助于有效的防御(附图S9A和B)。
玉米病原菌玉米黑粉菌(Ustilago maydis)侵染后,其效应蛋白Naked1(Nkd1)能够易位至宿主细胞核。通过其乙烯响应因子相关的两亲性抑制基序,Nkd1与转录辅抑制蛋白TOPLESS/TOPLESS相关蛋白相互作用。这种相互作用阻止了TOPLESS/TOPLESS相关蛋白招募激素信号相关的转录抑制因子,从而解除对生长素和茉莉酸信号通路的抑制。结果,宿主对(半)活体营养型病原菌的感病性增强。同时,生长素信号的适度上调抑制了病原相关分子模式触发的活性氧迸发,而这是早期防御反应的一部分。这些发现与研究者的结果完全吻合,因为在烟草受丁香假单胞杆菌侵染后,生长素和茉莉酸的水平开始略有上升。与大多数激素不同,丁香假单胞杆菌的效应子作为脱落酸信号通路的劫持者,通过促进气孔关闭,成为植物感病性的关键机制。脱落酸的调控在受丁香假单胞杆菌侵染后发生改变,其一种强效的水诱导效应子AvrE结合并抑制拟南芥1型蛋白磷酸酶的功能。1型蛋白磷酸酶通过抑制脱落酸信号通路的关键节点SnRK2来负向调控脱落酸。这一结果与研究者观察到的丁香假单胞杆菌侵染后烟草早期脱落酸含量下降的现象一致。然而,后期脱落酸含量恢复的机制仍然是一个新的研究方向,未来需要更多探索。
2 丁香假单胞杆菌侵染后的次生代谢与光合代谢重编程
代谢组学分析揭示,丁香假单胞杆菌侵染显著改变了烟草的代谢谱,次生代谢物(包括酚酸、类黄酮、萜类和生物碱)的水平显著增加。此外,这些次生代谢物的积累与酚类和类黄酮生物合成通路的诱导密切相关,后者是植物防御反应的标志[49],在保护植物免受病原菌入侵中发挥着关键作用。例如,苯丙烷类化合物肉桂醛可抑制燕麦镰孢菌(Fusarium sambucinum)的生长。玉米中的β- Costic acid在体内和体外均能限制轮枝镰孢菌(Fusarium verticillioides)和禾谷镰孢菌(Fusarium graminearum)的生长。通常,这些由病原菌诱导的防御性次生代谢物被称为植物抗毒素。大量研究已证实在水稻、玉米和大麦等主要作物中产生了多种基于萜类的植物抗毒素及其功能。例如,寄主植物受稻瘟病菌(Magnaporthe oryzae)和水稻黄单胞杆菌(Xanthomonas oryzae)等病原菌侵染后,会诱导产生二萜类化合物,以抑制孢子萌发和菌丝生长。此外,萜类化合物在共生互作中充当信号分子。独脚金内酯是一类倍半萜植物激素,由植物根系释放,诱导真菌响应,如孢子萌发和菌丝向寄主根部分支,从而触发植物的共生互作。因此,这些次生代谢物的快速积累可能作为烟草的即时防御策略,有助于在侵染早期建立有效的屏障抵御病原菌入侵。
次生代谢物的大量生产需要大量的碳和能量供应,这就要求对初级代谢途径,特别是光合作用,进行协调调整。次生代谢的激活通常伴随着初级代谢过程的重编程,以满足防御反应增加的能量和碳需求。为了探究光合活性是否参与这些代谢调整,研究者专门评估了侵染过程中光合作用的动态变化。同时,观察到从侵染后24至60小时,大多数光合作用相关基因呈渐进式下调,揭示光合基因表达与病原菌载量之间存在明显的负相关(附图S9C和D)。为了验证这种关系的功能相关性,研究者对一个光合作用相关基因进行了功能缺失分析。敲除CLH1导致病斑显著增大、病原菌载量高于野生型(附图S9E和F)。综上所述,这些发现表明光合活性降低会削弱植物抗性,同时强调了光合作用下调是侵染期间为实现有效免疫反应而采取的一种战略性能量重分配策略。
尽管代谢组学已揭示了病原菌侵染后广泛的代谢变化,但组织中代谢物的空间分布和动态变化在很大程度上仍不清楚。因此,更深入地理解光合作用衍生的碳如何空间分配到防御相关代谢物中,对于阐明植物免疫的代谢基础至关重要。将空间代谢组学与光合活性图谱相结合,可为揭示侵染过程中初级碳通量如何支持次生代谢和局部防御反应提供新的视角和方法。
3 烟草响应丁香假单胞杆菌侵染的关键调控因子
基因共表达网络分析鉴定出黑色、绿色和蓝色模块,这些模块在丁香假单胞杆菌侵染后显著上调,并与多种防御相关激素呈正相关。进一步的功能分析表明,蓝色模块中的关键基因编码重要的转录因子、激酶和代谢酶,它们可能参与调控下游基因的表达和代谢物的合成,有助于烟草抵御丁香假单胞杆菌侵染。特别地,蓝色模块中的WRKY23和WRKY6转录因子可能通过协调关键防御相关植物激素(水杨酸、茉莉酸和生长素)之间的协同相互作用,并激活下游防御相关基因的表达,从而增强烟草的抗病性。本研究不仅证实了它们的核定位,还证明了WRKY6和WRKY23的表达水平在丁香假单胞杆菌侵染期间显著上调。病毒诱导的基因沉默介导的WRKY6和WRKY23沉默导致更严重的萎蔫症状,并且沉默植株中的细菌生物量显著低于野生型,表明烟草抗性增强。进一步的wrky6和wrky23突变体表现出增强的病原菌抗性,表现为病斑面积减小和活性氧(过氧化氢/超氧阴离子)过度积累。然而,WRKY6和WRKY23在活性氧信号中的调控机制仍未明确,需要深入探索它们在调控活性氧介导的植物免疫中的作用。共表达网络分析进一步揭示,WRKY6和WRKY23与氨基酸及其衍生物(包括L-苯丙氨酸和黄苷相关代谢物)表现出强相关性。研究表明,L-苯丙氨酸是苯丙烷途径的中心前体,是木质素生物合成的关键底物。木质素作为植物细胞壁的结构成分,通过其作为物理屏障的沉积来促进抗病性。例如,芽孢杆菌(Bacillussp.)JR48菌株通过增强水杨酸信号来引发系统抗性,同时增强了木质素的积累并激活了苯丙烷途径中的防御相关基因。值得注意的是,越来越多的证据强调了WRKY转录因子通过代谢重编程在协调植物免疫反应中的关键作用。这些发现强调了WRKY6/WRKY23在活性氧信号和特异性代谢物生物合成中的双重潜在调控作用。因此,未来的工作应优先阐明WRKY6/WRKY23与氨基酸衍生代谢物之间的分子互作,特别是它们在精细调控防御相关代谢途径和在病原菌侵染过程中协调氧化还原稳态中的作用。
结论
本研究系统地阐明了烟草在丁香假单胞杆菌侵染过程中被激活的多层防御机制。转录重编程的时间动态揭示了一种双相响应策略:病原菌入侵后,通过快速激活胁迫响应通路和激素信号(水杨酸、茉莉酸和生长素)实现防御优先;而关键次生代谢物生物合成通路(特别是生物碱和类黄酮)的持续诱导,则强调了它们在化学防御病原菌中的关键作用。几个WRKY、ERF和NAC转录因子在协调阶段特异性网络中的核心调控功能,进一步凸显了它们作为植物免疫关键节点的进化保守性。
WRKY6和WRKY23的功能验证证实了它们作为抗性负调控因子的作用,沉默这些基因增强了活性氧积累以及关键下游代谢物(如L-苯丙氨酸和黄苷)的水平。在沉默株系中观察到的病原菌生物量显著减少,不仅证实了它们的生物学意义,也确立了这两个转录因子作为精准育种的有前景靶点。然而,野生型植株中未能实现完全抗性,这表明存在额外的调控层级,可能涉及与未表征的转录因子家族的交互作用或转录后修饰。未来的研究应优先关注这些调控网络的时空分辨率,并验证它们在重要经济作物中的保守性。本工作为植物-病原菌互作提供了新的见解,并为通过分子育种策略培育下一代抗病烟草品种建立了坚实的框架。

END


获取此文献原文PDF、申请加入学术群,联系您所添加的任一微科盟组学老师即可,如未添加过微科盟组学老师,请联系多组学老师30,无需重复添加。
了解更多转录组知识,点击进入《转录组》
点击阅读原文,免费下载该SCI原文
