
原文链接:10.1021/acs.analchem.5c07853
在食品安全检测领域,快速、精准识别无反应活性位点的有毒污染物,一直是困扰科研人员的难题。棉酚作为棉花籽制品中常见的有毒酚类化合物,具有生殖毒性、心脏毒性等危害,严重威胁人体健康,其高效检测对保障食品安全至关重要。
近日,郑州大学李朝晖、孙元强团队新提出限制分子内弯曲(RIB)机制,设计出基于 BODIPY 的荧光分子 IPR,其与人体血清白蛋白(HSA)形成IPR@HSA 超分子探针,通过 HSA 疏水空腔限制 IPR 弯曲振动激活荧光;以有毒污染物棉酚为模型分析物,棉酚结合 HSA 引发变构效应,进一步强化 IPR 限制实现信号二次放大,该探针响应时间不足 10 秒,检测精度达微摩尔级别,为食品安全监控提供了全新工具。相关研究成果发表于《ACS Analytical Chemistry》上。
核心结论
l选取光稳定性优异、量子产率高的 BODIPY 为荧光团骨架,通过在中位引入空间位阻较大的异丙基,邻位引入甲基,构建出 IPR 荧光分子。这些 bulky 取代基会增强分子的低频弯曲振动,通过振动耦合促进非辐射衰减,使 IPR 在溶液中荧光几乎完全淬灭,处于 “暗态”,为后续 “点亮” 响应奠定基础。
l将 IPR 与人体血清白蛋白(HSA)结合,形成 IPR@HSA 超分子探针:HSA 的疏水空腔会对 IPR 形成物理限制,有效抑制其分子内弯曲振动,阻断非辐射衰减通道,使 IPR 荧光“点亮”,实现从“暗态”到“亮态”的转变。分子动力学模拟与 ONIOM 模型计算证实,IPR 与 HSA 以 2:1 比例结合,主要通过范德华力相互作用,HSA 空腔的空间 confinement 是荧光激活的关键。
l棉酚与 HSA 的 IB 位点特异性结合后,会引发 HSA 构象变化(变构效应),进一步收紧疏水空腔,加剧对 IPR 分子振动的限制,导致荧光强度二次增强。这种“组装激活 + 变构放大”的双重机制,让探针对棉酚的检测兼具高灵敏度与高特异性。
佐证方法
l计算模拟:借助 Gaussian 16、GAMESS 等软件,通过量子化学计算明确非辐射跃迁路径,结合分子对接、100 ns 动力学模拟及 IGMH 分析,验证 RIB 机制与 IPR-HSA 结合模式及稳定性。
l结构表征: Bruker 核磁共振仪获取¹H/¹³C NMR 谱图验证 IPR 结构,通过 XPS 分析电子转移路径,结合 Job’s plot 确定 IPR 与 HSA 2:1 的结合比例,完成探针与复合物结构确认。
l性能测试:通过 UV-vis、荧光光谱等验证探针光学性能与“turn-on”响应,开展 pH、光稳定性及抗干扰测试,结合粘度响应与时间分辨荧光测试,佐证 RIB 机制与检测能力。
l实际样品验证:对猪肉样品经匀浆、提取、浓缩等前处理后,采用 HPLC 辅助加标回收实验,在 0.5-4 μM 浓度下,回收率 80.72%-119.49%,验证实际应用准确性。
图文说明
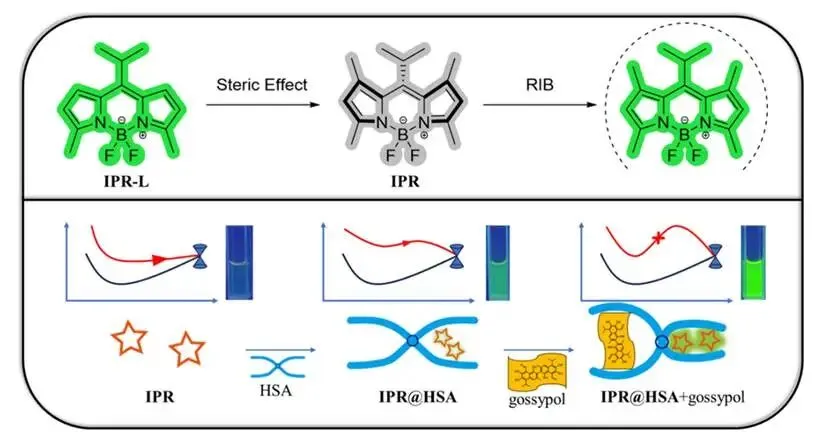
方案 1. 基于 RIB 策略的 IPR@HSA 超分子荧光探针用于棉酚检测的示意图。
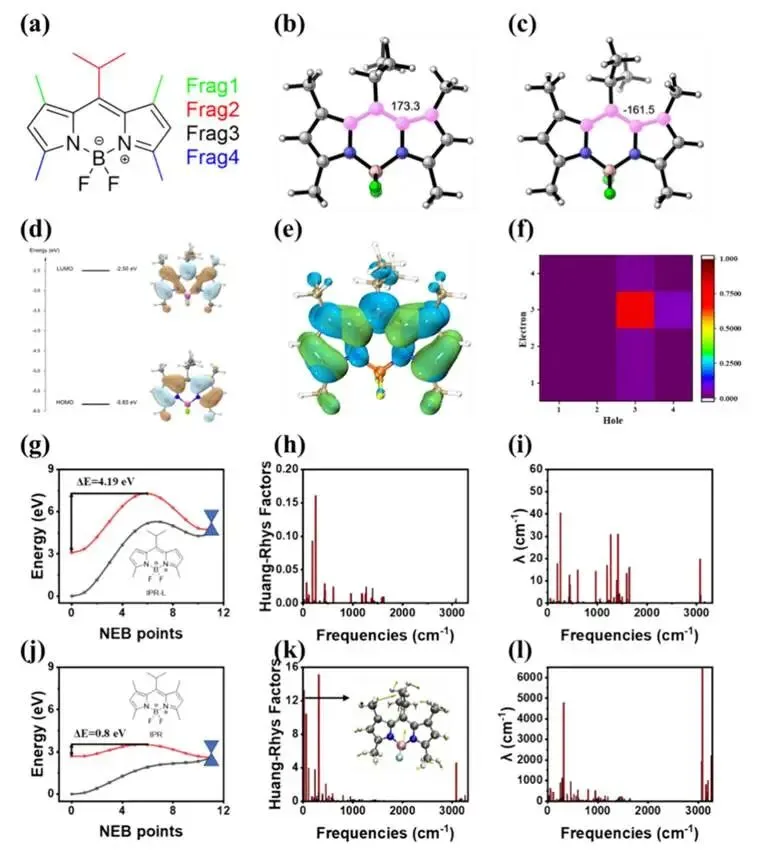
图 1. IPR 的结构与电子性质(a) 用于片段间电荷转移(IFCT)分析的 IPR 化学结构及片段标注:片段 1(绿色)、片段 2(红色)、片段 3(黑色)和片段 4(蓝色);(b, c) 优化后的(b)基态(S₀)和(c)第一激发态(S₁)分子几何结构;(d) 前线分子轨道与能级图;(e) 空穴 - 电子分析图,展示电子激发过程中电子(绿色)和空穴(蓝色)的分布;(f) 电荷转移矩阵热图,量化由 IFCT 分析得到的分子片段间的分子内电荷转移;(g-l) IPR-L 与 IPR 的光学性质计算结果:(g, j) 通过生成弗兰克 - 康登(FC)点与锥形交叉点(CI)之间的弹性带(NEB)插值路径得到的(g)IPR-L 和(j)IPR 的能量曲线,每个点均进行能量计算;(h, k) 分别为(h)IPR-L 和(k)IPR 在不同振动频率下的黄 - 里斯因子(Huang-Rhys factor);(i, l) 分别为(i)IPR-L 和(l)IPR 的重组能(λ)随振动频率的分布曲线;(l)中的插图为简正模式向量,指示电子态与振动态之间的主要耦合路径。
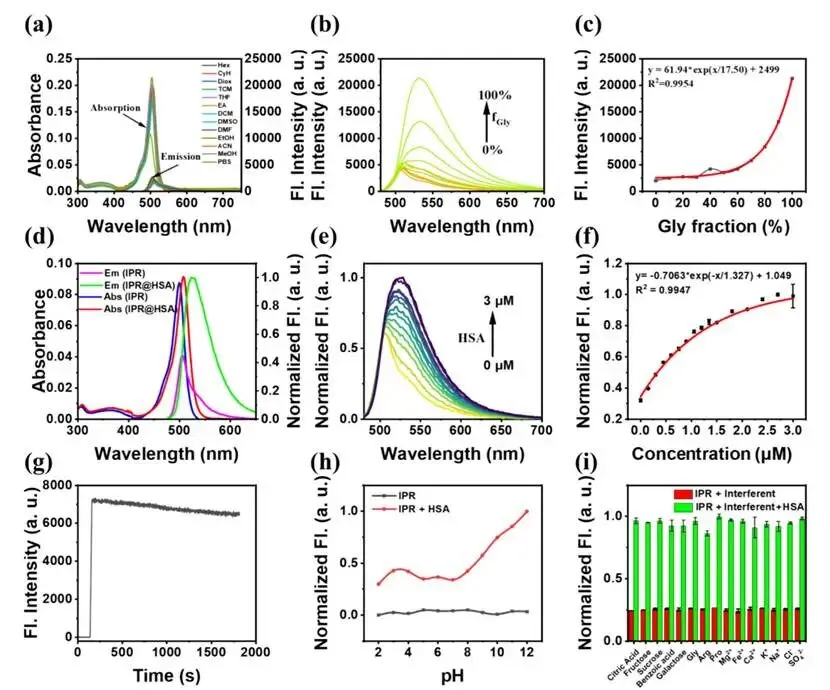
图 2.(a) 4 μM IPR 在有机溶剂和水相溶剂中的吸收 - 发射光谱。(b) 4 μM IPR 在甘油 / 磷酸盐缓冲液(Gly/PBS)中的荧光光谱。(c) 激发波长 λₑₓ=460 nm 时,IPR 在 532 nm 处的荧光强度随甘油体积分数的变化曲线。(d) 有无人体血清白蛋白(HSA)存在时,IPR 的吸收光谱与发射光谱。(e) 磷酸盐缓冲液(PBS)中,4 μM IPR 的归一化荧光光谱;(f) HSA 浓度(0-3 μM)与 4 μM IPR 归一化发射强度的线性关系图。(g) 4 μM IPR 对 1.0 mg/mL HSA 的时间依赖性光谱。(h) 在 pH 2-12 的布里顿 - 罗宾逊缓冲液(B-R 缓冲液)中,4 μM IPR 与 3.0 μM HSA 体系的归一化发射强度。(i) 激发波长 λₑₓ=460 nm 时,IPR 对 HSA 相对于干扰物质的选择性。
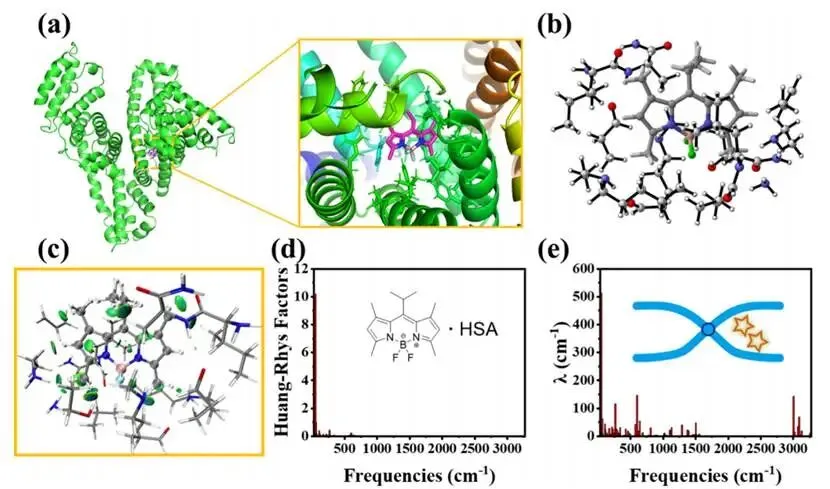
图 3. IPR@HSA 超分子复合物的结合位点表征(a) 分子对接结构图,显示 IPR 结合于 IIA 口袋内;(b) ONIOM(M06-2X-D3/6-31g (d):PM6-D3)优化后的簇模型细节图,该模型包含 IPR 周围半径 6 Å 范围内的原子(原文 "ONIOM (M062X-D3/6-31g (d):PM6D3)" 补全规范格式为 "ONIOM(M06-2X-D3/6-31g (d):PM6-D3)");(c) 基于 Hirshfeld 划分的独立梯度模型(IGMH)分析可视化 IPR@HSA 簇模型的弱相互作用,其中波函数在 M06-2X-D3/6-31g (d) 水平下获得;(d, e) IPR@HSA 簇模型的振动耦合计算结果,分别为黄 - 里斯因子(Huang-Rhys factor)和重组能(λ)随振动频率的分布曲线。
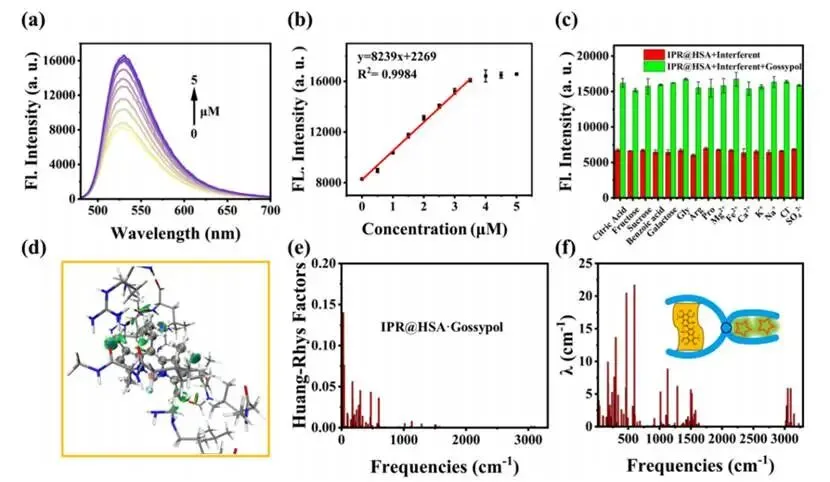
图 4.(a) 加入不同浓度棉酚后,IPR@HSA 复合物的发射光谱;(b) 532 nm 处荧光强度与所加棉酚浓度的线性关系图;(c) 激发波长 λₑₓ=460 nm 时,IPR@HSA 用于棉酚检测的选择性与抗干扰性评估;(d) 基于 Hirshfeld 划分的独立梯度模型(IGMH)分析,可视化棉酚结合型 IPR@HSA 簇模型的弱相互作用,其中波函数在 M06-2X-D3/6-31g (d) 水平下获得;(e, f) 棉酚结合型 IPR@HSA簇模型的振动耦合计算结果,分别为黄 - 里斯因子(Huang-Rhys factor)和重组能(λ)随振动频率的分布曲线。
科研服务