图1E1激活泛素并传递给E2,E3将泛素转移到底物,DUB则切除泛素链逆转降解。该流程是泛素化研究的标准图谱,为靶向E3/DUB药物研发提供了基础。
图1.泛素化与去泛素化过程发生于泛素-蛋白酶体系统中
图2 直观展示了泛素链的多样性,包括K48(降解)、K63(信号、自噬)、M1(线性、炎症)等多种连接方式。这论证了UPS能够通过不同的“泛素密码”向细胞传递不同的指令,从而参与从蛋白周转、DNA修复、炎症信号到代谢调控等几乎所有的生命活动。
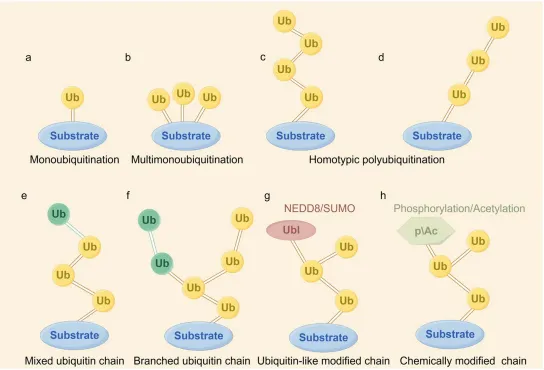 图2.各种泛素连接方式如下所示
图2.各种泛素连接方式如下所示
这是综述的主体和核心论证。文章以“持续增殖、抵抗死亡、代谢重编程、免疫逃逸” 等14个癌症特征为纲,逐一、系统地阐述了UPS在每个特征中的具体作用机制。
图3 以UPS为中心,辐射连接各个癌症特征,可视化了UPS作为“网络枢纽”的核心论点。
表1 是支撑这一论点的海量证据库。它以表格形式,穷举式地汇总了调控每个癌症特征的E3连接酶、去泛素化酶(DUB)、它们的底物、涉及的癌症类型和功能结果。
例如,在“持续增殖信号”特征下,可查看到Cbl降解EGFR、FBXW7降解c-Myc等具体机制;在“避免免疫摧毁”特征下,可查看到SPOP降解PD-L1、USP22稳定PD-L1等关键发现。
表1.癌症特征调控过程中的E2酶、E3连接酶及去泛素化酶
图4 泛素化调控凋亡、焦亡、铁死亡:IBRDC2/Cbl抑制凋亡;TRIM31等抑制焦亡、USP48促进焦亡;TRIM26促铁死亡、OTUB1抑铁死亡。靶向E3/DUB可调节死亡敏感性,如化疗联用OTUB1抑制剂。
图4.泛素-蛋白酶体系统通过多种机制在抵抗细胞死亡中发挥关键作用
图5 系统展示了UPS如何靶向调控糖酵解(HK2, PKM2)、脂质合成(ACC1, FASN)、谷氨酰胺代谢(GDH1)等代谢通路中的关键限速酶。
例如,E3连接酶MARCH8降解HK2抑制糖酵解,而DUB USP7稳定HK2促进Warburg效应。这论证了UPS是癌细胞“代谢开关”的直接操控者。
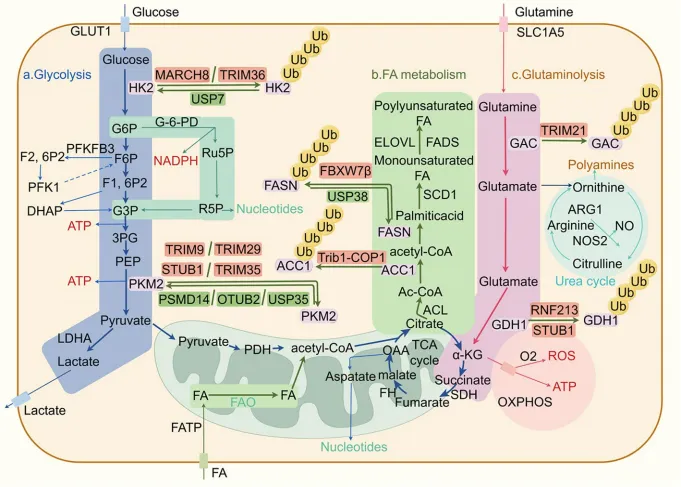 图5.泛素-蛋白酶体系统通过多种途径调控肿瘤代谢
图5.泛素-蛋白酶体系统通过多种途径调控肿瘤代谢
图6 重点阐释了UPS如何塑造免疫抑制性肿瘤微环境,特别是通过调控核心免疫检查点蛋白PD-L1的稳定性。
图示表明,一个由SPOP、FBXO22等E3连接酶驱动的“降解轴”和一个由USP22、CSN5等DUB驱动的“稳定轴”共同决定了PD-L1的蛋白水平,从而影响免疫逃逸。这为“联合DUB抑制剂与PD-1/PD-L1抗体”的疗法提供了理论基础。
图7 从蛋白酶体抑制剂(硼替佐米等)到E1抑制剂(pevonedistat)再到PROTAC(ARV-110/471进入II期临床),UPS靶向治疗已迈向精准降解。研究者可据此设计或寻找目标蛋白的PROTAC分子。
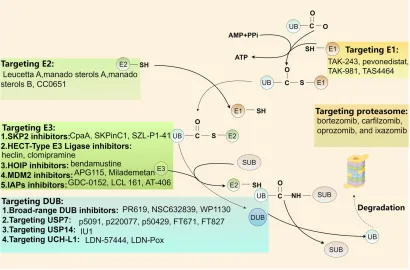
图7.泛素-蛋白酶体系统调控蛋白质作用机制示意图及其对应治疗策略