Cell Press头条 | 郑州大学于政权团队揭示"熬夜伤肠胃"的完整神经调控机制:迷走神经背运动核 -迷走神经-5-羟色胺轴调控肠道干细胞
睡眠作为维持人体稳态的核心生理过程,其紊乱已成为全球性公共卫生挑战。据统计,全球约 10% 的成年人受失眠困扰,而睡眠不足不仅与全因死亡率升高相关,更被证实是炎症性肠病(IBD)、肠易激综合征(IBS)等慢性胃肠疾病的重要风险因素。长期以来,科学界已知肠道是睡眠障碍的关键靶器官,但脑内异常神经信号如何跨越 “血脑屏障” 传递至肠道、进而调控肠道功能的分子机制始终悬而未决。

2026 年 2 月 5 日,郑州大学在线发表于 Cell 子刊 Cell Stem Cell的研究论文:“Sleep disturbance triggers aberrant activation of vagus circuitry and induces intestinal stem cell dysfunction ”登上了 Cell Press 头条。该研究首次揭示了 “迷走神经背运动核(DMV)- 迷走神经 - 5 - 羟色胺(5-HT)” 轴介导的脑 - 肠信号通路,阐明了睡眠剥夺(SD)通过该通路损伤肠道干细胞(ISC)功能的核心机制,为睡眠相关胃肠疾病的治疗提供了全新靶点。

郑州大学生命科学学院于政权团队、中国科学院深圳先进技术研究院脑认知与脑疾病研究所王枫、中国农业大学吕聪及美国加州大学欧文分校 Maksim V. Plikus 为论文共同通讯作者,郑州大学张明鑫博士,中国农业大学吴茜博士和博士生刘笛为论文共同第一作者,郑州大学为论文第一单位。
一、研究背景:聚焦脑 - 肠轴的 “睡眠 - 肠道” 调控空白
肠道不仅是消化器官,更是人体最大的内分泌和免疫器官,其上皮层的快速更新与损伤修复依赖于肠道干细胞(ISC)的自我更新和谱系分化能力。ISC 位于肠隐窝基底,被称为肠道稳态的 “守护者”,其功能异常直接导致肠道屏障受损、炎症加剧,是 IBD 等疾病的核心病理基础。此前研究发现,睡眠剥夺会特异性导致肠道活性氧(ROS)积累,但这一现象背后的神经调控通路完全未知。
同时,肠道是体内5-HT(也叫血清素)的主要合成场所(占全身 95%),由肠道内神经内分泌细胞——肠嗜铬(EC)细胞产生,其水平失衡与多种胃肠疾病密切相关。但传统观点认为,肠道 5-HT 的调控主要依赖肠道菌群和局部微环境,中枢神经系统如何远程调控肠道 5-HT 稳态尚未被揭示。此外,迷走神经作为脑 - 肠轴的核心传导通路,其背运动核(DMV)虽被证实参与应激反应调控,但睡眠障碍是否通过 DMV - 迷走神经通路影响肠道功能,仍缺乏直接证据。
基于上述研究空白,该团队提出核心科学问题:睡眠剥夺如何通过中枢神经信号调控肠道 ISC 功能?其关键传导通路和分子靶点是什么?
二、关键研究结果:层层递进解析睡眠剥夺的肠道损伤效应
(一)急性睡眠剥夺特异性损伤肠道干细胞功能,且损伤具有持续性
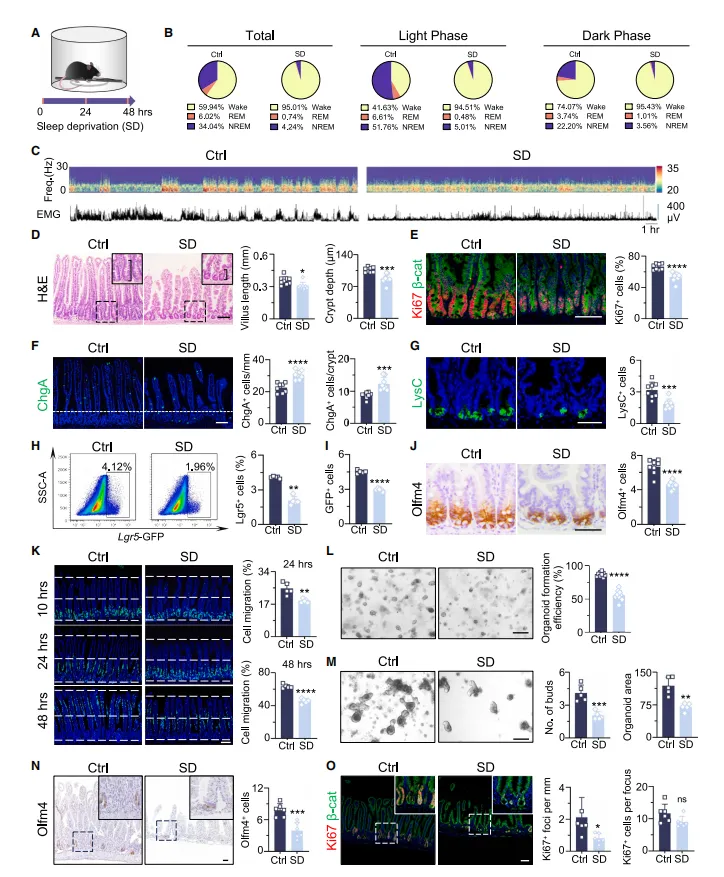
研究团队采用两种经典睡眠剥夺模型(机械性干扰和多平台水浴法)对小鼠进行 2 天造模,结果显示:小鼠快速眼动(REM)睡眠从 6.02% 降至 0.74%,非快速眼动(NREM)睡眠从 34.04% 降至 4.24%,睡眠结构被严重破坏。伴随睡眠剥夺,小鼠肠道出现显著病理改变:肠隐窝 - 绒毛结构缩短,Paneth 细胞数量减少,EC 细胞异常扩增,肠道上皮增殖能力下降、凋亡增加,且这些变化在小肠近 / 中段最为显著,呈现区域特异性。
更关键的是,睡眠剥夺导致 Lgr5⁺ ISC 和 Olfm4⁺干 / 祖细胞数量显著减少,且 Olfm4⁺细胞的减少持续 7 天,表明 ISC 功能损伤具有长效性。功能验证实验证实,睡眠剥夺小鼠的肠隐窝类器官形成能力、出芽能力显著下降,经 12 Gy γ 射线辐射后的肠道再生灶数量减少,直接证明 ISC 的自我更新和损伤修复能力受损。值得注意的是,抗生素清除肠道菌群后,睡眠剥夺仍能诱导上述肠道病变,表明该过程不依赖肠道菌群,而是由神经 - 内分泌信号直接调控。
(二)睡眠剥夺通过 ROS 过量积累激活 ISC 的翻译应激反应
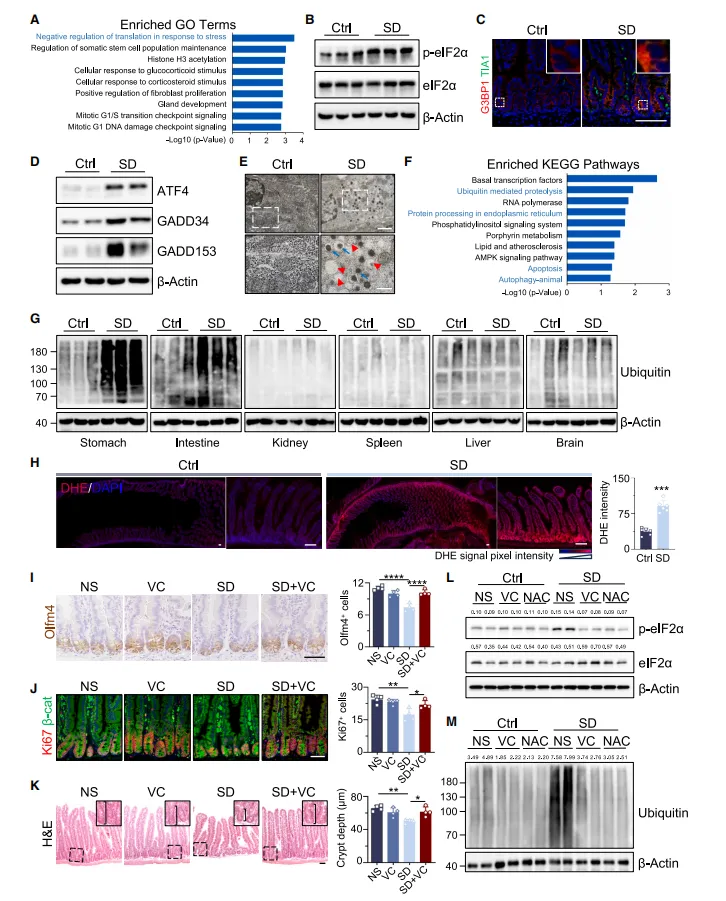
为解析 ISC 功能损伤的分子机制,研究团队对睡眠剥夺小鼠的肠隐窝进行蛋白组学分析,发现差异蛋白显著富集于 “应激反应的翻译负调控” 和 “干细胞群维持” 通路。进一步实验证实,睡眠剥夺会导致 ISC 中翻译应激核心分子 p-eIF2α 显著上调,形成大量应激颗粒,同时 ATF4、GADD34 等整合应激反应(ISR)关键分子表达升高,触发自噬和 K48 依赖的蛋白降解。
深入研究发现,睡眠剥夺会导致肠道 ROS 特异性过量积累,伴随 DNA 损伤增加、抗氧化能力下降。而补充维生素 C(VC)或 N - 乙酰半胱氨酸(NAC)等抗氧化剂,可有效清除 ROS,逆转 ISC 的翻译应激和功能异常,证实 ROS 过量积累是 ISC 功能损伤的关键上游诱因。
(三)肠道 5-HT 骤升是介导 ISC 损伤的核心信号分子
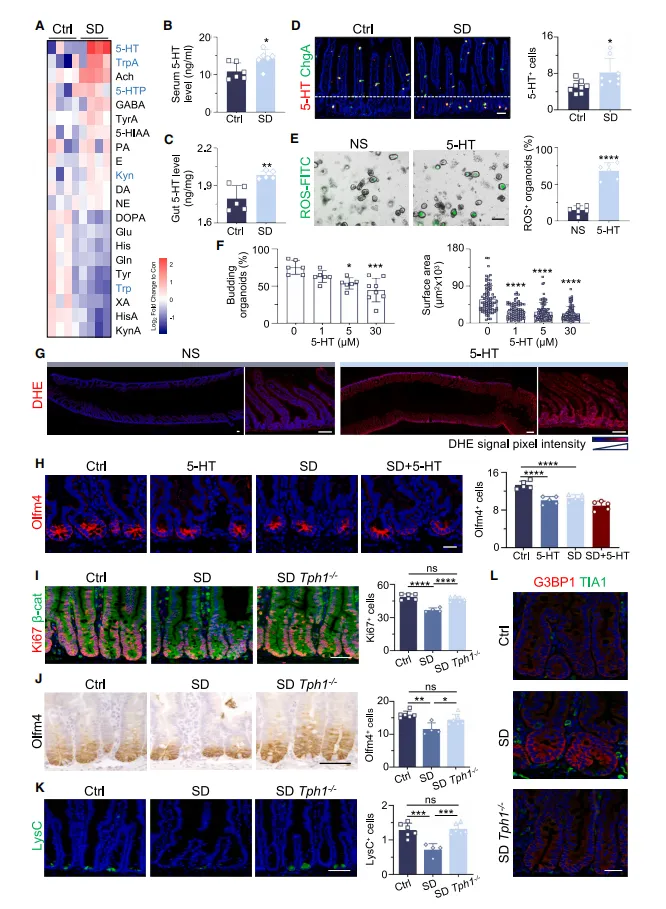
通过 LC-MS/MS 靶向代谢组学分析,研究团队发现睡眠剥夺小鼠肠道的 5-HT 水平显著升高,且血清 5-HT 水平经 ELISA 验证同步上升。体外实验显示,5-HT 以剂量依赖方式抑制肠类器官增殖和出芽,诱导 ROS 积累;体内注射 5-HT 可完全模拟睡眠剥夺的肠道病变,证实 5-HT 的直接损伤作用。
为明确 5-HT 的来源,研究团队采用 Tph1 敲除小鼠(肠道 5-HT 合成缺失)进行验证,结果显示:Tph1 敲除小鼠在睡眠剥夺后,肠道 ISC 数量、隐窝 - 绒毛结构、氧化应激水平均接近正常,完全抵抗了睡眠剥夺的肠道损伤效应。进一步机制研究发现,睡眠剥夺不仅促进 EC 细胞合成 5-HT,还通过抑制 Slc6a4 基因(编码 5-HT 重摄取转运体 SERT)的表达,减少 5-HT 重摄取,最终导致肠道 5-HT“合成增加 + 清除减少” 的双重骤升。
(四)ISC 通过 HTR4 受体感知 5-HT 信号,HTR4 是关键靶点
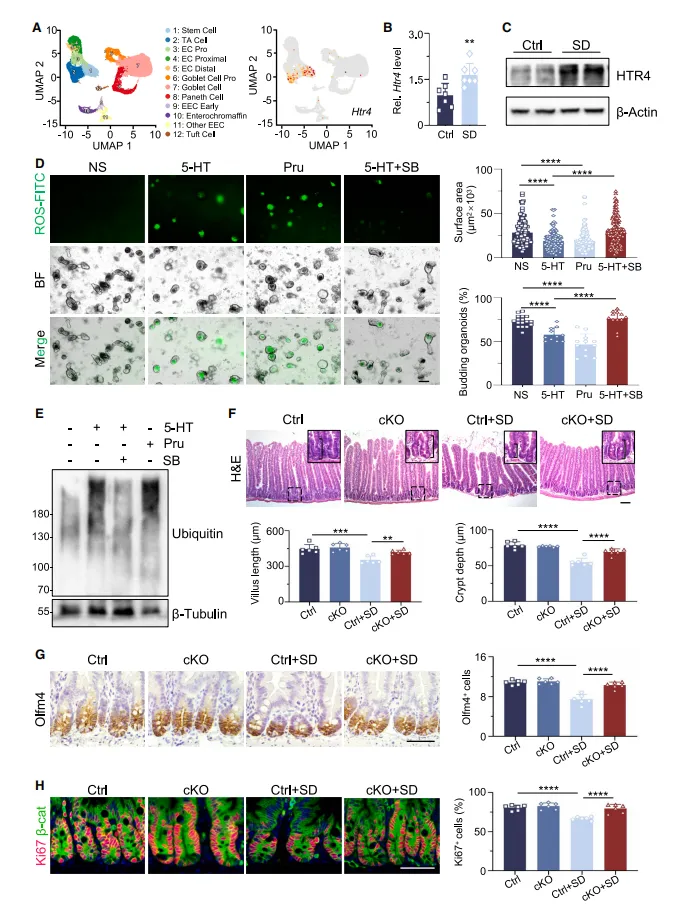
单细胞 RNA 测序分析显示,Htr4 是 ISC 上表达的主要 5-HT 受体,且睡眠剥夺会显著上调肠道隐窝中 HTR4 的转录和蛋白水平。功能验证证实,HTR4 激动剂普卡必利可模拟 5-HT 的损伤效应,抑制肠类器官生长并诱导 ROS 积累;而 HTR4 拮抗剂 GR113808 或 SB203186 可有效阻断 5-HT 的作用,逆转睡眠剥夺诱导的 ISC 功能异常。
更具说服力的是,肠道上皮特异性 Htr4 条件性敲除小鼠,在睡眠剥夺后未出现 ISC 功能损伤和肠道病理改变,其肠道 5-HT 水平虽升高,但无法传递至 ISC,证实 HTR4 是 5-HT 介导 ISC 损伤的唯一受体。
(五)迷走神经 - 乙酰胆碱(ACh)通路介导脑 - 肠信号传递
为明确中枢神经信号的传导通路,研究团队首先排除了交感神经系统(SNS)和下丘脑 - 垂体 - 肾上腺(HPA)轴的作用:睡眠剥夺小鼠的血清去甲肾上腺素、皮质醇水平无显著变化,化学消融交感神经或调控糖皮质激素受体均无法逆转肠道损伤。
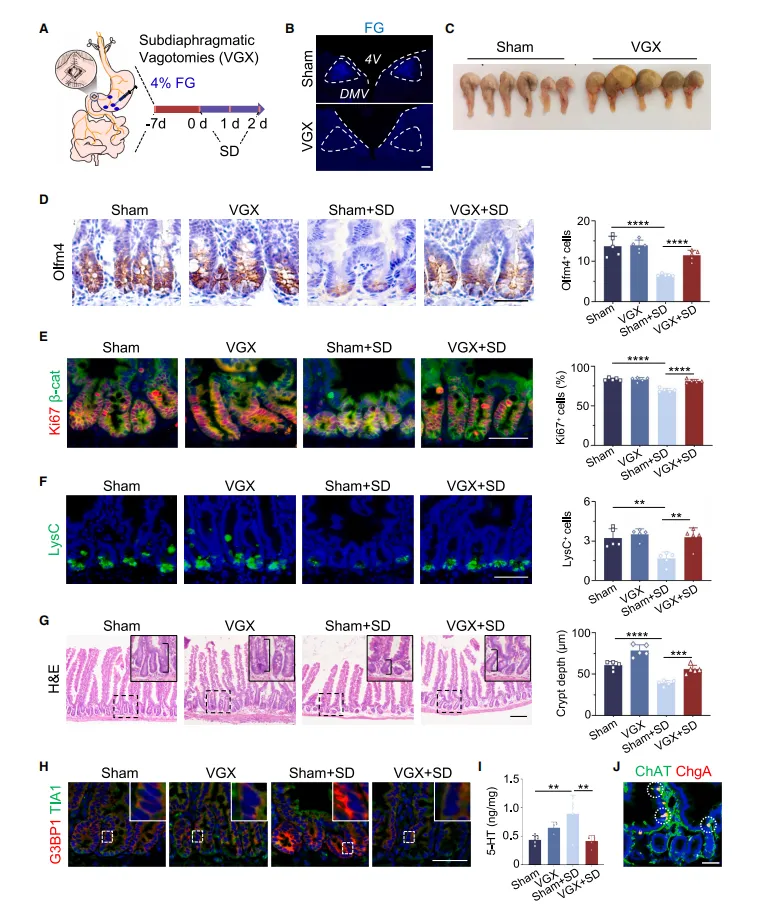
随后,膈下双侧迷走神经切断术(VGX)实验给出关键证据:迷走神经切断后,睡眠剥夺小鼠的 5-HT 水平恢复正常,ISC 功能和肠道结构损伤被完全阻断,证实迷走神经是脑 - 肠信号传递的唯一通路。
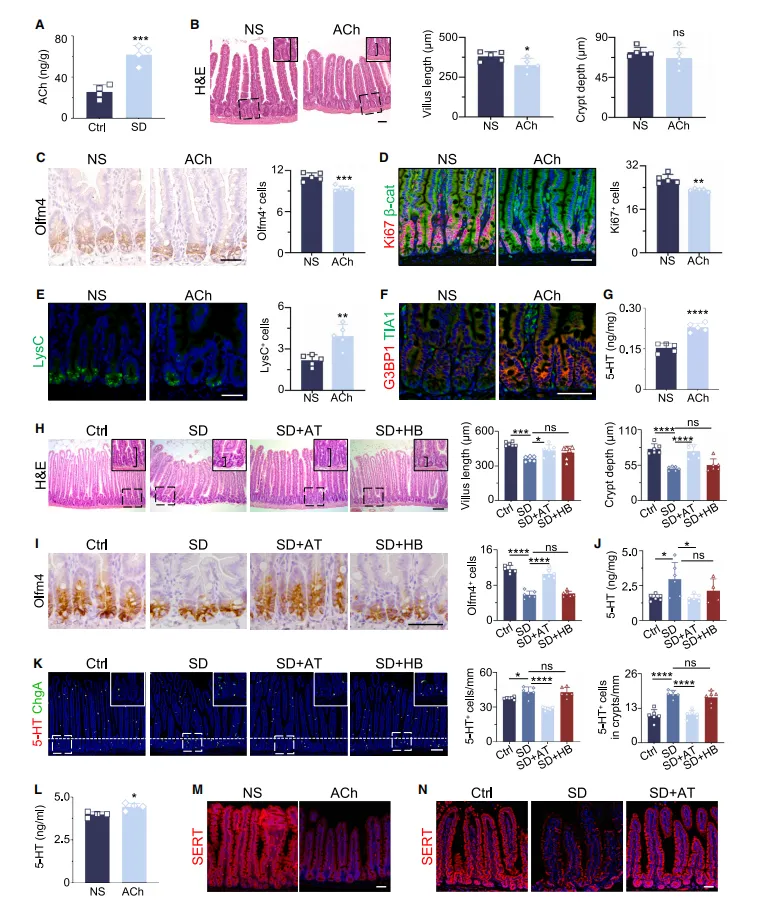
进一步研究发现,睡眠剥夺会导致肠道 ACh 水平显著升高,体内注射 ACh 或其类似物卡巴胆碱,可模拟睡眠剥夺的肠道病变;而毒蕈碱受体拮抗剂阿托品(AT)能有效阻断这一效应,烟碱受体拮抗剂则无作用,表明 ACh 通过毒蕈碱受体发挥作用。肠道上皮特异性 Chrm3 敲除小鼠的验证结果显示,Chrm3 是 ACh 的主要作用受体,其缺失可完全抵抗睡眠剥夺诱导的 5-HT 骤升和肠道损伤。
(六)DMV 是睡眠剥夺的中枢感知靶点,异常激活具有长效性
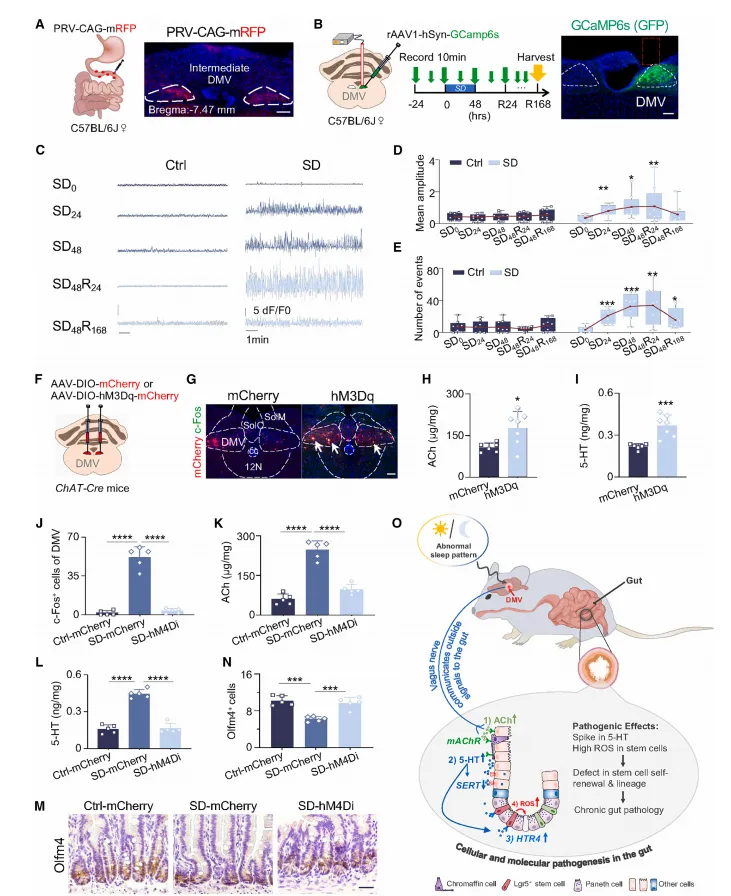
通过 c-Fos 免疫荧光染色和 PRV 病毒逆行追踪,研究团队发现:睡眠剥夺会激活脑内多个核团,但仅 DMV 是同时被激活且与肠道存在神经连接的核团。光纤光度法记录显示,睡眠剥夺后 DMV 神经元的钙信号频率和振幅显著升高,且这一异常活性持续 7 天,与 ISC 功能损伤的持续性一致。
化学遗传学实验进一步证实:激活 DMV 神经元可诱导肠道 ACh 和 5-HT 骤升,模拟睡眠剥夺的肠道病变;而抑制 DMV 神经元则能有效逆转睡眠剥夺诱导的 ACh/5-HT 升高和 ISC 功能异常,最终证实 DMV 是睡眠剥夺调控肠道功能的中枢核心。
三、核心分子机制:构建 “DMV-ACh-5-HT-HTR4” 调控通路
综合所有研究结果,团队提出完整调控模型:
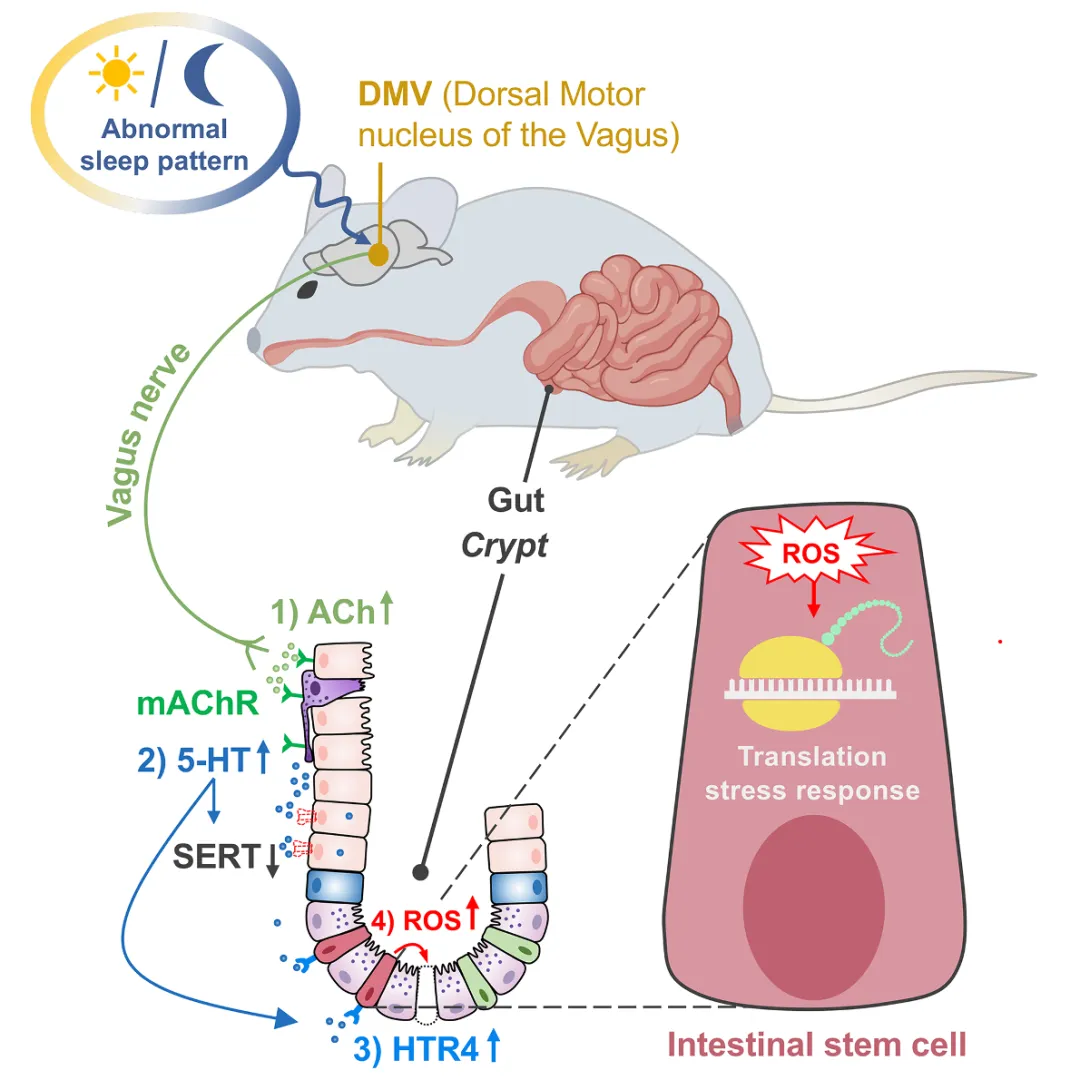
这一通路清晰揭示了睡眠障碍从 “中枢神经” 到 “肠道干细胞” 的信号传递链条,首次将 DMV、迷走神经、ACh、5-HT、HTR4 等关键节点串联成完整的神经 - 内分泌调控网络。
四、潜在治疗策略:突破传统认知,具有明确转化价值
基于核心机制,研究团队筛选出三类可缓解睡眠相关肠道损伤的潜在药物:阿托品(阻断 Chrm3)、GR113808(阻断 HTR4)、维生素 C/NAC(清除 ROS),且这些药物均为临床常用药或安全营养素,具有良好的转化前景。同时,该研究为睡眠障碍相关胃肠疾病的治疗提供了 “中枢 - 外周” 双重靶向思路,突破了传统对症治疗的局限。
该研究通过多学科交叉技术,从分子、细胞、组织到整体层面,系统解析了睡眠剥夺损伤肠道干细胞功能的神经 - 内分泌机制,不仅填补了脑 - 肠轴调控领域的研究空白,更为睡眠相关胃肠疾病的精准治疗提供了全新靶点和策略。未来,随着对 DMV 上游调控通路、HTR4 下游信号分子等方向的深入探索,有望进一步完善这一调控网络,为开发更高效的治疗方案奠定基础。同时,该研究也提醒我们,改善睡眠质量可能是预防和辅助治疗慢性胃肠疾病的重要手段,为临床实践提供了全新视角。
本文原创仅指编译原创,文献内容与图片版权归原著所有,文献解读仅用于学术分享,如有侵权请与后台联系
关注公众号了解更多医院招聘、科研快讯、文献解读和期刊选择相关内容

本公司致力于课题设计、项目申报、组学分析、细胞实验、动物实验、论文指导等多项科研服务,扫描下方二维码可免费咨询
