郑州大学第一附属医院杨建军等团队AM!!仿生工程化病毒模拟囊泡用于增强STING激动剂向树突状细胞的胞质递送
- 2026-03-24 00:59:38

肿瘤免疫治疗面临的核心挑战之一是"冷肿瘤"问题,即免疫抑制性肿瘤微环境阻碍了抗原呈递和T细胞 priming 过程。STING(干扰素基因刺激因子)信号通路作为连接先天免疫与适应性免疫的关键节点,能够将免疫"冷"肿瘤转化为"热"肿瘤,因而成为癌症免疫治疗的重要靶点。环二核苷酸(CDN)类STING激动剂如ADU-S100已进入临床试验阶段,但其临床转化受限于两大瓶颈:一是CDN带有双负电荷,难以穿透细胞膜进入胞质激活STING受体;二是STING蛋白在多种细胞类型中广泛表达,非特异性激活可导致T细胞凋亡、调节性B细胞增殖及免疫检查点分子上调,反而促进免疫逃逸。树突状细胞(DCs),特别是I型常规树突状细胞(cDC1s),因其卓越的抗原交叉呈递能力和T细胞 priming 功能,被认为是STING激动剂的最优靶细胞。然而,如何实现CDN向cDC1s的特异性靶向递送,同时确保高效的内涵体逃逸,仍是该领域亟待解决的关键科学问题。
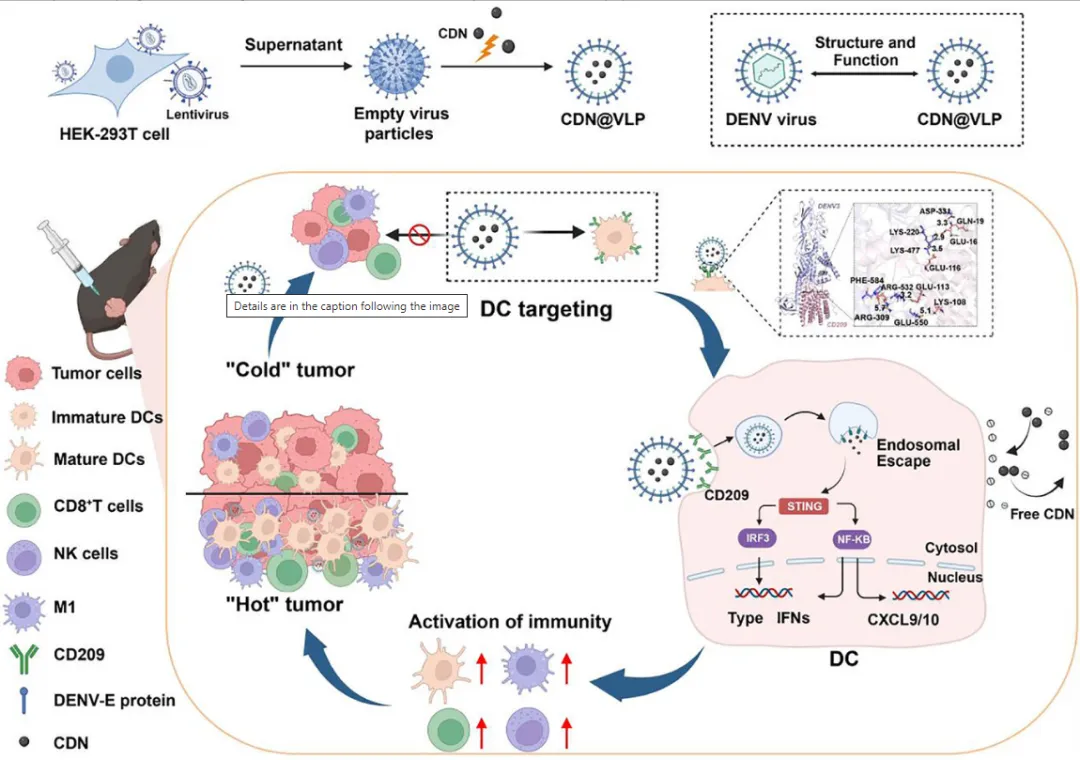
在这项研究中,研究人员开发了一种基于登革病毒(DENV)的病毒样颗粒(VLP)递送平台,用于实现STING激动剂向树突状细胞的精准胞质递送。研究团队利用DENV-2型prM/E基因构建稳定表达细胞系,通过蔗糖密度梯度离心纯化获得直径约50 nm的VLP2,并采用电穿孔技术将CDN(ADU-S100)封装其中,载药效率达75.72%。通过系统筛选四种DENV血清型(VLP1-4),研究发现DENV3型VLP3具有最优的DC靶向能力,其E蛋白与DC表面受体DC-SIGN(CD209)的结合自由能最低(-156.09 kcal/mol),较VLP2提升2.3倍cDC1靶向积累。机制研究表明,VLP通过DC-SIGN介导的内吞作用进入DCs,随后在酸性内涵体环境中E蛋白构象改变触发膜融合,实现内涵体逃逸和胞质释放。在B16F10黑色素瘤模型中,瘤内注射5 μg CDN@VLP3即可实现97.26%的肿瘤抑制率,较游离CDN提升疗效40倍且无剂量限制性毒性。转录组分析进一步揭示,CDN@VLP3通过上调XCL1、CCL4和CCL5等关键趋化因子,促进cDC1向肿瘤的募集,形成"招募-摄取-激活"的正反馈环路。此外,该平台与抗PD-1抗体联用可产生协同抗肿瘤效应,静脉给药亦显示良好疗效和安全性。
该研究建立的CDN@VLP平台通过仿生模拟登革病毒天然嗜性,成功解决了STING激动剂临床应用中效力与特异性的权衡难题。该平台的核心优势体现在三个层面:在靶向层面,VLP3通过E蛋白与DC-SIGN的高亲和力结合,实现cDC1特异性摄取,同时减少CD8+ T细胞的非特异性内吞(降低14.8倍),避免T细胞耗竭;在递送层面,病毒源性E蛋白介导的内涵体逃逸机制确保CDN高效进入胞质,激活STING通路,诱导I型干扰素持续产生(IFN-β提升12.8倍);在免疫调控层面,该平台不仅直接激活cDC1,还通过趋化因子网络促进其肿瘤浸润,重塑免疫微环境。研究还证实该平台具有良好的淋巴引流能力和全身给药潜力,为转移性肿瘤治疗提供了新策略。该工作为STING激动剂的临床转化建立了可推广的范式,也为其他需细胞特异性递送的生物制剂(如疫苗、基因治疗载体)提供了重要的技术参考。未来研究可进一步优化VLP表面修饰(如PEG化)以降低潜在免疫原性,拓展其重复给药的应用场景。

自然基金本子没思路,不知道怎么写?强烈推荐自然基金项目申报书参考范文合集。
1. 基于高熵金属氧化物的析氢析氧反应电催化剂 设计及多元活性位点协同效应研究
2. 原位构筑异质结阵列调控氧化物固态电解质晶 界空间电荷层及其全固态电池性能研究
3. 面向快充锂金属电池的梯度结构石榴石电解质设计及其界面应力自适应机制研究
4. 非晶氧化物无序局域环境对钌单原子电子结构 的精准调控及其析氧反应路径重构研究
5. 基于表面原子层修饰的高分辨率光催化材料的动态电子结构调控及其光电催化机制
6. 多轴应变下KNN外延薄膜的铁电畴结构演化与极化翻转动力学研究
7.面向高稳定钾离子电池的层状氧化物正极电解液界面原位构筑与动态演化机制研究


说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《材料研究进展》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
投稿邮箱:materials_mse@foxmail.com
