2026年2月,郑州大学第五附属医院团队在期刊《World Journal of Gastrointestinal Oncology》(IF:2.5)在线发表题为:Taurine suppresses gastric intestinal metaplasia in patient-derived organoids and Atp4a -/- mice的高水平研究论文。
背景:胃肠化生(GIM)是慢性胃炎进展为胃癌过程中的关键癌前病变,目前治疗选择有限。越来越多的证据表明,牛磺酸作为一种细胞保护性氨基酸,可能调节胃上皮功能障碍。然而,其在GIM背景下的应用和效果尚不清楚。
目的:利用患者来源类器官和Atp4a-/-小鼠模型研究牛磺酸对GIM的治疗作用。
方法:选用来源于患者的GIM类器官(n = 3)和会自发发生GIM的Atp4a-/-小鼠作为实验模型。通过阿尔新蓝-过碘酸希夫(Alcian blue-PAS)染色评估形态学变化。通过定量PCR、西方印迹和免疫组化检测胃上皮标志物MUC5AC及GIM相关标志物(尾型同源盒基因2 [CDX2]、MUC2、三叶因子家族3 [TFF3])的表达水平。
结果:我们确认,牛磺酸治疗显著缓解了Atp4a-/-小鼠的病理变化,包括腺体肥大和空泡扩张,并减轻了GIM的严重程度,相比未处理模型组,差异显著。在牛磺酸治疗下,MUC5AC表达显著增加,而肠特异性标志物CDX2、MUC2和TFF3表达下降(P < 0.05)。同时,在患者来源的GIM类器官中,牛磺酸治疗显著改善了GIM特征,表现为MUC5AC表达增加,以及CDX2、MUC2和TFF3表达下降。
结论:本研究强调了牛磺酸作为GIM治疗潜在药物的应用前景,为其临床管理提供了有希望的策略。
1. 首次系统验证牛磺酸对胃上皮肠化生(GIM)的治疗作用,填补该领域研究空白。
2. 采用Atp4a-/-基因敲除小鼠自发GIM模型与患者来源类器官双模型策略,兼顾机制研究与临床转化相关性。
3. 证实牛磺酸通过双向调控机制逆转GIM:下调肠道标志物CDX2、MUC2、TFF3,同时上调胃标志物MUC5AC,恢复胃上皮身份。
4. 成功建立并表征人源GIM类器官模型,为GIM研究提供可靠的体外人源实验平台。
5. 揭示牛磺酸作为安全、廉价、易获取的膳食补充剂或药物干预手段,为胃癌化学预防提供具有临床转化潜力的新策略。
胃癌是全球高发恶性肿瘤,胃上皮肠化生(GIM)作为Correa级联反应中的关键癌前病变,其年进展率可达0.25%-10%,中国成人患病率高达23%。目前临床缺乏有效逆转GIM的治疗手段,仅局限于幽门螺杆菌根除和内镜监测。牛磺酸作为一种条件性必需氨基酸,具有细胞保护、抗氧化和代谢调节等多重生物学功能,近期研究提示其在结直肠癌、肺癌等多种肿瘤中发挥抑癌作用,但其在GIM这一关键癌前阶段的调控作用尚未被探索。
传统细胞系难以模拟体内生理病理环境,而三维类器官技术能忠实保留组织来源的功能与分子特征,为消化系统疾病研究提供强大工具,但GIM来源的类器官模型仍较为稀缺。Atp4a-/-小鼠因H+-K+-ATP酶α亚基缺失导致慢性无胃酸症,可自发产生GIM病理改变,是研究GIM发病机制和药物筛选的可靠动物模型。
本研究基于此背景,首次系统评估牛磺酸在GIM中的治疗潜力,采用基因工程小鼠模型联合患者来源类器官的双模型策略,以期为GIM的临床干预提供新思路。
1. 动物模型构建与干预:采用CRISPR/Cas9技术构建的Atp4a-/-小鼠作为自发GIM模型,12周龄开始给予1000 mg/kg/d牛磺酸饮水干预4周,设立野生型对照组和模型对照组。
2. 病理学评估:取胃组织进行石蜡包埋切片,分别行HE染色和Alcian blue-Periodic acid Schiff(AB-PAS)染色,评估黏膜形态结构、腺体增生及酸/中性黏蛋白分布变化。
3. 分子标志物检测:采用qPCR检测肠道标志物CDX2、MUC2、TFF3及胃标志物MUC5AC的mRNA表达;免疫组化检测上述蛋白表达并采用德国半定量评分系统进行量化分析。
4. 人源类器官培养:取3例GIM患者病变组织及配对正常胃黏膜,经胶原酶XI消化后包埋于Matrigel,使用含R-spondin、Noggin、EGF等因子的培养基建立人胃类器官。
5. 类器官药物干预:将正常及GIM类器官分别给予200 mmol/L牛磺酸或基础培养基处理1周,qPCR检测标志物基因表达,Western blot验证CDX2和TFF3蛋白水平变化。
Figure 1展示了Atp4a-/-小鼠GIM模型的建立及牛磺酸干预效果。HE染色显示野生型小鼠胃黏膜结构规则,而Atp4a-/-小鼠出现黏膜粗糙、腺体扩张及空泡变性;牛磺酸治疗后黏膜表面趋于光滑,腺体结构恢复规则。AB-PAS染色证实野生型以中性黏蛋白(紫红色)为主,模型组出现大量酸性黏蛋白(蓝紫色),干预组酸性黏蛋白明显减少。qPCR结果显示模型组肠道标志物Cdx2、Muc2、Tff3显著上调,牛磺酸显著抑制其表达;胃标志物Muc5ac在模型组下调,经牛磺酸处理后显著回升。
Figure 2呈现了免疫组化验证的蛋白水平变化。CDX2在野生型胃黏膜几乎不表达,模型组广泛阳性,干预组阳性细胞显著减少且局限于局灶腺体。MUC2和TFF3呈现相似表达模式,模型组强阳性,牛磺酸干预后显著降低。MUC5AC在模型组阳性面积减小且染色减弱,干预后染色强度恢复。半定量评分统计分析证实上述改变具有显著性差异,表明牛磺酸在转录和翻译水平均可缓解GIM病理特征。
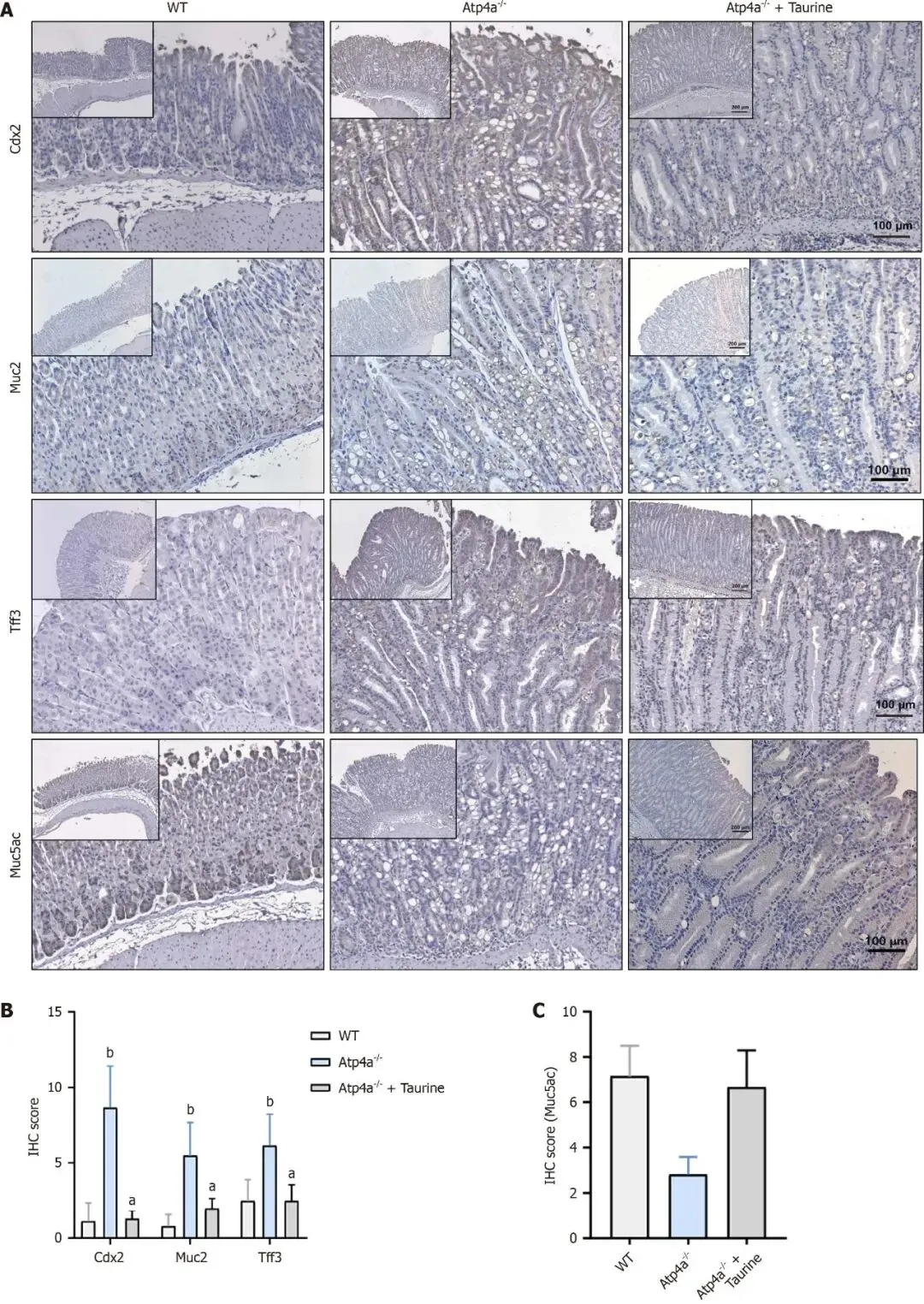
Figure 3展示了人源GIM类器官模型的建立及牛磺酸干预效应。A图显示正常胃类器官7天培养的典型生长过程。B-M图为3例独立患者样本的qPCR结果,显示与配对正常类器官相比,GIM类器官中CDX2、MUC2、TFF3显著高表达而MUC5AC显著低表达,证实模型成功再现GIM分子特征。经牛磺酸干预后,GIM类器官中三种肠道标志物表达显著降低,患者1和3的MUC5AC显著上调,患者2呈上调趋势,而正常类器官标志物表达无显著变化,提示牛磺酸对GIM具有选择性调控作用。
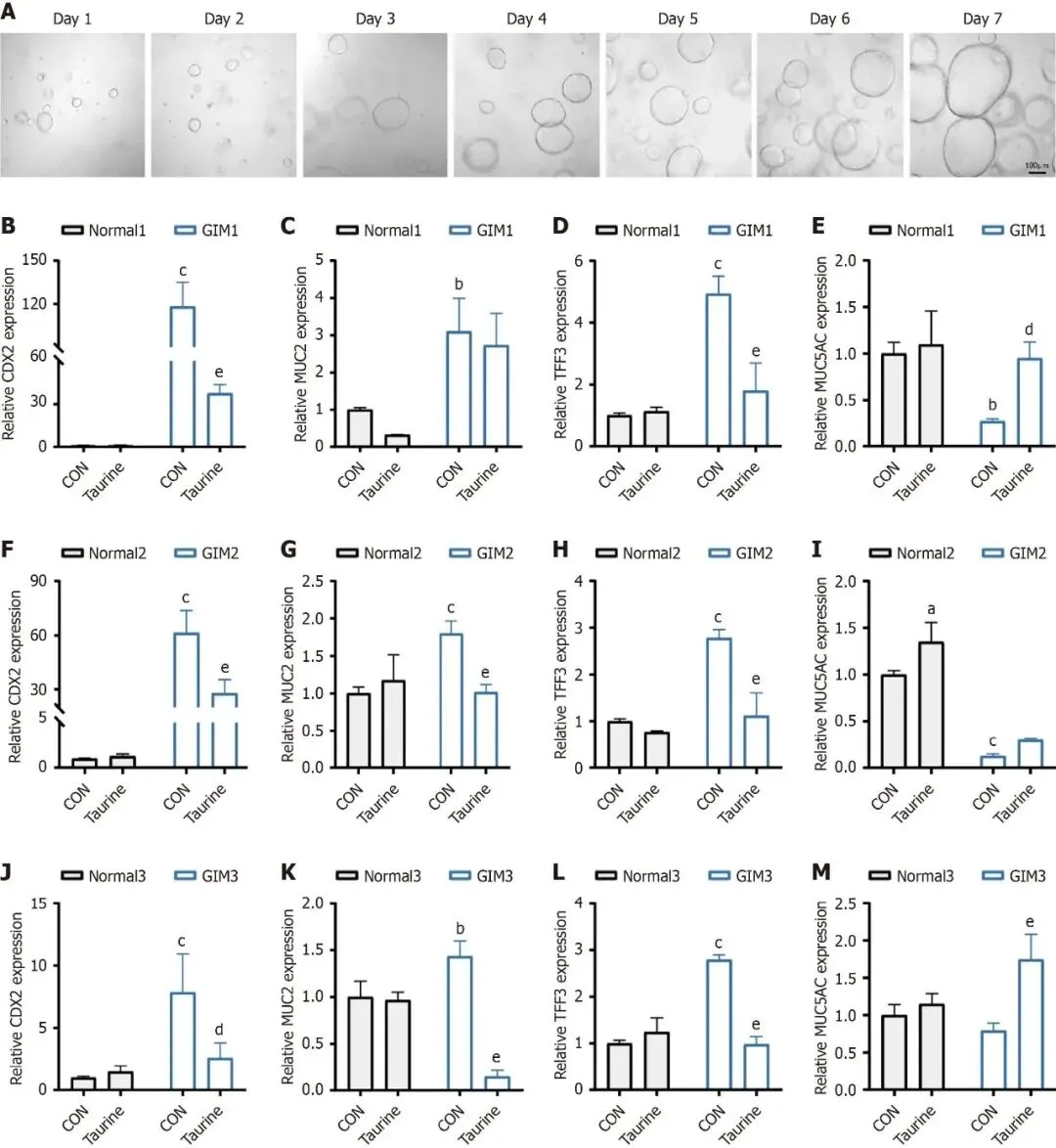
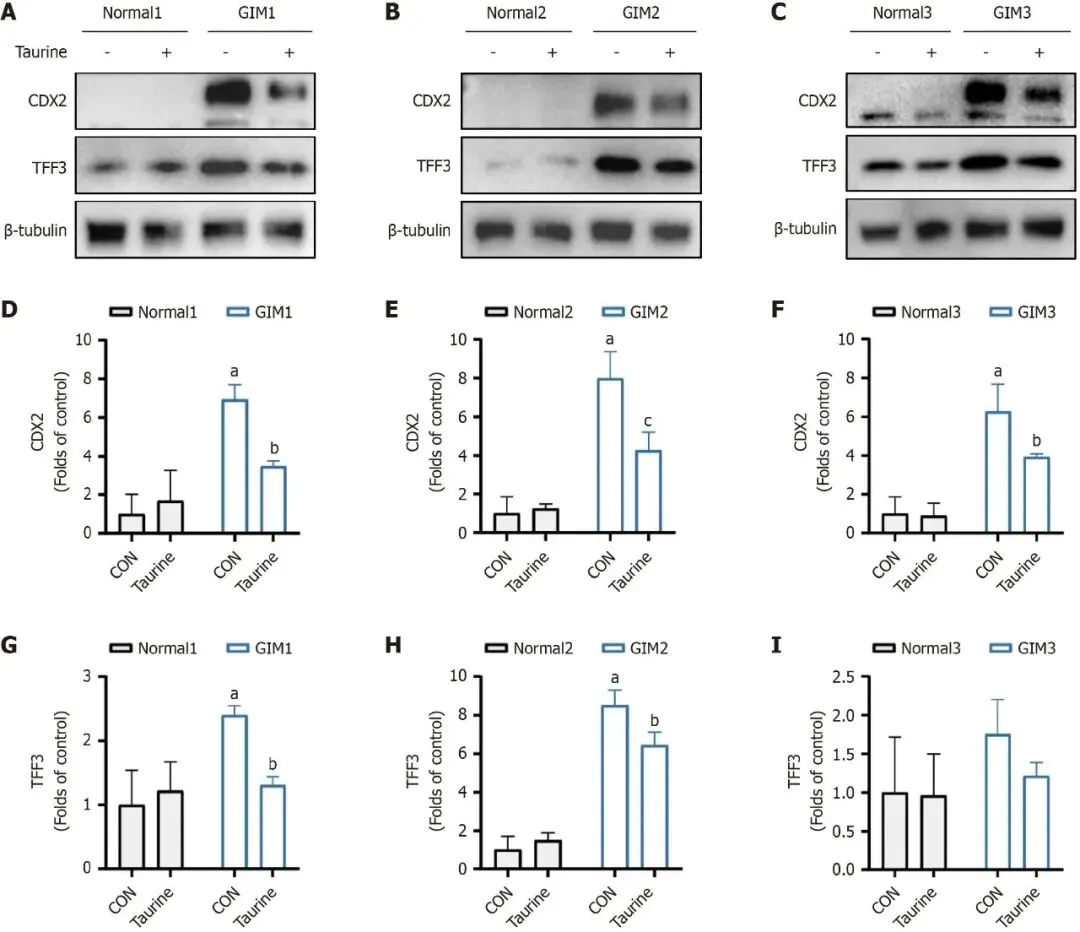
Figure 4通过Western blot在蛋白水平验证类器官干预结果。A-C图显示3例患者GIM类器官中CDX2和TFF3蛋白条带,D-I图为定量统计结果。与正常对照相比,GIM类器官CDX2和TFF3蛋白水平显著升高;牛磺酸干预后两种蛋白表达均显著下调,与mRNA结果一致,进一步证实牛磺酸在人源体系中可抑制GIM相关标志物表达,支持其临床转化潜力。
原文链接
https://pubmed.ncbi.nlm.nih.gov/41695925/
版权声明
标注‘原创’仅代表原创编译,本平台不主张对原文的版权。本平台转载仅出于学术交流和传播信息的需要,不代表本平台观点或证实其内容的真实性。原文版权归原作者所有,作者如不希望被转载或有侵权行为,请联系本平台删除。