郑州大学王蕾团队ACS Nano| 益生菌芽孢"特洛伊木马":肠-脑双重调控策略突破帕金森病口服治疗瓶颈
- 2026-05-25 05:25:35


文献溯源

原名: Probiotic Spore-Based Oral Biotherapeutics Promote Brain Targeting toward Gut-Brain Dual-Regulation for Parkinson's Disease Treatment
01
研究内容
帕金森病(PD)是一种以神经炎症和多巴胺能神经元退化为特征的神经退行性疾病。传统PD治疗主要靶向脑部,但忽视了肠道来源的影响。近年来,随着微生物组-肠-脑轴的阐明,肠道作为"第二大脑"受到广泛关注——肠道菌群失调在PD发病机制中扮演重要角色。然而,口服给药面临多重屏障挑战(生化屏障、肠道黏液屏障、肠上皮屏障、血-中枢神经系统屏障),实现口服脑靶向药物递送极具挑战性。益生菌芽孢不仅能介导肠-脑通讯,还具有口服脑靶向药物递送的潜力,这为肠-脑双重调控提供了重要价值。
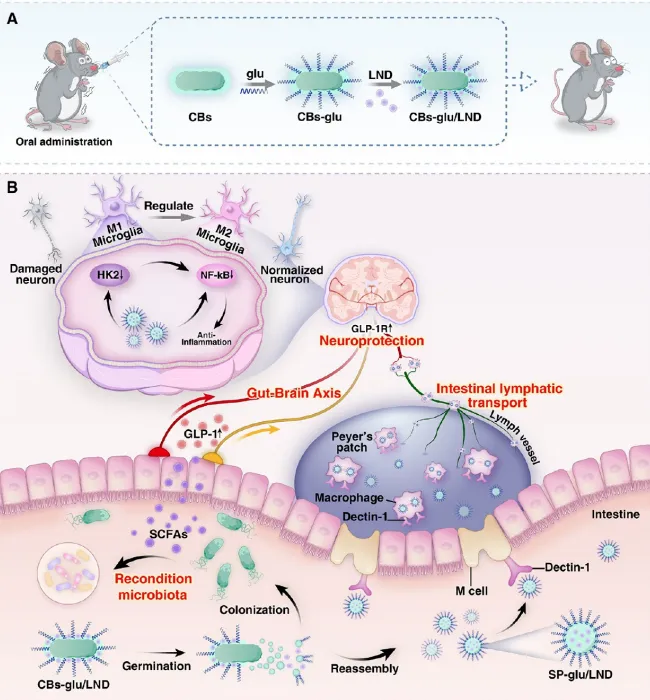
本研究设计了一种基于丁酸梭菌芽孢(CBs)的口服抗PD生物治疗药物CBs-glu/LND。该体系通过酯化反应将β-葡聚糖(glu)修饰于芽孢表面,并负载HK2抑制剂洛尼达明(LND)。口服后,芽孢系统穿越胃肠道化学屏障,在肠道萌发为丁酸梭菌,同时芽孢外壳蛋白(SP)从表面脱落并重新组装成载药纳米系统(SP-glu/LND)。β-葡聚糖修饰的纳米颗粒通过识别M细胞和巨噬细胞表面高表达的Dectin-1受体,经派尔集合淋巴结进入肠道淋巴系统,搭乘巨噬细胞这一"特洛伊木马"穿越血-脑屏障到达脑部。在脑部,SP-glu/LND抑制HK2-NF-κB通路,将小胶质细胞从促炎M1型重编程为抗炎M2型;在肠道,丁酸梭菌定植并分泌短链脂肪酸(SCFAs),通过肠-脑轴间接调节脑功能。
02
研究亮点及创新点
1.仿生"特洛伊木马"策略实现口服脑靶向递送:本文创新性地利用益生菌芽孢作为"自主纳米发生器",在肠道原位生成载药纳米颗粒,并通过β-葡聚糖介导的M细胞和巨噬细胞双靶向,实现"细胞搭车"式脑靶向递送。这一策略巧妙规避了传统纳米药物制备复杂、稳定性差的问题,利用机体固有免疫细胞的炎症趋化特性,使药物精准富集于PD炎症病灶。如图4所示,巨噬细胞搭载的SP-glu纳米系统成功穿越血-脑屏障,在脑内与F4/80阳性巨噬细胞共定位,而与TMEM119阳性小胶质细胞无关联,证实了外周巨噬细胞介导的递送机制。

科研思维积累
2."障碍-策略-验证"的问题导向思维:针对口服脑靶向的四大屏障(生化、黏液、肠上皮、血-脑屏障),研究设计了针对性的解决策略并逐一验证。生化屏障→芽孢外壳天然抗性;黏液屏障→M细胞缺乏黏液层的特性;肠上皮屏障→Dectin-1介导的跨细胞转运;血-脑屏障→炎症趋化的巨噬细胞搭车策略。图4H清晰展示了这一"过关斩将"的递送路径,并通过体内外实验(M细胞模型、流式细胞术、活体成像、免疫荧光共定位)逐级验证每个环节的有效性。这种将复杂问题拆解为可验证单元的方法论,确保了递送机制的可控性和可靠性。
3."交叉-融合-创新"的学科交叉思维:研究有机融合了微生物学(益生菌芽孢生物学)、纳米医学(自组装纳米系统)、免疫学(Dectin-1受体识别、巨噬细胞极化)、神经科学(PD病理机制、小胶质细胞代谢重编程)和药理学(淋巴靶向递送、HK2抑制剂)等多学科知识。特别值得注意的是,将肿瘤免疫治疗中成熟的"巨噬细胞搭车"策略(参考文献16、31-32)迁移应用于神经退行性疾病治疗,体现了跨领域知识迁移的创新思维。同时,对肠-脑轴这一新兴领域的深度整合,使研究从单纯的药物递送技术提升为系统性的疾病调控策略。

END

往期回顾

点击 阅读原文,关注我们!
