郑州大学董子钢/王梅云/郭智萍团队PNAS发文:揭示WNK1磷酸化PHGDH驱动丝氨酸代谢,破解胃癌奥沙利铂耐药,并提供全新疗效预测标志物
本文适合肿瘤学、代谢生物学领域的硕博研究生、一线科研工作者,从事胃癌临床诊疗与临床转化研究的医师,深耕肿瘤精准诊疗、多组学技术研发的从业者,以及关注肿瘤化疗耐药、代谢靶向治疗的医药研发人员与科研爱好者阅读。全文七千多字,在移动端需要连续滑动多次才能读完,读者请谨慎阅读。一、研究亮点(核心创新与前沿突破)
本研究聚焦胃癌代谢重编程与化疗耐药两大临床难题,实现了基础科研与临床转化的双重突破,核心创新点如下:
1. 发现全新分子调控轴:首次阐明WNK1-PHGDH丝氨酸代谢调控轴,填补了胃癌丝氨酸代谢翻译后修饰调控的研究空白,打破了既往PHGDH转录水平调控的单一认知。
2. 定位关键功能磷酸化位点:精准鉴定PHGDH蛋白Ser349、Ser371双磷酸化位点,明确该修饰是调控PHGDH酶活性与蛋白稳定性的核心开关。
3. 揭示代谢耐药全新机制:解析“PHGDH磷酸化→丝氨酸合成亢进→GSH抗氧化通路激活→氧化应激死亡受阻→奥沙利铂耐药”的完整分子通路,厘清代谢重编程与化疗敏感性的内在关联。
4. 提出双重临床标志物:证实PHGDH磷酸化水平、肿瘤丝氨酸含量可同时作为胃癌代谢脆弱性标志物与奥沙利铂疗效预测标志物,为临床个体化用药提供依据。
5. 开拓治疗新策略:验证靶向抑制PHGDH可逆转胃癌奥沙利铂耐药,为代谢靶向联合化疗的临床方案提供了坚实的实验依据。
二、研究背景(前沿进展与研究缺口)
代谢重编程是肿瘤发生发展的核心标志性特征,肿瘤细胞通过重塑代谢通路满足自身快速增殖、抵御应激微环境的需求,其中氨基酸代谢紊乱更是介导肿瘤进展、治疗耐药的关键环节。丝氨酸作为非必需氨基酸,不仅是蛋白质合成的原料,更是谷胱甘肽(GSH)合成的前体物质,参与细胞氧化还原平衡调控,直接影响肿瘤细胞的氧化应激耐受与存活。
磷酸甘油酸脱氢酶(PHGDH)是丝氨酸从头合成通路的限速酶,在乳腺癌、结直肠癌等多种肿瘤中异常高表达,且与患者不良预后密切相关。但当前领域内存在诸多关键科学缺口:其一,胃癌中丝氨酸代谢异常的核心驱动机制尚不明确,PHGDH在胃癌中的功能定位未被阐明;其二,既往研究多聚焦PHGDH转录水平调控,其翻译后修饰对酶活性、蛋白稳定性的调控机制完全未知;其三,胃癌临床治疗中,奥沙利铂是新辅助化疗核心药物,化疗耐药是制约疗效的核心难题,但丝氨酸代谢与奥沙利铂敏感性的关联尚未被揭示;其四,临床缺乏可精准预测胃癌奥沙利铂疗效的无创/微创代谢标志物,个体化治疗难以推进。
WNK1激酶作为丝氨酸/苏氨酸激酶,既往研究仅聚焦其渗透压调控、应激应答功能,其在肿瘤代谢重编程中的调控作用从未被挖掘。基于以上研究空白,本研究围绕丝氨酸代谢核心酶PHGDH,深入挖掘其上游调控机制,最终搭建起“激酶-代谢酶-代谢表型-化疗耐药”的完整科研体系。
三、科研问题聚焦(核心科学与临床问题)
本研究紧扣临床需求、锚定领域空白,聚焦五大核心问题展开全方面探究,所有实验设计均围绕以下问题逐一突破:
1. 临床胃癌组织中丝氨酸代谢是否存在异常?PHGDH是否是驱动胃癌丝氨酸代谢重编程的核心因子?
2. 胃癌中PHGDH蛋白的翻译后修饰特征是什么?上游调控激酶是哪一分子?二者存在怎样的相互作用?
3. WNK1调控PHGDH的具体分子机制(磷酸化位点、酶活性、蛋白稳定性)是什么?
4. WNK1-PHGDH调控轴如何通过重塑丝氨酸代谢,影响胃癌细胞氧化还原平衡与化疗敏感性?
5. PHGDH及其磷酸化修饰能否作为临床胃癌患者奥沙利铂疗效预测、代谢脆弱性评估的双重标志物?
四、实验策略设计
本研究遵循“临床表型挖掘→核心分子筛选→分子机制深挖→功能验证→临床转化”的逻辑,全程层层递进、排除干扰变量,实现从临床样本到基础机制再回归临床的完整闭环,每一步实验均围绕既定目标设计,兼顾严谨性与转化价值。
1. 研究目标(What)
明确胃癌丝氨酸代谢重编程的核心调控机制,挖掘WNK1-PHGDH轴在胃癌进展中的功能,阐明其介导奥沙利铂耐药的分子通路,筛选可用于临床疗效预测的代谢标志物,提出靶向代谢联合化疗的全新治疗策略。
2. 核心发现(What)
胃癌中WNK1通过磷酸化PHGDH Ser349/Ser371位点,增强PHGDH酶活性并抑制其泛素化降解,进而驱动丝氨酸合成亢进、提升细胞抗氧化能力,最终介导胃癌奥沙利铂化疗耐药;PHGDH磷酸化水平可作为双重代谢标志物,指导临床化疗方案选择。
3. 分步验证路径(How & Why)
1. 第一步:临床样本组学初筛,锁定核心代谢轴:通过非靶向代谢组学、生物信息学分析,筛选胃癌差异代谢通路与核心酶。为何这样做:从临床真实表型出发,避免体外细胞研究的片面性,精准锁定疾病核心异常通路,减少研究盲目性。
2. 第二步:体外体内功能验证,明确核心分子功能:通过基因敲低/过表达、同位素示踪、PDX模型,验证PHGDH对胃癌增殖、丝氨酸合成的调控作用。为何这样做:夯实核心分子的功能表型,为后续机制研究奠定基础。
3. 第三步:上游调控分子筛选,定位关键激酶:通过质谱、免疫共沉淀筛选PHGDH互作激酶,聚焦WNK1并验证二者相互作用。为何这样做:翻译后修饰是代谢酶快速调控的核心方式,激酶筛查是解析上游调控的最优路径。
4. 第四步:位点精准鉴定,解析酶活调控机制:通过生物信息学预测、位点突变、体外激酶实验,定位双磷酸化位点。为何这样做:明确功能位点才能精准解析分子机制,为后续靶向干预提供精准靶点。
5. 第五步:蛋白稳定性调控,完善机制链条:通过泛素化、蛋白酶体抑制实验,解析PHGDH降解通路。为何这样做:完善转录后调控全链条,让分子机制更完整、更具说服力。
6. 第六步:临床转化验证,落地科研价值:结合临床队列数据,验证标志物与化疗疗效的相关性。为何这样做:实现基础研究向临床应用的转化,贴合临床科研的核心需求。
五、关键分子机制探究
第一阶段:锁定PHGDH为胃癌丝氨酸代谢核心驱动因子
研究目标:明确胃癌中丝氨酸代谢异常的核心调控酶,排除其他代谢通路干扰。
核心发现:胃癌组织与细胞中PHGDH表达、酶活性显著升高,直接驱动丝氨酸从头合成亢进,是丝氨酸代谢重编程的核心诱因。
验证方式:临床样本代谢组学、TCGA数据库分析、13C葡萄糖同位素示踪、PHGDH敲低功能实验。
设计逻辑:先锁定核心靶标,再开展机制研究,避免后续实验偏离核心方向。
第二阶段:筛选并验证WNK1为PHGDH上游调控激酶
研究目标:找到介导PHGDH磷酸化的上游激酶,解析二者相互作用模式。
核心发现:WNK1与PHGDH在细胞质内共定位,且通过PHGDH的ASB结构域发生特异性直接结合。
验证方式:质谱互作蛋白筛选、Co-IP免疫共沉淀、免疫荧光共定位、结构域截短突变实验。
设计逻辑:优先筛查丝氨酸/苏氨酸激酶,贴合磷酸化修饰的调控规律,快速锁定核心上游分子。
第三阶段:鉴定PHGDH功能性磷酸化位点
研究目标:明确WNK1调控PHGDH的关键磷酸化位点,解析位点对酶活性的影响。
核心发现:WNK1特异性磷酸化PHGDH Ser349、Ser371双位点,双位点协同调控PHGDH催化活性。
验证方式:生物信息学位点预测、定点突变、体外激酶实验、磷酸化特异性抗体检测。
设计逻辑:单点突变+双位点突变联合验证,排除单一位点的非特异性调控,精准锁定功能位点。
第四阶段:揭示PHGDH蛋白稳定性调控机制
研究目标:阐明WNK1调控PHGDH蛋白表达的分子通路,完善转录后调控机制。
核心发现:WNK1介导的磷酸化,可拮抗E3泛素连接酶UHRF2介导的泛素化蛋白酶体降解,进而稳定PHGDH蛋白。
验证方式:环乙酰亚胺(CHX)蛋白半衰期实验、泛素化检测、蛋白酶体抑制剂干预、E3泛素酶筛选。
设计逻辑:区分转录调控与转录后调控,明确蛋白降解通路,完善分子调控闭环。
第五阶段:关联代谢重编程与化疗耐药表型
研究目标:明确WNK1-PHGDH轴对胃癌奥沙利铂敏感性的调控作用。
核心发现:PHGDH高活性通过提升GSH含量、清除活性氧,削弱奥沙利铂诱导的肿瘤细胞氧化应激死亡,进而介导化疗耐药。
验证方式:细胞药敏实验、PDX动物模型、临床队列相关性分析。
设计逻辑:从基础机制回归临床表型,实现基础科研与临床问题的深度绑定。
六、数据解读
本研究通过临床样本、细胞、动物模型多维度验证,证实WNK1-PHGDH轴是胃癌丝氨酸代谢重编程的核心驱动力,其异常激活通过重塑细胞氧化还原平衡,介导奥沙利铂化疗耐药,PHGDH磷酸化是极具临床价值的双重代谢标志物。
Figure 1 :确立丝氨酸代谢与PHGDH在胃癌中的核心驱动作用
核心问题:丝氨酸代谢在胃癌中是否发生重编程?其关键酶PHGDH是否驱动肿瘤进展?
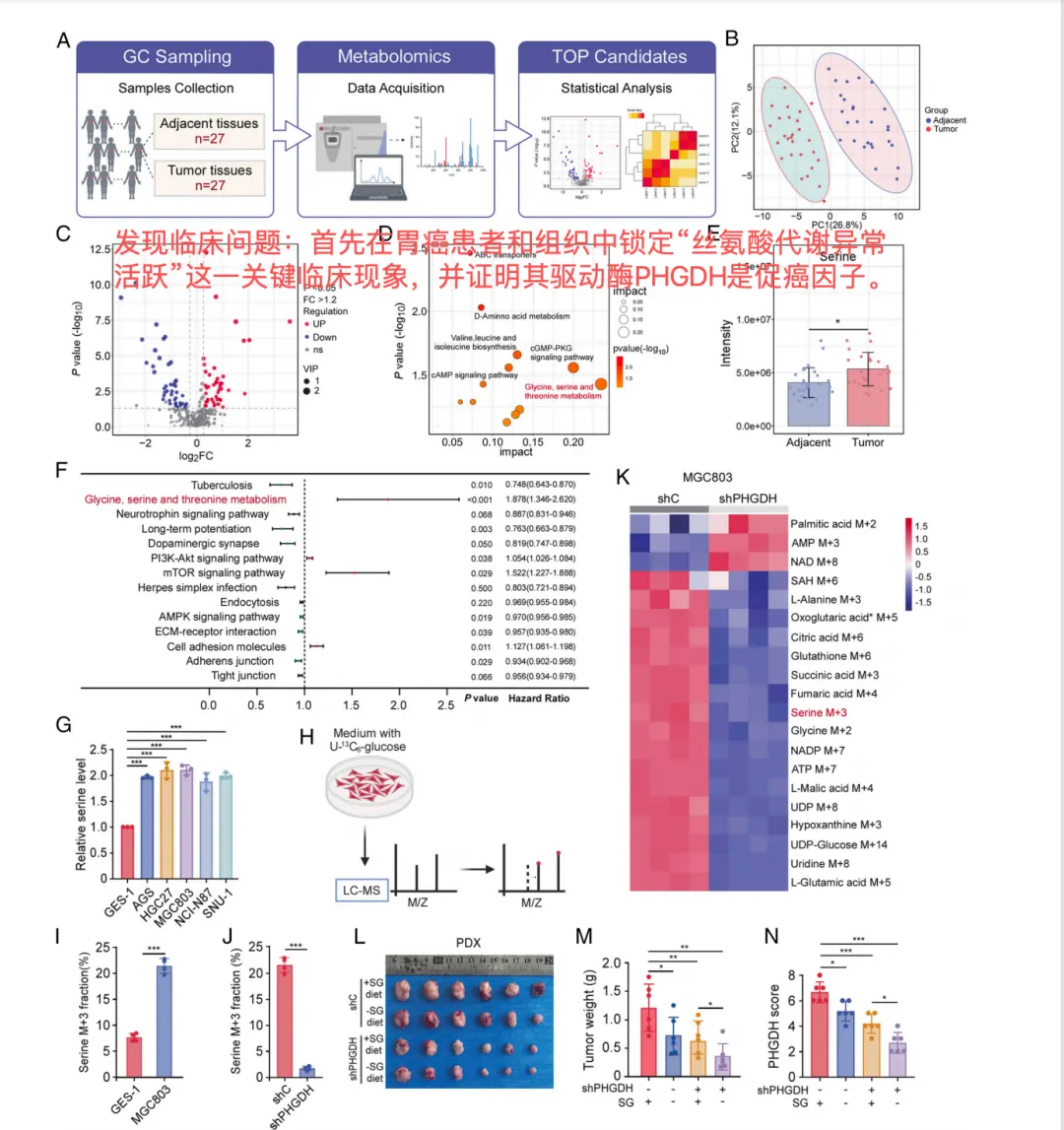
数据与发现:
1A-1E (临床样本代谢组学):通过对27对胃癌与癌旁组织的非靶向代谢组学分析,发现肿瘤与正常组织代谢谱明显分离。其中,丝氨酸等代谢物在肿瘤中显著上调,KEGG通路富集分析提示“甘氨酸、丝氨酸和苏氨酸代谢”通路异常活跃。
1F (生物信息学分析):TCGA数据分析显示,丝氨酸代谢相关基因集与胃癌患者不良预后显著相关。
1G-1I (细胞水平验证):在胃癌细胞系中直接检测到丝氨酸水平升高,并使用U-[13C]-葡萄糖示踪实验证明,胃癌细胞(MGC803)的丝氨酸从头合成通量(M+3标记)比正常胃上皮细胞(GES-1)高出约3倍,确证了其合成能力的增强。
1J-1K (功能验证):敲低PHGDH可显著降低胃癌细胞中13C标记的丝氨酸生成,证明PHGDH是驱动丝氨酸合成的关键酶。
1L-1N (体内功能):在患者来源异种移植(PDX)模型中,敲低PHGDH能显著抑制肿瘤生长。若同时配合无丝氨酸/甘氨酸饮食,抑瘤效果更为明显。
结合了临床样本分析(代谢组学)、公共数据库挖掘(TCGA)、稳定同位素示踪(13C-葡萄糖)和体内外功能缺失实验(敲低PHGDH) 多种技术。
回答了“丝氨酸代谢在胃癌中是否重要?”。答案是肯定的。该组图系统性地证明了胃癌中存在丝氨酸代谢的异常活化,其限速酶PHGDH通过促进丝氨酸合成,直接驱动肿瘤的生长,是胃癌的一个关键代谢弱点。
Figure 2 解读:阐明WNK1激酶磷酸化激活PHGDH的分子机制、、
核心问题:PHGDH的活性受何种上游信号调控?具体分子机制是什么?
数据与发现:
2A-2F (激酶鉴定与验证):通过磷酸化蛋白质组学筛选出与PHGDH互作的候选激酶,并锁定WNK1。实验证明:①重组WNK1可在体外磷酸化PHGDH;②在细胞中过表达WNK1可增强PHGDH磷酸化,敲低则降低;③WNK1的激酶活性是其发挥功能所必需的。
2G-2K (磷酸化位点鉴定与功能):通过生物信息学预测和点突变,鉴定出Ser349和Ser371是WNK1磷酸化PHGDH的关键位点。制备了位点特异性磷酸化抗体(pS349, pS371)进行验证。酶动力学分析显示,模拟磷酸化(S2D)部分恢复酶活,而磷酸化缺陷(S2A)突变体则严重损害了PHGDH的催化活性和底物亲和力。
2L-2N (功能互补):在WNK1缺失的背景下,磷酸化缺陷突变体(S2A)的酶活显著低于野生型,而磷酸化模拟突变体(S2D)能部分回补酶活。
采用了蛋白质组学筛选、免疫共沉淀、体外激酶实验、点突变、酶动力学分析和磷酸化特异性抗体等分子与生化手段。
回答了“PHGDH如何被激活?”。研究揭示了一条全新的调控轴:上游激酶WNK1通过直接磷酸化PHGDH蛋白的S349和S371位点,从而增强其酶学活性,将激酶信号与代谢酶功能直接偶联。
Figure 3 :建立PHGDH-丝氨酸代谢轴与奥沙利铂耐药的临床关联
核心问题:PHGDH介导的丝氨酸代谢亢进是否导致化疗耐药?其临床意义如何?
数据与发现:
3A-3D (患者队列验证):对14名接受奥沙利铂新辅助化疗的胃癌患者肿瘤组织分析发现,与治疗响应者相比,无响应者的肿瘤组织具有更高的PHGDH酶活、丝氨酸和谷胱甘肽(GSH)水平,以及更低的脂质活性氧(ROS)。这提示高活性的丝氨酸代谢与抗氧化能力增强和化疗耐药相关。
3E-3F (生物信息学支持):公共数据集(GSE128967)分析表明,在奥沙利铂响应者中,丝氨酸代谢通路显著富集。
3G-3N (功能与临床前治疗):在60名患者的队列中,无响应者肿瘤的PHGDH表达更高。体外实验显示,抑制PHGDH可增敏奥沙利铂的疗效,而过表达PHGDH则诱导耐药。机制上,PHGDH缺失会加剧奥沙利铂引起的DNA损伤(γ-H2AX↑)。在PDX模型中,PHGDH抑制剂与奥沙利铂联用展现出显著的协同抑瘤效果。
3O-3P (类器官模型验证):在患者来源胃癌类器官(PDO)中,PHGDH抑制剂NCT-503与奥沙利铂联用能显著增强治疗效果。
整合了临床样本生化检测、公共转录组数据分析、体外药物敏感性实验、体内PDX模型治疗实验以及更接近临床的PDO模型验证。
回答了“这一代谢机制有临床意义吗?”。研究证实,PHGDH/丝氨酸代谢轴的激活是导致胃癌对奥沙利铂化疗耐药的重要机制,靶向PHGDH具有增敏化疗的临床转化潜力。
Figure 4 :确立PHGDH磷酸化作为预测化疗响应的关键生物标志物、
核心问题:PHGDH的磷酸化状态是否是其功能核心?能否作为预测化疗疗效的生物标志物?
数据与发现:
4A-4E (磷酸化是关键功能事件):实验证明,磷酸化缺陷的PHGDH-S2A突变体(而非野生型)会导致DNA损伤增加(γ-H2AX↑),并使细胞对奥沙利铂更敏感。碱性彗星实验也证实,失去磷酸化会加剧奥沙利铂引起的DNA损伤。
4F-4I (临床生物标志物验证):在60名患者的训练队列中,无响应者肿瘤的WNK1、PHGDH及磷酸化PHGDH(pPHGDH-S349/S371)水平均显著高于响应者。通过免疫组化(IHC)和CT影像展示了pPHGDH高表达与治疗反应差的相关性。受试者工作特征(ROC)曲线分析显示,pPHGDH、PHGDH和WNK1三者联合的预测效能最佳(AUC=0.80),并在一个32人的独立验证队列中得到了验证(pPHGDH的AUC=0.76)。
4H-4I (预测效能分析):多因素分析表明,pPHGDH是独立于年龄、分期等常规临床病理因素的预测指标。
通过构建功能特异性突变体、对比其介导的化疗敏感性差异,并在两个独立的临床队列中进行严格的生物标志物关联分析与验证。
回答了“哪个分子事件最具预测和机制价值?”。研究明确指出,PHGDH的磷酸化修饰(pPHGDH-S349/S371)是其激活和导致耐药的功能核心事件,并且其蛋白水平可以作为预测胃癌患者对奥沙利铂化疗响应的可靠生物标志物。
七、研究结论
1. 丝氨酸代谢重编程是胃癌的核心代谢特征,PHGDH作为限速酶高表达、高活性,是驱动胃癌进展的关键代谢分子;2. WNK1通过磷酸化PHGDH Ser349、Ser371双位点,同步提升PHGDH酶活性与蛋白稳定性,进而驱动丝氨酸合成亢进;3. WNK1-PHGDH轴通过增强细胞抗氧化能力、维持氧化还原平衡,抑制奥沙利铂诱导的肿瘤细胞氧化死亡,最终介导化疗耐药;4. PHGDH磷酸化水平、肿瘤丝氨酸含量可作为胃癌代谢脆弱性评估与奥沙利铂疗效预测的双重标志物,靶向抑制PHGDH可有效逆转胃癌化疗耐药。
八、实验材料、核心数据与技术方法
1. 核心实验材料
临床样本:27例胃癌患者癌组织与配对癌旁正常组织;TCGA、GSE27342胃癌数据库数据集;
细胞系:人正常胃黏膜上皮细胞GES-1、胃癌细胞系AGS、HGC27、MGC803、NCI-N87、SNU-1、293T细胞;
动物模型:PDX人源肿瘤异种移植模型、WNK1基因敲除小鼠;
核心试剂:PHGDH、WNK1、磷酸化特异性抗体;泛素化、蛋白酶体抑制剂;13C葡萄糖同位素;shRNA慢病毒载体;位点突变质粒等。
2. 核心实验数据
胃癌组织丝氨酸含量显著升高(P=0.017);PHGDH在胃癌组织与细胞中表达、酶活性显著上调;WNK1敲低后PHGDH磷酸化水平、酶活性、丝氨酸含量显著下降;PHGDH双位点突变后,蛋白降解速率加快、泛素化水平升高;PHGDH高表达的胃癌患者对奥沙利铂化疗应答率显著降低。
3. 核心实验技术方法
组学技术:非靶向代谢组学、13C葡萄糖同位素代谢流分析、LC-MS/MS质谱蛋白组学;
分子生物学技术:Western Blot、qPCR、免疫共沉淀(Co-IP)、免疫荧光共定位、基因敲低/过表达、定点突变、体外激酶实验;
蛋白功能研究:泛素化检测、蛋白半衰期检测、酶动力学分析;
生物信息学:PLS-DA、KEGG富集分析、GSEA分析、位点预测、生存分析;
体内外功能实验:细胞增殖/克隆形成实验、PDX动物模型、IHC免疫组化。
一、研究的核心价值
这项研究的核心价值在于它系统性地构建并验证了一个全新的生物学轴心:WNK1激酶 → 磷酸化激活PHGDH → 增强丝氨酸合成 → 帮助癌细胞抵抗铁死亡和化疗。这远不止是发现了一个新调控因子,而是清晰地描绘了“激酶信号如何通过修饰代谢酶,进而重塑细胞命运”的完整路线图。
具体体现在三个层面:
机制深度:它揭示了磷酸化对PHGDH的双重调控——既“开大油门”(增强酶活性),又“踩住刹车”(防止蛋白被降解),这种精细调控确保了代谢的持续亢进。
临床紧密度:研究自始至终围绕“奥沙利铂耐药”这一临床难题。它没有停留在解释现象,而是将机制核心(PHGDH磷酸化)转化为预测化疗反应的潜在生物标志物,并验证了“PHGDH抑制剂+化疗”的联合治疗策略,转化路径非常清晰。
逻辑严谨性:从无偏见的组学筛选,到精确的分子互作验证,再到细胞死亡机制探索,最后在患者样本和类器官模型中回溯验证,每一步都环环相扣,形成了强大的证据链。
二、团队脉络:专注于“代谢调控与耐药”的精密解剖
从这项研究可以推断,该团队的核心思路是利用多组学技术解码肿瘤代谢的调控网络,并阐明其在治疗抵抗中的具体作用。他们擅长整合代谢组学、蛋白质组学、磷酸化组学进行初步“抓取”,再用同位素示踪、基因编辑、患者来源模型等工具进行“深挖”和“验证”。本研究正是这一思路的集中体现:发现了“激酶磷酸化代谢酶”这一关键调控模式。接下来,他们可能会沿着这条线索,探索其他代谢酶是否受类似调控,或将这一轴心的上下游信号网络继续铺开。
三、领域差异:在共识中实现了关键突破
丝氨酸代谢促进肿瘤生长和耐药,这在领域内并非全新认知。但本研究实现了关键的“破局”:
共识层面:大家已知PHGDH很重要,其高表达与不良预后相关,抑制它可能增敏治疗。
本研究的突破:① 发现了全新的上游开关:首次证明WNK1激酶通过磷酸化直接“遥控”PHGDH活性,这超越了以往关注的基因扩增或转录调控。② 揭示了全新的稳定机制:发现磷酸化能保护PHGDH不被降解。③ 提出了更优的标志物:将“磷酸化的PHGDH”而非“PHGDH总量”作为标志物,更能反映其活跃状态,预测价值更高。
四、选题与设计
选择这个课题,是基于清晰的临床需求(胃癌化疗耐药)和明确的科学缺口(PHGDH如何被精确调控)。实验设计完美遵循了“表型-分子-功能-临床”的递进逻辑:
确定表型:先用代谢组学发现胃癌“丝氨酸代谢异常”。
锁定分子:用代谢流证实是“合成增强”,故聚焦限速酶PHGDH。
寻找上游:用磷酸化蛋白质组学无偏见筛选,找到了调控它的激酶WNK1,并通过生化实验精确定位修饰位点。
阐释功能:阐明丝氨酸如何通过合成谷胱甘肽来抵抗氧化应激和铁死亡,从而保护癌细胞。
临床回归:在患者组织中验证磷酸化PHGDH与耐药的相关性,并在动物和类器官模型中测试靶向治疗的可行性。
这个设计的精妙之处在于,没有绕弯路。每一步都为下一步提供了最直接的线索,用最合适的技术回答了最核心的问题,最终编织成一个无冗余的故事。
五、对未来研究的启示
这项研究如同一份高标准的“地图”,指明了几个富有前景的方向:
研究范式:它展示了如何将临床问题转化为可研究的科学问题,并最终形成具有诊断或治疗价值的方案。
技术视角:强调多组学,特别是修饰组学与代谢组学的结合,是发现新调控机制的有力武器。
靶点理念:关注代谢酶的“活性状态”(如磷酸化),而不仅仅是“数量”,这为开发更精准的药物和生物标志物提供了新思路。
治疗策略:强化了“靶向代谢增敏传统疗法”的联合策略,鼓励人们去寻找肿瘤代谢中类似的“阿喀琉斯之踵”。
总结而言, 这项工作的深远意义,在于它成功地将一个复杂的生物学过程拆解、剖析并重新整合,不仅回答了一个具体的科学问题,更提供了一套解决类似问题的系统性方法论。它的价值,在于其完整的逻辑、深刻的理解和明确的出口。
本文原创仅指公众号文章创造,文献内容与图片版权归原著所有,文献解读仅用于学术分享,如有侵权请与后台联系。
关注公众号了解更多科研资讯、文献解读和期刊选择相关内容;
科研之路,规划比努力更重要,多组学技术服务赋能科研优人一步;欢迎交流合作;微信:BioArtOmics
欢迎大家一键三连,喜欢我,你就转发我;有话说,你就评论我;都不干你就点个赞!!!