IF20.4!郑州大学于政权院长登顶《Cell》子刊!揭示睡眠缺失损伤肠道功能
- 2026-04-30 02:21:26




📚睡眠障碍与多种慢性胃肠道疾病密切相关,但大脑如何将睡眠异常信号传递至肠道、影响肠道干细胞功能的分子机制尚不明确,亟待深入解析。
🔬郑州大学生命科学学院院长于政权带领的研究团队在《Cell Stem Cell》上发表的题为“睡眠障碍引发迷走神经回路异常激活并导:致肠道干细胞功能障碍”的研究,发现睡眠障碍通过DMV‑迷走神经‑5‑HT轴异常激活,诱导肠道干细胞氧化应激与功能障碍,揭示脑‑肠调控新通路。

文献题目:睡眠障碍引发迷走神经回路异常激活并导:致肠道干细胞功能障碍
发表期刊:Cell Stem Cell
发布时间:2026年2月5日
影响因子:IF=20.4/Q1
睡眠不足已成为全球性公共健康问题,长期睡眠障碍与炎症性肠病等多种慢性胃肠道疾病风险升高密切相关。肠道干细胞是维持肠道屏障与修复的核心,睡眠紊乱可导致肠道活性氧异常积累并损伤肠道功能,但睡眠信号从大脑传递至肠道、调控肠道干细胞的具体神经环路与分子机制仍未被阐明。
本研究采用急性睡眠剥夺小鼠模型,结合脑电图监测、组织学分析、类器官培养、多组学技术、神经示踪、光纤钙记录及化学遗传操控,系统解析了睡眠剥夺通过迷走神经背核-迷走神经-肠道轴影响肠干细胞功能的神经机制。
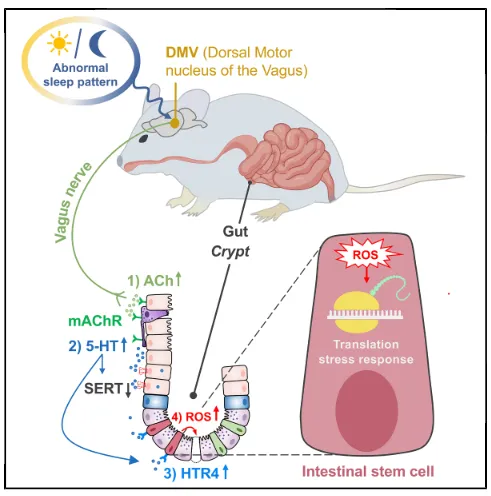
首次揭示迷走神经背核(DMV)是感知睡眠剥夺信号并传递至肠道的中枢枢纽。
发现睡眠剥夺异常激活迷走神经,释放过量乙酰胆碱,通过毒蕈碱受体引发肠道5-羟色胺(5-HT)爆发。
证实过量5-HT经HTR4受体诱导肠道干细胞氧化应激,导致干细胞功能障碍和肠道病理。


急性睡眠剥夺使小鼠REM与NREM睡眠显著减少,导致小肠绒毛隐窝缩短、上皮增殖细胞减少、凋亡增加,Lgr5⁺与Olfm4⁺肠干细胞数量下降,类器官形成与再生能力受损,且该作用不依赖肠道菌群,呈现近端小肠特异性(图1)。
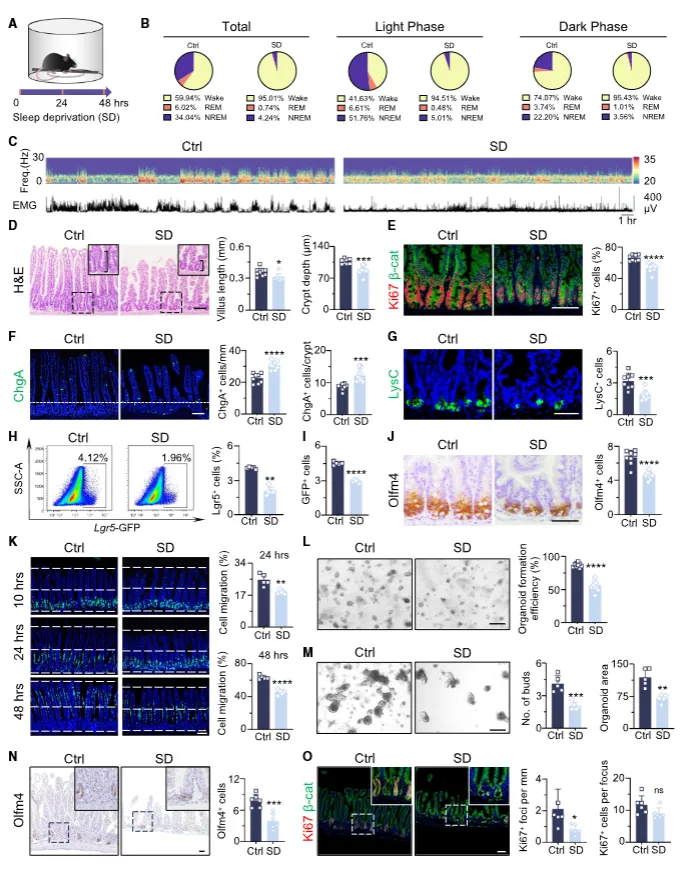
图1:短期睡眠剥夺显著损伤肠道干细胞功能并破坏肠道上皮细胞更新
睡眠剥夺诱导肠道特异性活性氧积累,激活eIF2α 磷酸化与整合应激反应,形成应激颗粒并增强自噬与泛素化蛋白降解。补充维生素C、NAC等抗氧化剂可逆转肠干细胞损伤,缓解应激通路异常激活(图2)。
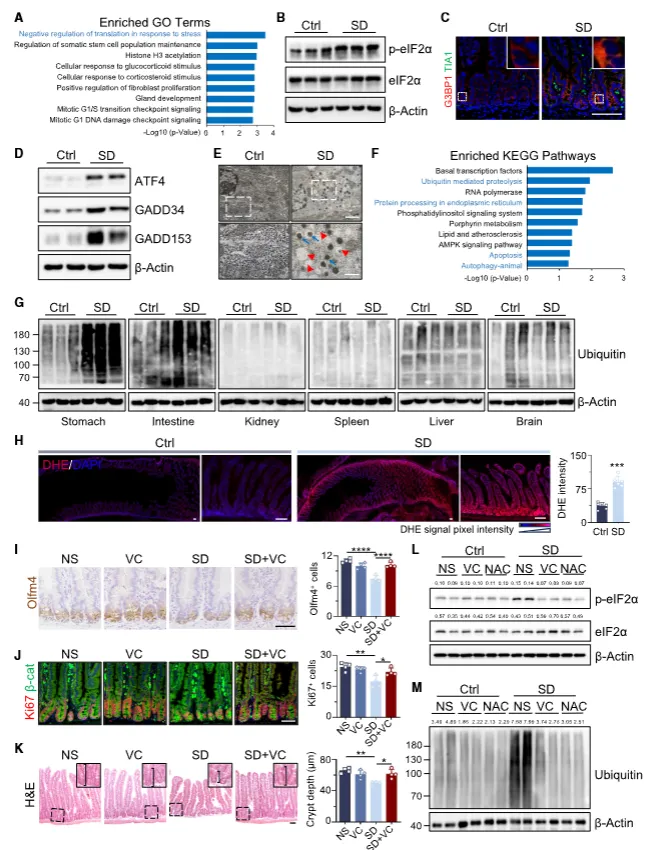
图2:短期睡眠剥夺通过激活翻译应激反应损伤肠道干细胞
睡眠干扰使肠道及血清5‑羟色胺显著升高,肠嗜铬细胞数量增加。体外5‑HT处理直接引发类器官氧化应激、抑制增殖;敲除5‑HT合成关键基因Tph1可阻断睡眠剥夺导致的肠损伤,证明5‑HT是核心介导因子(图3)。
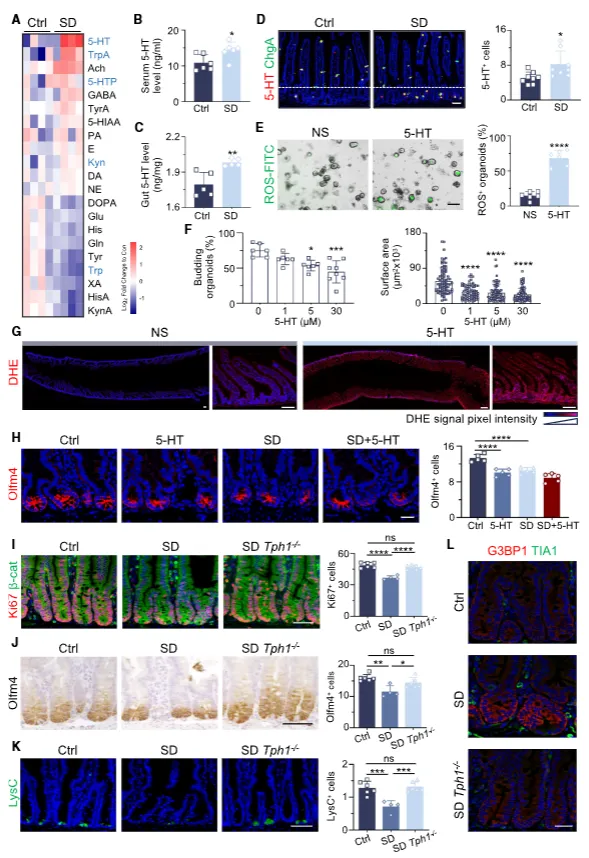
图3:急性睡眠干扰破坏5‑羟色胺稳态并诱导肠道氧化应激
单细胞测序显示HTR4是肠干细胞主要5‑HT受体,睡眠剥夺使其表达上调。HTR4激动剂可模拟5‑HT损伤效应,拮抗剂或条件性敲除HTR4则能挽救睡眠剥夺导致的肠干细胞功能下降与氧化应激(图4)。
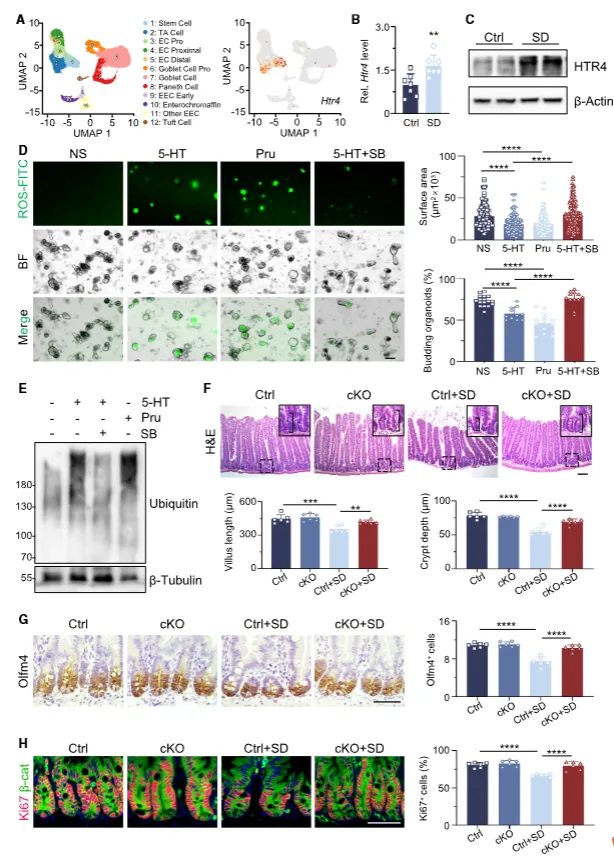
图4:肠道干细胞通过其受体HTR4响应5‑羟色胺
排除交感神经与HPA轴参与,双侧迷走神经切断术可完全阻断睡眠剥夺对肠道的损伤,恢复肠干细胞数量与隐窝结构,并阻止肠道5‑HT升高,证明迷走神经是大脑向肠道传递睡眠异常信号的关键通路(图5)。
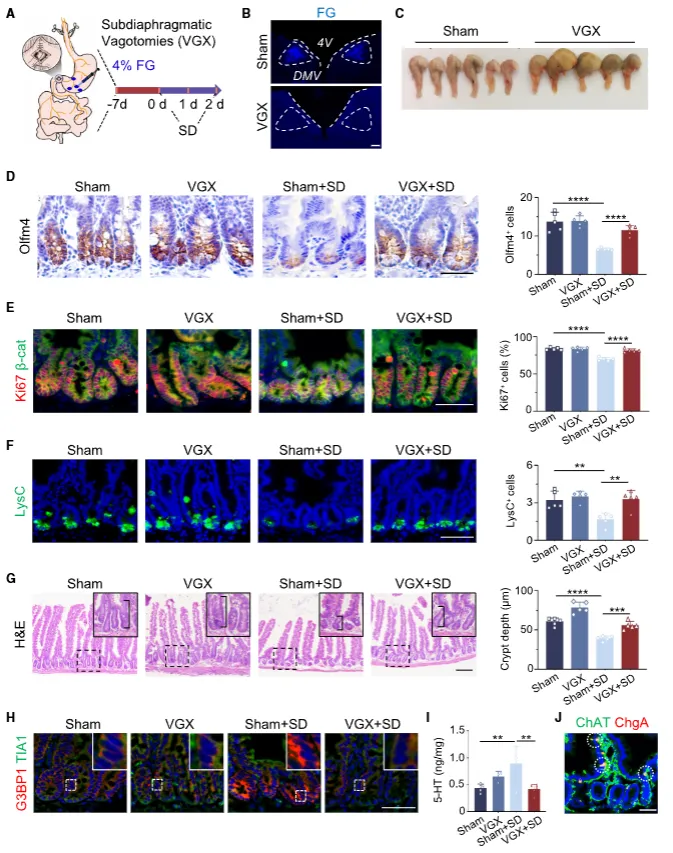
图5:迷走神经激活连接睡眠剥夺与肠道
睡眠剥夺使肠道乙酰胆碱水平上升,乙酰胆碱通过毒蕈碱受体Chrm3促进肠嗜铬细胞释放5‑HT并抑制其重吸收,造成5‑HT堆积。使用阿托品阻断毒蕈碱受体可改善睡眠剥夺引发的肠道病变(图6)。
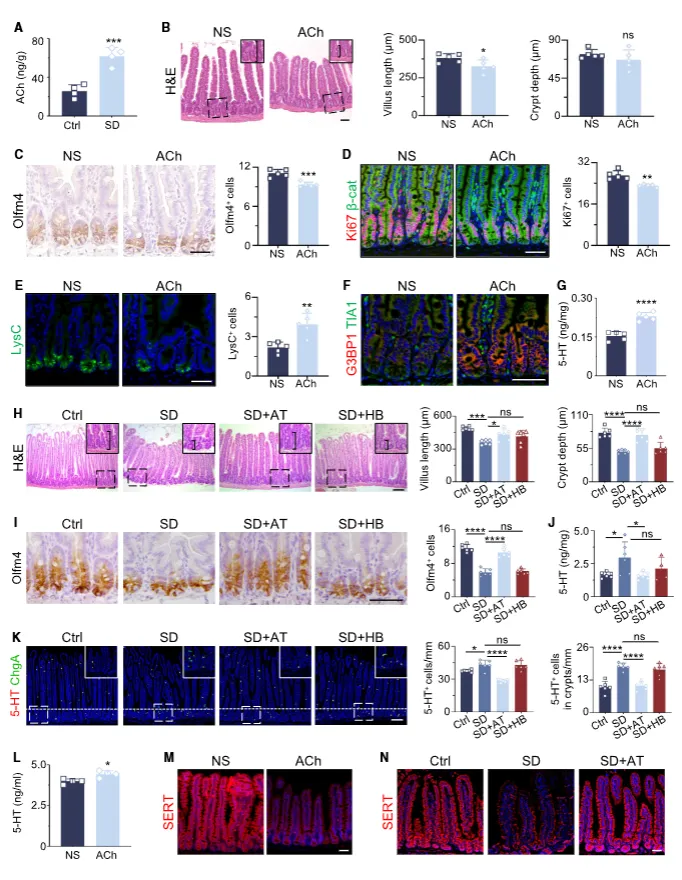
图6:乙酰胆碱升高导致肠道内5‑羟色胺过量积累
睡眠剥夺异常激活脑干迷走神经背核(DMV),钙信号与化学遗传学实验证实DMV过度兴奋通过迷走神经释放乙酰胆碱。抑制DMV可逆转睡眠剥夺导致的肠道损伤,明确DMV是感知睡眠障碍的中枢节点(图7)。
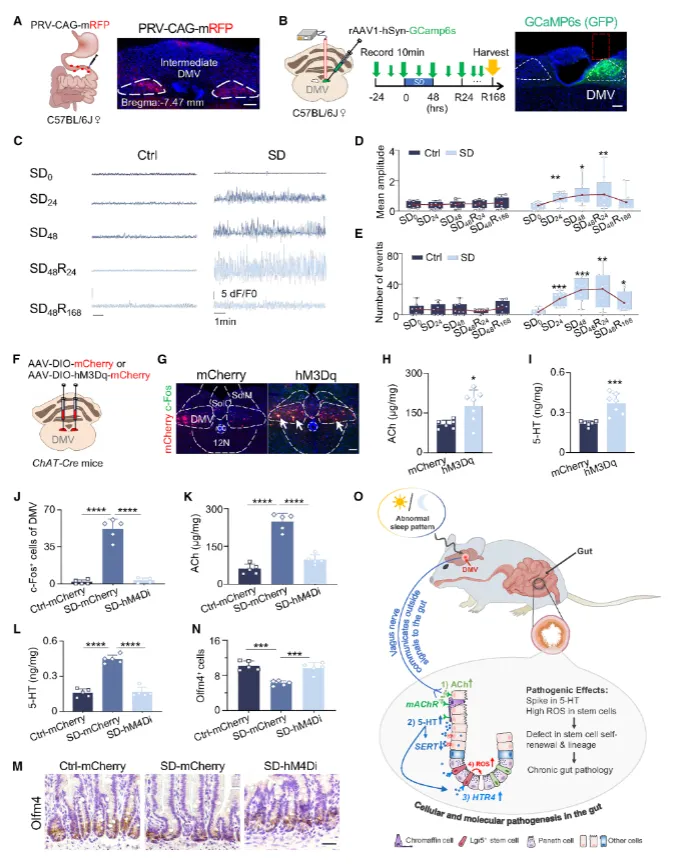
图7:迷走神经背核是介导睡眠剥夺调控肠道的中枢区域
聚焦“神经-干细胞交互”方向,可复刻至慢性应激、抑郁或昼夜节律紊乱模型,优先检测肠道5-HT、ROS及干细胞标志物(Lgr5/Olfm4),验证通路保守性。
必备睡眠剥夺仪(或自制多平台水浴)、迷走神经切断术器械、光纤钙记录系统(可用化学遗传替代)、单细胞测序(可外包)。抗体需备c-Fos、ChAT、5-HT、HTR4、p-eIF2α及K48泛素。
先SD时长严格2天(过长致死),取材定于近端空肠(损伤最显著)。先验证5-HT升高和ROS表型(Tph1 KO小鼠为金标准),再行迷走神经干预。建议先做体外类器官验证5-HT直接效应,再推进体内复杂手术。
本研究揭示睡眠剥夺通过异常激活DMV-迷走神经-肠道轴,诱导乙酰胆碱依赖的5-HT爆发,经HTR4受体介导肠道干细胞氧化应激与功能障碍。该发现阐明脑-肠神经调控新通路,为睡眠相关胃肠病提供了潜在治疗靶点。

微信号:TVZZ0808
拆解高分逻辑,定制专属方案




