一、急性睡眠剥夺损害ISC功能并破坏肠上皮细胞更新
本研究发现,急性睡眠剥夺破坏小鼠睡眠与行为,损害小肠近端及中段肠道干细胞功能和再生能力,引发肠道病理且不依赖肠道微生物群(图1)。
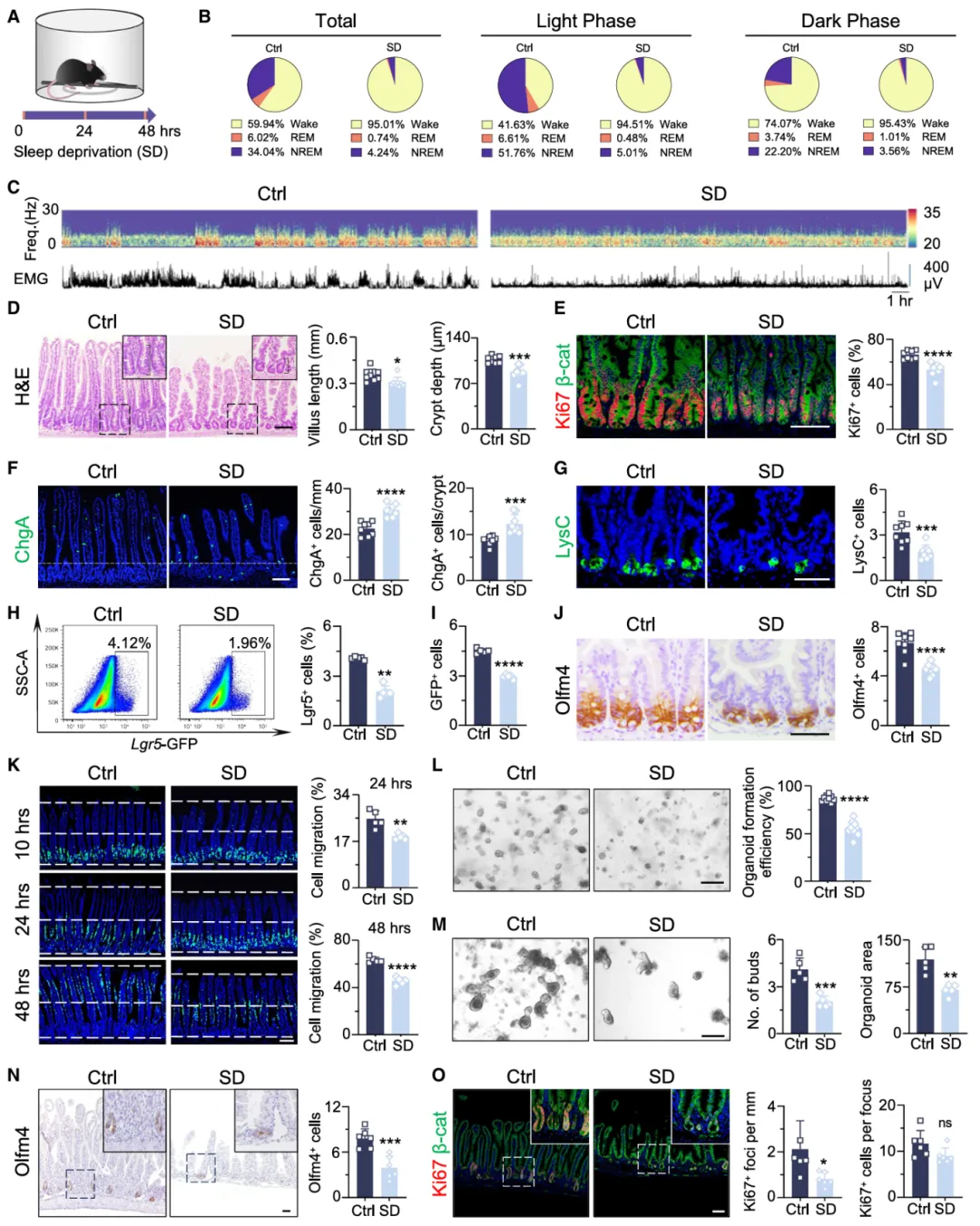
图1.急性睡眠剥夺损害肠道干细胞功能并破坏上皮细胞更新
二、短期SD通过激活翻译应激反应损害ISC
蛋白质组学分析表明,SD 通过诱导肠道选择性氧化应激,激活 ISC 翻译应激、自噬及泛素 - 蛋白酶体通路,抗氧化剂可挽救 ISC 功能损伤(图2)。
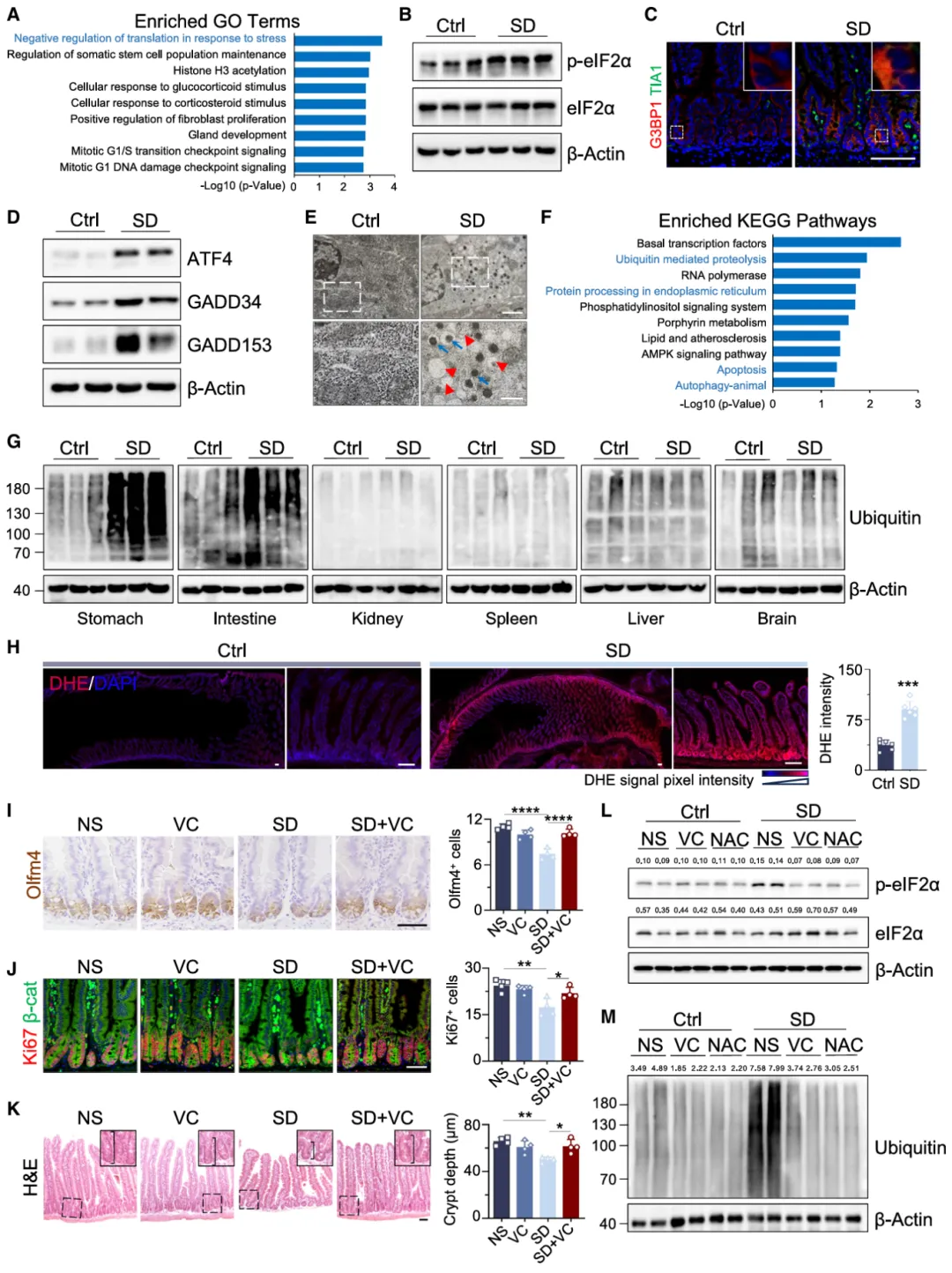
图2.短期睡眠剥夺通过激活翻译应激反应损害肠道干细胞
三、短期SD破坏5-HT稳态并诱导肠道氧化应激
睡眠剥夺使小鼠肠道 5‑羟色胺异常升高,既源于合成增加,也因再摄取减少。5‑羟色胺可直接诱发肠道氧化应激与干细胞损伤,是介导睡眠剥夺致肠道病变的关键分子(图3)。
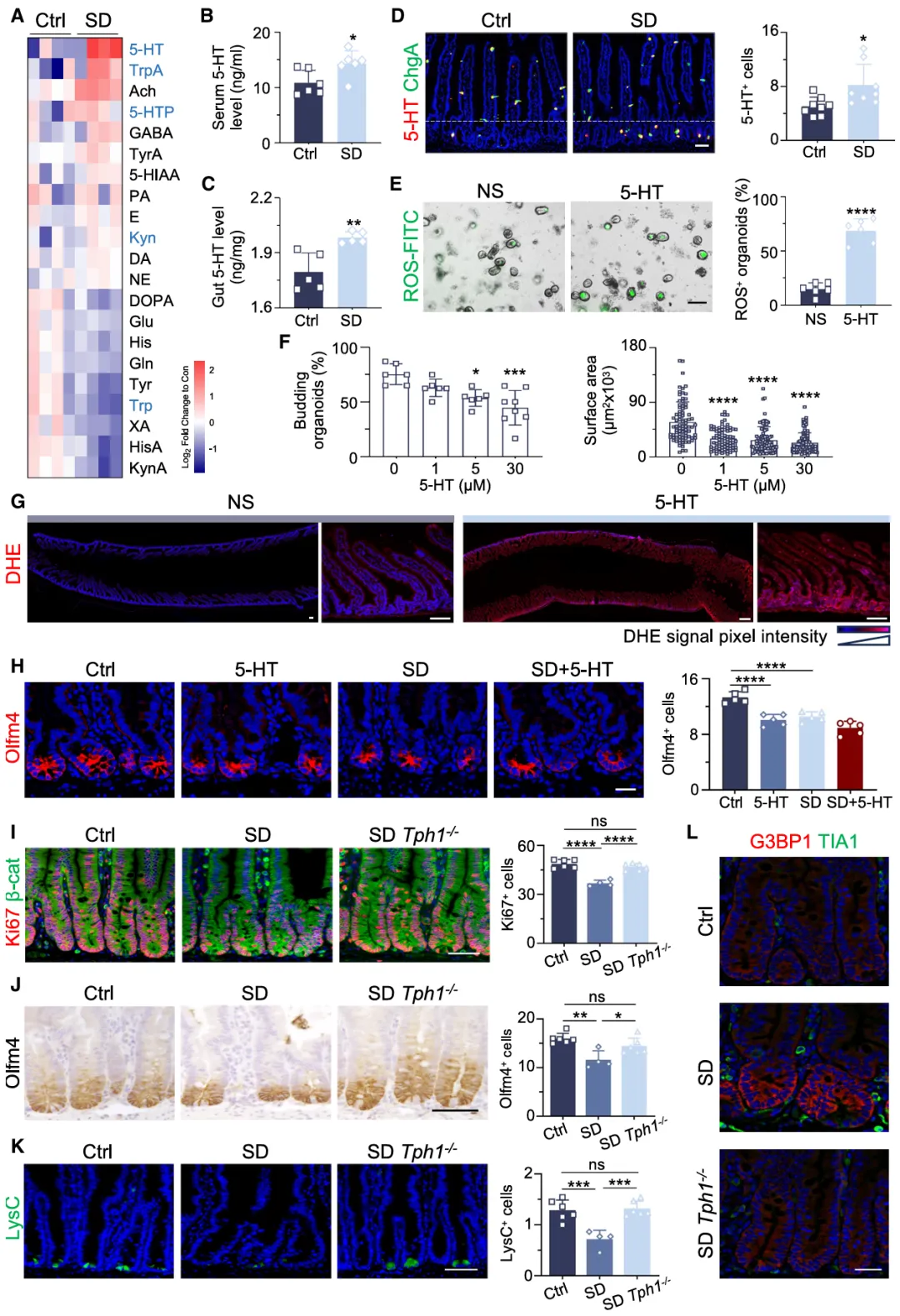
图3.急性睡眠剥夺破坏肠道 5-羟色胺稳态并诱导氧化应激
四、ISCs通过其同源受体HTR4响应5-HT
Htr4 是肠道干细胞主要的 5‑羟色胺受体,睡眠剥夺后表达上调。激动剂可模拟肠道损伤,拮抗剂与条件性敲除则能缓解,证实其介导 5‑HT 对 ISC 的损伤作用(图4)。
图4.肠道干细胞通过其受体 HTR4 对 5-羟色胺作出响应
五、迷走神经激活连接SD与肠道
HPA 轴和交感神经系统不参与睡眠剥夺的中枢信号向肠道传递;而双侧迷走神经切断可阻断睡眠剥夺诱导的肠道 5-HT 升高及肠道损伤,证实迷走神经激活介导该过程(图5)。
图5.迷走神经激活将睡眠剥夺与肠道联系起来
六、升高的Ach驱动肠道中的5-HT积累
睡眠剥夺使肠道乙酰胆碱升高,通过激活上皮毒蕈碱受体 Chrm3,促进 5-HT 释放并抑制其再摄取,引发肠道干细胞损伤(图6)。
图6.乙酰胆碱升高驱动肠道 5-羟色胺积累
七、SD对肠道的影响起源于DMV
筛选与逆行示踪证实,DMV 是唯一介导睡眠剥夺信号的脑区。其异常激活通过迷走神经释放乙酰胆碱,调控 5-HT 与氧化应激,造成肠道干细胞损伤(图7)。
图7.迷走神经背侧运动核是介导睡眠剥夺调控肠道的中枢脑区