2026年2月,郑州大学第一附属医院团队在期刊《Frontiers in Immunology》(IF:5.9)在线发表题为:Integrated multi-omics, spatial profiling and organoid modeling drive transformative advances in chronic liver disease and hepatocellular carcinoma immunomicroenvironment research的高水平研究论文。
慢性肝病(CLD)是全球重大的公共卫生挑战,需要系统地理解其复杂的免疫病理机制。
本综述全面总结了前沿技术在慢性肝病免疫学研究中的突破性应用,包括单细胞测序、空间转录组学和器官类模型:单细胞测序以前所未有的分辨率解析免疫细胞异质性,识别稀有细胞亚群,并通过多组学整合揭示动态变化和调控网络;空间转录组学通过在门管区、纤维化隔墙和肿瘤微环境等结构背景下描绘免疫-基质相互作用,补充了单细胞测序的研究,揭示空间组织化的免疫逃逸机制和微环境重塑;器官类技术构建人源化肝-免疫模型,重现疾病特异性特征,如纤维化、脂肪性肝炎和肝细胞癌,从而实现机制验证、药物筛选和个体化治疗探索。
多组学分析、空间映射和器官类建模的协同整合正在推动慢性肝病免疫学范式的转变——从静态细胞描述迈向时空机制解码,从群体水平洞察转向个体化病理生理与治疗预测。这些先进方法为建立针对肝脏免疫微环境时空调控的精准免疫治疗策略奠定了技术基础。
1. 系统整合单细胞测序、空间转录组学和类器官模型三大前沿技术,构建从细胞分辨率到空间定位再到功能验证的完整研究链条,实现慢性肝病免疫微环境的多维度解析。
2. 利用单细胞测序技术识别出AIF1+B细胞、CX3CR1+CD63+肝门相关巨噬细胞等稀有致病细胞亚群,揭示其在自身免疫性肝炎和代谢功能障碍相关脂肪性肝炎中的特异性功能。
3. 通过空间转录组学精确定位门脉区、纤维化间隔和癌灶区域的三维免疫微环境特征,发现肿瘤免疫屏障结构是肝癌免疫治疗耐药的关键空间机制。
4. 建立人源化肝免疫类器官模型,成功模拟肝纤维化、脂肪性肝炎和肝癌的病理特征,实现免疫代谢交互作用的体外机制验证和个体化药物筛选。
5. 提出多组学数据整合的计算分析框架,结合RNA速率分析和谱系追踪工具,动态解析免疫细胞状态转换轨迹,为精准免疫分型和治疗靶点发现提供新策略。
Figure 1展示了慢性肝病免疫微环境研究的核心技术流程与分析框架。该图呈现了从样本处理到多组学整合的完整技术路径:单细胞测序通过单细胞悬液获取数据,经t-SNE聚类识别新细胞亚群;空间转录组学利用组织切片spot测序,绘制细胞在门脉区、纤维化区域和癌灶等功能区的分布与互作网络;类器官技术则实现疾病建模、机制验证和药物筛选。这三种技术协同形成从细胞分辨率到空间定位再到功能验证的完整研究链条,并通过多组学整合输出新细胞亚群、细胞互作网络和功能空间区域三大核心分析维度。
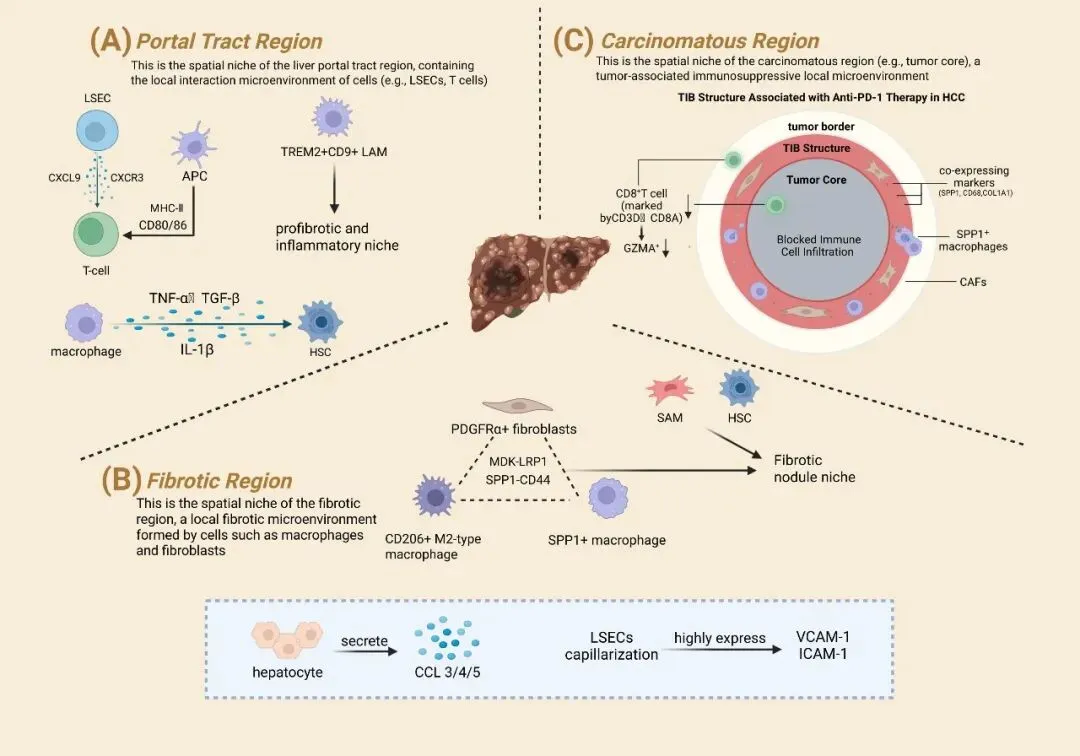
Figure 2呈现了慢性肝病三个关键解剖区域的免疫微环境特征及共享的血管-免疫调控机制。图A显示门脉区是免疫应答启动的关键位点:炎症性肝窦内皮细胞分泌CXCL9招募CXCR3+T细胞,活化巨噬细胞释放IL-1β,TNF-α/TGF-β上调驱动炎症和肝星状细胞活化,抗原提呈细胞高表达MHC-II和CD80/86促进T细胞活化,TREM2+CD9+脂质相关巨噬细胞聚集形成炎症微环境。图B展示纤维化区域的"纤维化生态位":PDGFRα+成纤维细胞、CD206+M2型巨噬细胞和SPP1+巨噬细胞通过MDK-LRP1/SPP1-CD44互作激活肝星状细胞,57个上调基因(如TIMP1/COL1A1)支持其促纤维化特征。图C揭示癌灶区域的肿瘤免疫屏障结构:SPP1+巨噬细胞与癌相关成纤维细胞在肿瘤边缘共定位,形成物理屏障阻断CD8+T细胞浸润,介导抗PD-1治疗耐药。底部插图展示肝细胞分泌CCL3/4/5诱导肝窦内皮细胞毛细血管化,高表达VCAM-1/ICAM-1的共享血管-免疫调控机制。
原文链接:
https://pubmed.ncbi.nlm.nih.gov/41668742/
版权声明
标注‘原创’仅代表原创编译,本平台不主张对原文的版权。本平台转载仅出于学术交流和传播信息的需要,不代表本平台观点或证实其内容的真实性。原文版权归原作者所有,作者如不希望被转载或有侵权行为,请联系本平台删除。