郑州大学张毅等团队Signal Transduction and Targeted Therapy!!CLDN18.2靶向IL-7/XCL1武装CAR-T细胞:消化道癌治疗新策略
- 2026-03-31 06:20:09
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

癌症在全球范围内仍是导致死亡的主要原因之一,尽管手术、放疗、化疗和靶向治疗等传统手段在过去几十年中一定程度上降低了死亡率,但临床效果仍存在局限,亟待创新方法突破困境。嵌合抗原受体T细胞(CAR-T)疗法通过将识别肿瘤表面抗原的单链可变片段导入T细胞,使其特异性攻击癌细胞,在血液肿瘤中已显示出潜力,然而在实体瘤如消化道癌中的应用受到肿瘤微环境抑制和CAR-T细胞功能不足的制约。郑州大学张毅等团队针对这一挑战,开发了针对Claudin18.2(CLDN18.2)的第四代CAR-T细胞,该细胞同时分泌白细胞介素-7(IL-7)和趋化因子XCL1,被命名为ExCAR-T细胞(在临床试验中称为RD07细胞)。这项研究旨在通过增强CAR-T细胞的持久性和免疫激活能力,改善对消化道癌的治疗效果。相关成果于2026年3月9日发表在《Signal Transduction and Targeted Therapy》期刊上,论文标题为“Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armed CAR-T cells in digestive tract cancer: preclinical and clinical analysis”。该工作从基础研究延伸至临床验证,为消化道癌患者提供了新的治疗思路。
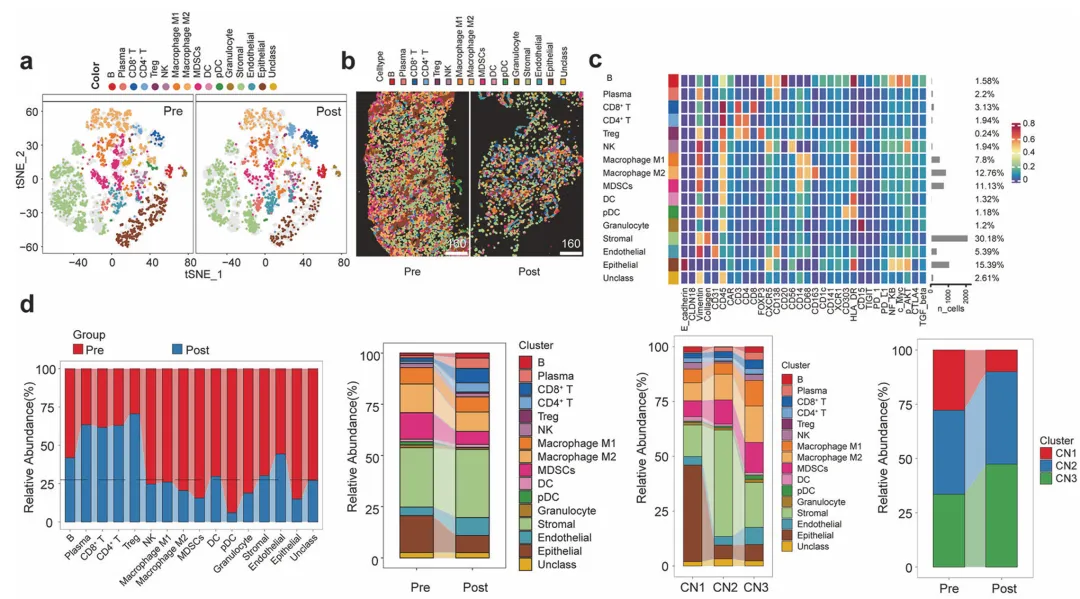
在临床前研究中,ExCAR-T细胞在小鼠消化道癌模型中表现出显著且持久的抗肿瘤效果。通过激活CAR-T细胞自身特性以及调动内源性免疫细胞反应,该疗法有效抑制了肿瘤生长。进一步临床试验针对既往系统治疗失败的消化道癌患者展开,RD07细胞展示出良好的耐受性,在10名参与试验的患者中,7名患者出现肿瘤消退现象。特别值得注意的是,在CLDN18.2表达水平中至高度的患者群体中,完全缓解率达到100%,表明靶向策略的有效性与生物标志物表达相关。单细胞RNA测序结合空间景观分析揭示,RD07治疗不仅能直接发挥细胞毒性作用,还可重塑肿瘤微环境,激活内源性免疫细胞如T细胞和巨噬细胞,从而增强整体抗肿瘤应答。在达到部分缓解的患者中,研究人员检测到CAR-T细胞毒性活性提升以及T细胞受体克隆型扩增,印证了该疗法对免疫系统的广泛调节能力。
综合 preclinical 与临床数据,RD07细胞疗法在消化道癌治疗中展现出可观的安全性及疗效,其核心优势在于双管齐下:既通过CLDN18.2靶向直接清除肿瘤细胞,又利用IL-7和XCL1分泌改善免疫微环境,克服实体瘤治疗障碍。这一策略为CAR-T疗法在实体瘤领域的应用提供了新范式,支持RD07作为创新治疗方案的进一步开发。未来研究可聚焦于优化患者筛选标准、探索联合疗法以及长期随访评估,以推动其临床转化。总体而言,该成果不仅深化了对CAR-T细胞作用机制的理解,也为消化道癌患者带来了切实希望,标志着精准免疫治疗向前迈出重要一步。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
