郑州大学陈学年团队 | 铜催化丙硼烷加合物 (L·B₃H₇) 与重氮化合物的 B−H 键插入反应
- 2026-04-22 20:03:35
01
研究背景
B−H 键插入反应是形成 C−B 键最直接的方法之一,能高效合成各类有机硼化合物。由于亲电卡宾需富电子硼烷参与反应,故底物常选用 BH3 与强路易斯碱的加合物。作者课题组近期系统研究了 B3H7-B3H8− 体系,阐明了基于 B−H 键亲核性的形成机制,改进了碱金属盐合成法,并探究了其相互转化、还原反应及相关 N-杂环加合物的合成与反应性。然而,相较于上述基础性质的系统研究,B3H7 或 B3H8− 的 B−H 键区域选择性官能化却鲜有报道,目前仅限于少数卤化反应案例。
02
研究内容
近日,郑州大学陈学年教授团队报道了一种通过铜催化丙硼烷加合物 (L·B3H7) 与重氮化合物的 B−H 键插入反应,对丙硼烷进行高度区域选择性的官能团化。其中与多核硼烷配位的路易斯碱无需超强碱。该方法表现出较高的产率、广泛的底物适用性,以及在温和条件下优异的官能团兼容性。值得注意的是,反应中的 B−H 键具有高度选择性,位于丙硼烷的底部 B(2) 位置,从而形成具有硼立体中心的化合物。B(2)-取代的丙硼烷产物可以继续与 α-重氮化合物反应,形成 B(2,3)-二取代丙硼烷衍生物。此外,这种方法还可以用于药物分子的 10B 标记,为 BNCT 靶向药物的研发提供了新的合成途径 (图 1)。
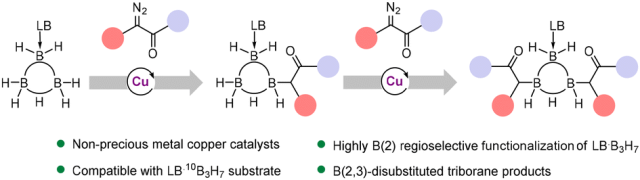
图1 铜催化卡宾插入丙硼烷加合物的 B−H 键。
通过反应条件的筛选,确定了最佳反应条件:使用 10 mol% 的 Cu(MeCN)4PF6 作为催化剂,12 mol% 的 NaBArF 作为添加剂,2 当量的重氮底物,在二氯甲烷中室温反应 12 小时。随后,对重氮类底物范围做了详细的评估 (图 2)。
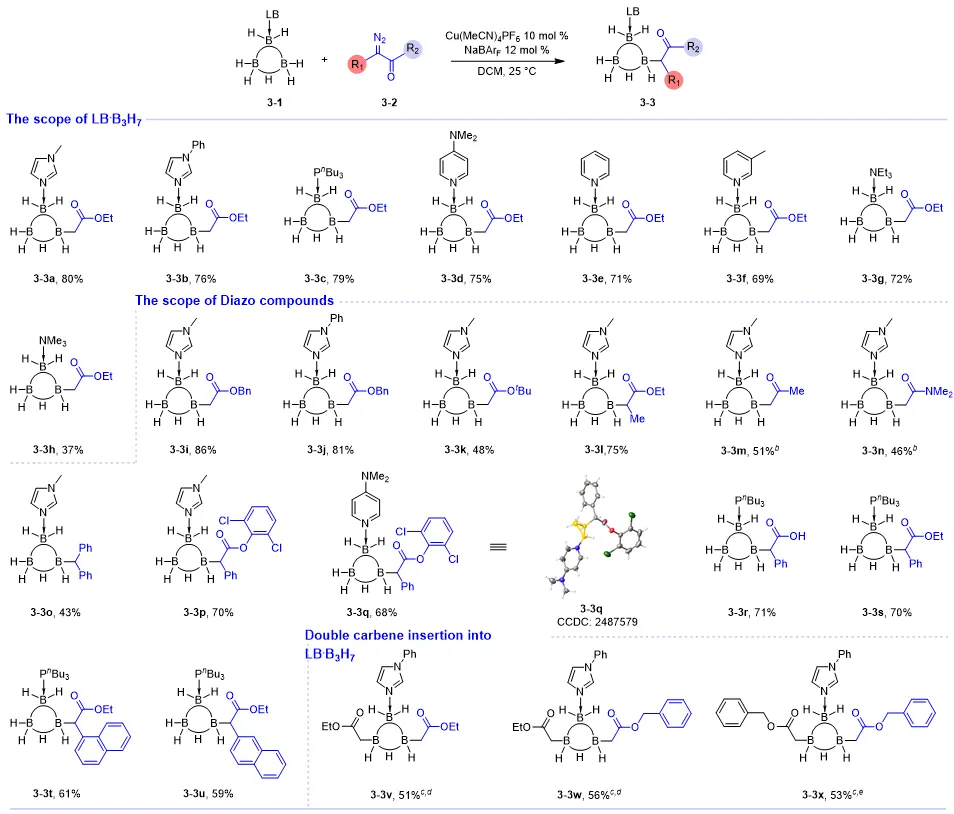
图2 底物范围。
结合机理实验及已报道文献,提出了可能的反应机理:首先,重氮底物与铜配位形成中间体 Int-1,再经过消除释放一分子 N2,从而形成高活性的铜卡宾中间体 Int-II。丙硼烷加合物的 B(2)−H 键通过过渡态 TS-I 与 Int-II 发生协同卡宾插入反应,形成 B(2)−C 键,最终生成产物 (图 3)。
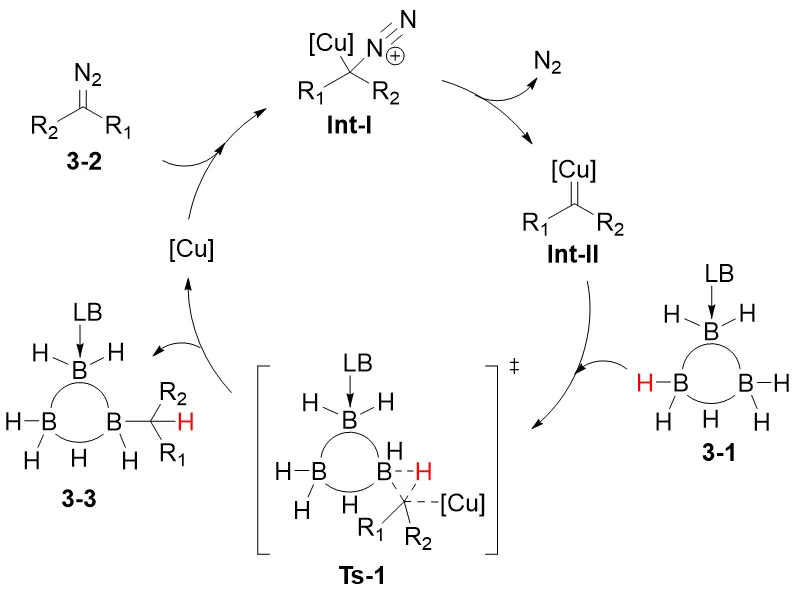
图3 可能的反应机理。
03
总结展望
在国家自然科学基金面上项目等基金的资助下,陈学年教授团队发展了一种铜催化策略,实现了卡宾对丙硼烷 B−H 键的区域选择性插入。该方法为官能化有机硼烷的制备及硼手性中心的构建提供了一条通用途径,并有望应用于 10B 标记药物及 BNCT 领域。
04
论文信息

A copper-catalyzed B–H bond insertion reaction of triboranes (L·B3H7) with diazo compounds
Lei Cao (曹磊), Jia-Rui Chang, Xi-Meng Chen (陈西孟), Yan-Na Ma (马艳娜) and Xuenian Chen (陈学年)
Org. Chem. Front., 2026, Advance Article
https://doi.org/10.1039/D6QO00098C
*文中图片皆来源上述文章
点击“阅读原文”直达上述文章
05
通讯作者简介

陈学年
郑州大学
陈学年,二级教授,博士生导师,郑州大学学科特聘教授,河南省硼化学与先进能源材料重点实验室主任,河南省化学会常务理事。长期从事硼化学,金属有机化学,无机化学,配位化学和材料化学等领域研究。2013 年回国后主持两项区域创新发展联合重点基金和三项国家自然科学基金面上项目。在 Chem. Soc Rev., J. Am. Chem. Soc., Angew. Chem. Int. Ed., Nat. Commun., Chem. Sci. 等期刊发表学术论文 100 余篇,拥有多项美国和中国专利技术。多次应邀在国际、国内会议和著名高校、科研院所做邀请报告。
课题组网页:www.boronchemistry.net
推荐阅读
川大附属成都市第二人民医院林世博团队综述 | 过渡金属催化环化反应合成双(杂)芳基轴手性分子
川大曾小明/董召文团队 | Cr(II)-Phen 催化实现烷基 OTf/卤代物与氯代锡的交叉电偶联构筑 C(sp³)–Sn 键

微信改版,公众号文章不再以时间轴排列啦!
将Frontiers Journals设为星标⭐ 不错过更多精彩内容!
喜欢今天的内容?
👇 就来分享、点赞、在看三连吧 👇
