郑州大学董子钢等团队PNAS!!胃癌化疗耐药新机制,PHGDH磷酸化成关键开关
- 2026-04-25 16:58:58
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

代谢重编程是癌症进展的核心特征,而丝氨酸代谢在胃癌发生发展及化疗耐药中的作用长期未明。针对这一难题,郑州大学董子钢等团队在《美国科学院院刊》(PNAS)发表研究,首次揭示无赖氨酸激酶1(WNK1)介导的PHGDH磷酸化是调控胃癌丝氨酸代谢重编程、驱动奥沙利铂耐药的关键机制,并为化疗响应预测提供了新型生物标志物。研究通过整合多组学分析与功能验证,为胃癌精准治疗开辟了新方向。
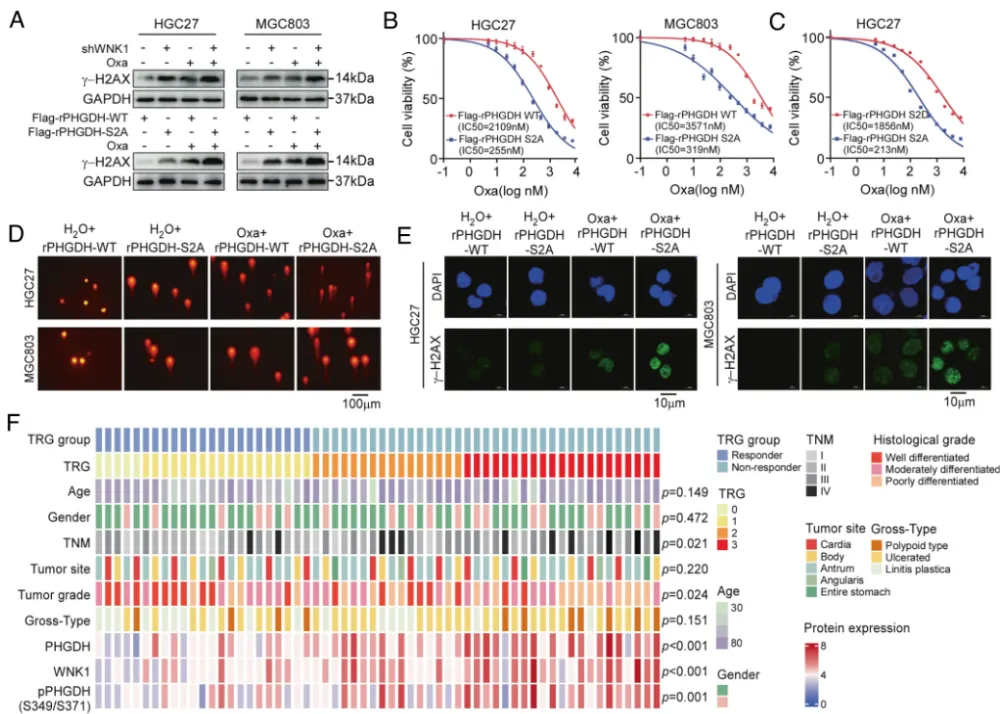
研究通过代谢组学与13C标记代谢通量分析,发现胃癌组织丝氨酸水平显著升高,其合成主要依赖限速酶PHGDH的异常激活。机制上,团队鉴定出WNK1是PHGDH的上游激酶,可在其ASB结构域的Ser349和Ser371位点进行磷酸化修饰。该修饰不仅增强PHGDH催化活性,还通过阻断E3泛素连接酶UHRF2介导的泛素化降解,提升蛋白稳定性。体内实验显示,WNK1基因敲除小鼠胃部肿瘤负荷显著降低,伴随丝氨酸水平下降与氧化还原失衡;临床样本分析进一步证实,PHGDH活性、丝氨酸及谷胱甘肽(GSH)丰度与奥沙利铂耐药呈正相关,非响应者肿瘤组织中p-PHGDH(S349/S371)水平显著更高。这表明WNK1-PHGDH轴通过促进丝氨酸合成、维持GSH/GPX4抗氧化系统,帮助癌细胞逃避氧化应激与化疗杀伤。
该研究阐明了WNK1-PHGDH-丝氨酸代谢轴在胃癌中的双重作用:既是驱动肿瘤进展的代谢开关,也是化疗耐药的关键漏洞。PHGDH磷酸化水平(p-PHGDH S349/S371)可作为预测奥沙利铂响应的独立生物标志物,在60例临床队列中预测准确率达0.78,外部验证集亦达0.76。更重要的是,靶向PHGDH(如抑制剂NCT-503)可显著增敏奥沙利铂疗效,在患者来源类器官模型中联合治疗使肿瘤抑制率提升超30%。这一发现为胃癌患者分层治疗提供依据,提示未来可通过检测p-PHGDH水平筛选化疗获益人群,或联合PHGDH抑制剂突破耐药瓶颈。研究不仅深化了对氨基酸代谢调控肿瘤行为的认知,更为临床转化提供了可操作的代谢干预靶点。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
