IF42.5!苏州大学&郑州大学用“国自然”荣登《Cell》顶刊!揭示AARS1乳酰化p53促癌机制!
- 2026-04-18 19:37:44





乳酸是糖酵解的代谢产物,近年发现其可通过组蛋白乳酸化调控基因表达,但细胞内乳酸如何被感知并转化为蛋白质乳酸化的机制尚不明确。苏州大学团队通过全基因组CRISPR筛选发现,丙氨酰-tRNA合成酶AARS1是细胞内乳酸传感器和乳酸转移酶,直接结合乳酸并通过ATP依赖方式催化全局赖氨酸乳酸化。
AARS1介导p53的K120和K139位点乳酸化,抑制p53的液-液相分离、DNA结合和转录活性,促进肿瘤发生。β-丙氨酸可竞争性抑制乳酸与AARS1结合,阻断p53乳酸化并抑制肿瘤生长。该研究揭示了代谢物乳酸直接调控蛋白质功能的新范式。
📢如果你也想用“国自然”发文的话,关注西瓜生信,联系我们带你进一步了解~


文章标题:丙氨酰-tRNA合成酶AARS1是乳酸传感器和乳酸转移酶,通过乳酸化p53促进肿瘤发生
发表期刊:Cell
发表时间:2024年4月22日
影响因子:IF42.5/Q1

研究背景

瓦博格效应是癌症的标志性代谢特征,肿瘤细胞即使在有氧条件下也依赖糖酵解产生大量乳酸。传统认为乳酸是代谢废物,但近年发现乳酸可通过组蛋白乳酸化修饰调控基因表达。抑制p53的液-液相分离、DNA结合和转录活性,从而促进肿瘤发生。β-丙氨酸可竞争性抑制该过程,为癌症治疗提供新策略。

研究方法

本研究通过TCGA数据库分析发现乳酸与p53信号通路负相关,体内外实验证实乳酸抑制p53活性并促进p53乳酸化。全基因组CRISPR筛选鉴定出AARS1为介导p53乳酸化的关键酶。采用MST、CD、EMSA、FRAP、LC-MS/MS等方法系统阐明AARS1催化乳酸-AMP形成及转移至赖氨酸的生化机制。

你也想挑战前沿生信研究方向?你也想拥有同款高分数据库,却苦于不知从何入手?别再观望了,赶紧联系西瓜生信团队!我们提供全方位专业支持,从数据分析到思路设计,助你轻松搞定科研难题!
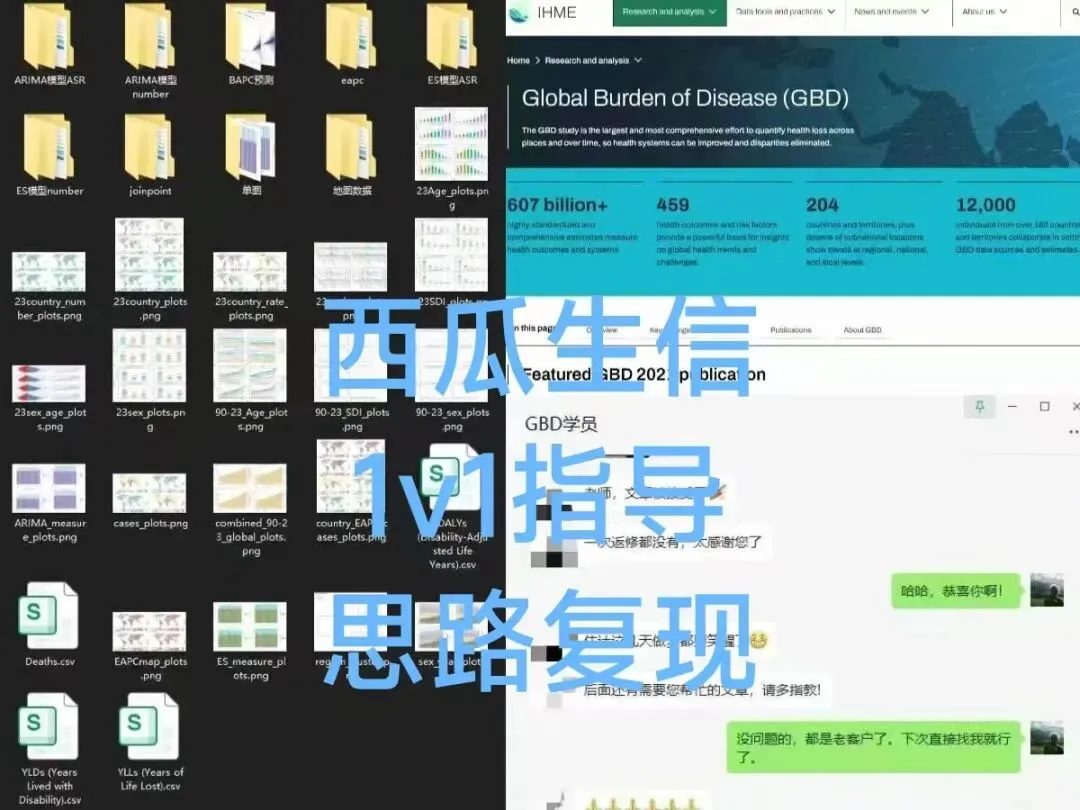

肿瘤来源的乳酸是p53的天然抑制物,通过乳酸化抑制p53
TCGA乳腺癌数据分析显示,高乳酸信号与p53信号通路评分显著负相关。在MMTV-PyMT乳腺癌小鼠模型中,腹腔注射乳酸钠加速肿瘤发生并抑制p53活性。LDHA条件性敲除延迟肿瘤形成、降低肿瘤乳酸含量并增加p53活性(图1)。
体外实验中,乳酸或乳酸钠处理可诱导p53乳酸化,而糖酵解抑制剂2-DG或LDHA抑制剂oxamate减少p53乳酸化并增强p53靶基因表达。利用细胞裂解液而非纯乳酸直接处理p53才能降低其活性,且降低程度与乳酸化水平相关,提示存在催化乳酸化的酶。
全基因组CRISPR筛选鉴定AARS1为全局赖氨酸乳酸化的介导者
构建p53-GFP报告基因的HeLa细胞,经乳酸和Nutlin-3处理后分选GFP高表达细胞进行CRISPR筛选,AARS1是最显著的候选基因。AARS1敲低增强p53报告基因活性和靶基因表达,抑制细胞增殖和集落形成,并阻断乳酸诱导的促肿瘤效应(图2)。
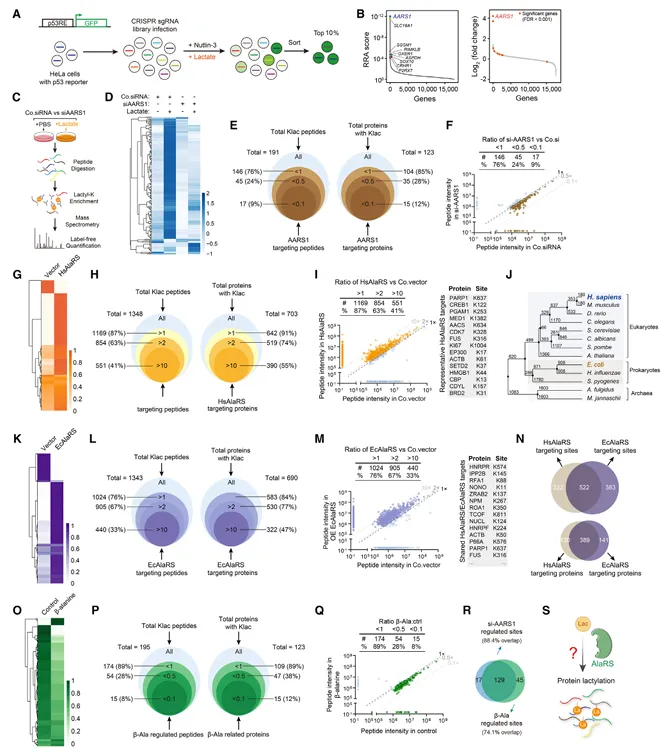
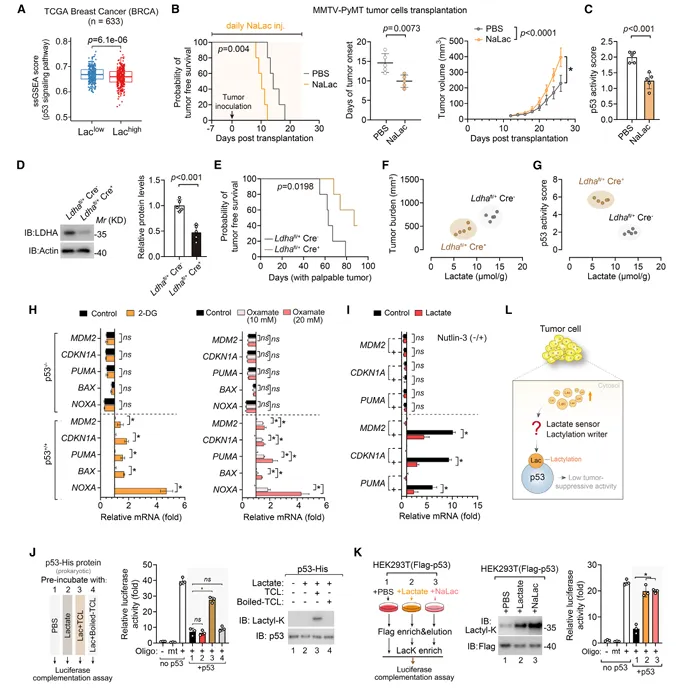
图2.全基因组CRISPR筛选鉴定AARS1为全局赖氨酸乳酸化的介导者
蛋白质组学分析显示,AARS1敲低使约80%的乳酸化肽段强度下降,而AARS1过表达使90%的乳酸化肽段强度升高。大肠杆菌EcAlaRS同样具有催化真核细胞乳酸化的能力,且与AARS1的靶点高度重叠。β-丙氨酸可有效抑制全局乳酸化。
AARS1直接结合乳酸并以ATP依赖方式催化赖氨酸乳酸化
MST分析显示EcAlaRS和HsAlaRS与乳酸的Kd分别约为13 μM和35 μM,β-丙氨酸亲和力更高并可竞争性抑制乳酸结合。分子对接鉴定出保守的乳酸结合残基,突变这些残基完全消除乳酸结合和乳酸化催化活性(图3)。
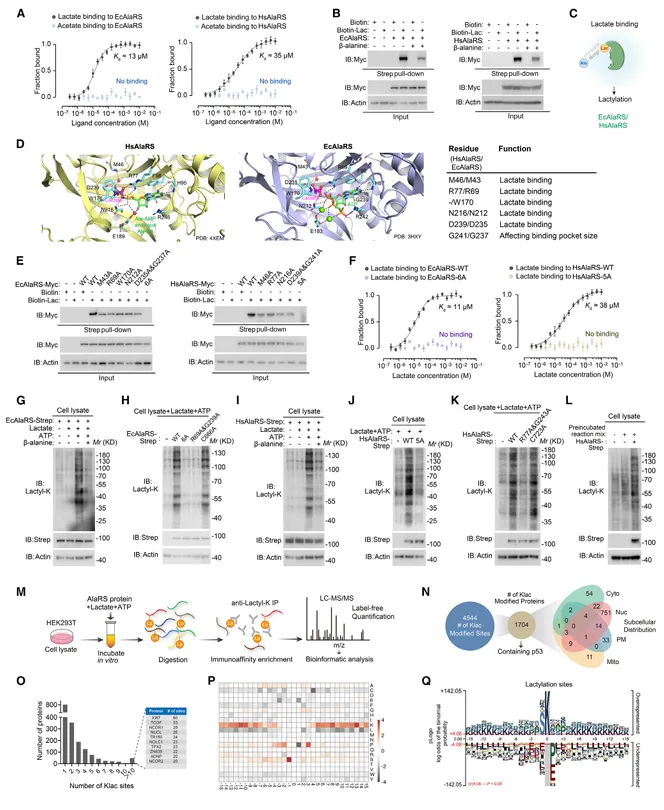
图3.AARS1直接结合乳酸并以ATP依赖方式催化赖氨酸乳酸化
体外反应需要同时存在乳酸、ATP和AARS1,且ATP结合突变体同样失活。通过去除AARS1后无法催化乳酸化,证实AARS1直接转移乳酸基团而非产生可扩散中间体。质谱鉴定出EcAlaRS催化的4,544个乳酸化位点,覆盖1,704个蛋白,乳酸化位点周围氨基酸序列具有偏好性。
AARS1通过ATP依赖的乳酸-AMP中间体将乳酸共价转移至赖氨酸
蛋白质组学显示AARS1是p53的结合蛋白,Co-IP证实两者直接相互作用,Kd约为39 μM和21 μM。在细胞和体外,AARS1-WT而非乳酸或ATP结合突变体可催化p53的K120和K139位点乳酸化,并被β-丙氨酸抑制(图4)。
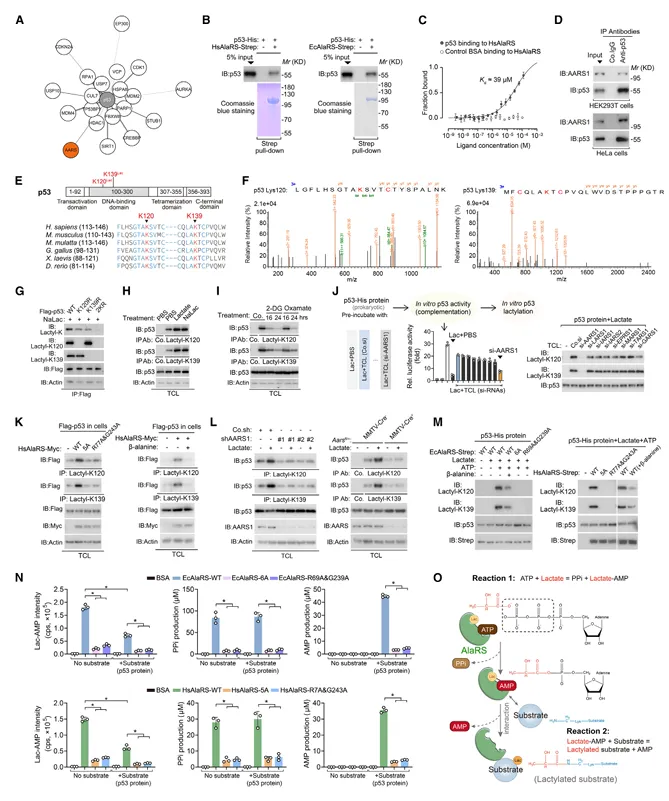
图4.AARS1通过ATP依赖的乳酸-AMP中间体催化赖氨酸乳酸化
AARS1催化乳酸和ATP生成乳酸-AMP并释放焦磷酸,加入底物p53后乳酸-AMP被消耗并产生AMP。AARS1对乳酸的催化效率约为丙氨酸的1/2000,但细胞内乳酸浓度远高于丙氨酸,足以支持乳酸化发生。
p53位点特异性乳酸化削弱其DNA结合和液-液相分离,降低肿瘤抑制功能
p53的K120和K139位于DNA结合域。通过遗传密码扩展技术构建位点特异性乳酸化p53蛋白。EMSA和MST显示,p53Dual-Lac与p53RE-DNA的亲和力降低约1000倍,p53K120-Lac降低约100倍,p53K139-Lac降低约10倍(图5)。
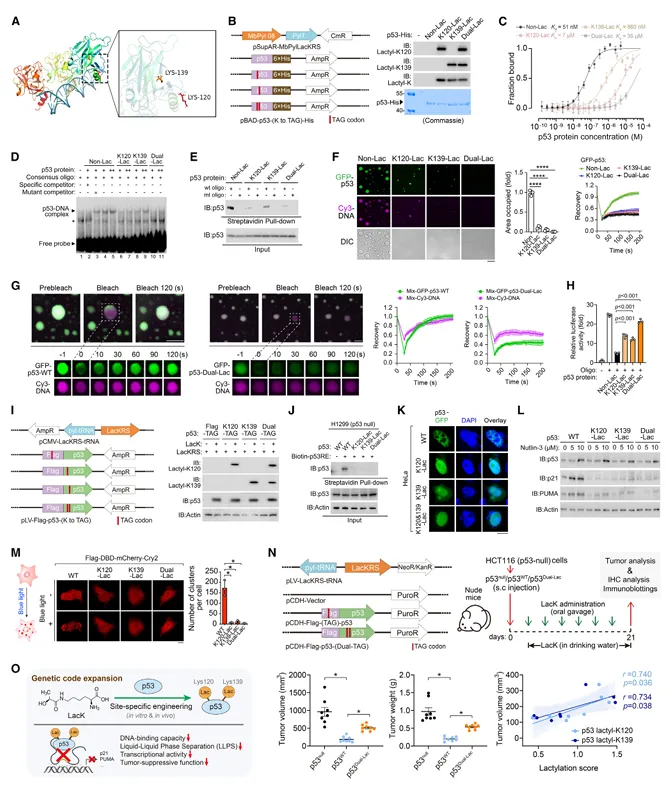
图5.p53位点特异性乳酸化削弱其DNA结合和LLPS
p53Non-Lac与p53RE-DNA可形成液滴,而乳酸化变体形成液滴能力显著减弱。在p53-/-细胞中,表达乳酸化p53的细胞无法结合p53RE-DNA、无法形成核内凝聚体、转录活性降低,且在小鼠体内更具致瘤性。肿瘤中p53乳酸化水平与肿瘤体积正相关。
模拟乳酸化的K120/K139癌症相关突变体表现出LLPS和肿瘤抑制能力降低
分析TP53数据库和COSMIC数据库发现,p53的K120和K139存在多种癌症相关突变突变模拟了乳酸化对电荷的改变(图6)。
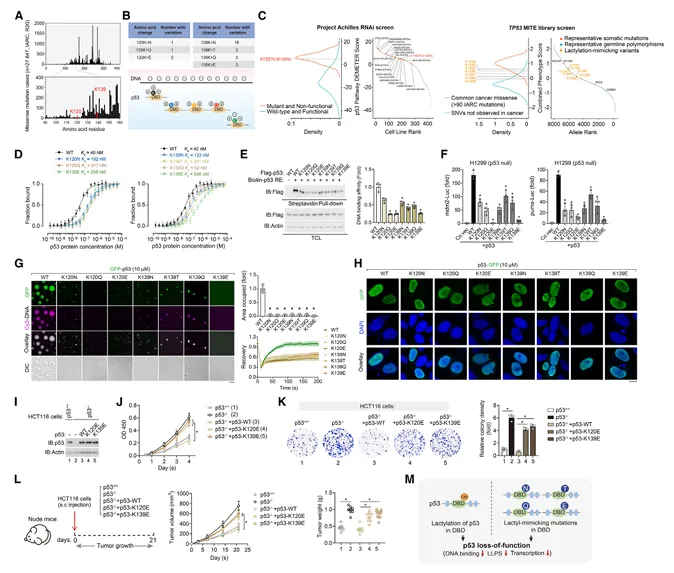
图6.疾病相关的K120/K139模拟乳酸化突变体表现出LLPS和肿瘤抑制能力降低
功能实验显示,K-to-E突变体与p53RE-DNA结合力丧失最严重,转录活性几乎完全消失,LLPS能力受损,在p53-/-细胞中无法抑制增殖、集落形成和异种移植瘤生长。此外,乳酸化与乙酰化在相同位点相互排斥:乳酸化p53不能被乙酰化,乙酰化p53也不能被乳酸化,而乙酰化与乳酸化功能相反。

本研究首次揭示丙氨酰-tRNA合成酶AARS1是细胞内乳酸传感器和乳酸转移酶,通过ATP依赖的乳酸-AMP中间体催化全局赖氨酸乳酸化,并特异性乳酸化p53的K120和K139位点。乳酸化通过中和赖氨酸正电荷,破坏p53 DNA结合域与响应元件的结合,抑制p53的液-液相分离、转录活性和肿瘤抑制功能。
由于AARS1在多种癌症中高表达且与不良预后相关,靶向AARS1-乳酸化轴可能成为广谱抗癌新策略,但需注意AARS1同时具有翻译功能,需选择性干预其乳酸转移酶活性。
📢如果你也想用“国自然”进行发文,思路复现,那就快来联系我们吧~

有需要的朋友联系~

IF30.9!南京大学&南京医科大学联手用“国自然”荣登《Cell》子刊!竟发现父亲运动可通过精子miRNA提升后代耐力!

