郑州大学第一附属医院 | 突破慢性术后痛治疗瓶颈!ACC-CaMKII-AcbC 通路为靶点,解锁疼痛调控新机制
- 2026-04-20 21:21:54

导读:
为探究慢性术后痛(CPOP)的神经环路机制,本研究采用皮肤 / 肌肉切开牵拉(SMIR)模型模拟 CPOP,通过免疫荧光、在体电生理、光纤 photometry、化学遗传学和光遗传学等技术,发现伏隔核核心区(AcbC)神经元在 SMIR 小鼠中异常激活,且接收前扣带回皮层(ACC)CaMKII 阳性神经元的兴奋性投射;抑制 AcbC 神经元或 ACC-CaMKII-AcbC 通路可缓解 SMIR 小鼠的机械痛敏,激活该神经元或通路则在正常小鼠中诱导疼痛表型,证实 AcbC 神经元及 ACC-CaMKII-AcbC 通路在 CPOP 发病中起关键作用,为术后疼痛治疗提供了潜在靶点。
注:该文章发表于《iScience》,该期刊五年影响因子4.7,JCR一区,中科院二区。

本研究聚焦 CPOP 的神经环路机制,首次明确 AcbC 神经元接收 ACC 区 CaMKII 阳性神经元的兴奋性投射,形成 ACC-CaMKII-AcbC 通路;证实该通路和 AcbC 神经元可双向调控疼痛敏感性,SMIR 术后通路活性增强,抑制通路或 AcbC 神经元能缓解痛敏,激活则诱导疼痛;结合多种先进技术,从形态、功能、环路层面系统验证,揭示了 CPOP 中神经环路的特异性变化,为术后疼痛的精准靶向治疗提供了全新靶点,兼具机制创新性与临床转化价值。
慢性术后痛(CPOP)是术后持续超过 3 个月的顽固性疼痛,发生率在 10%-50% 之间,胸外科手术、肢体截肢等术后发生率更高,不仅影响患者康复、增加再入院率,还带来沉重的社会经济负担。中枢敏化是 CPOP 的重要机制,但其相关神经环路的可塑性变化尚不明确。伏隔核(NAc)作为基底节与边缘系统的关键枢纽,参与疼痛调节,其核心区(AcbC)神经元主要为中等棘神经元(MSNs),分为 D1R-MSNs 和 D2R-MSNs 亚型,功能存在差异。前扣带回皮层(ACC)与 NAc 存在神经连接,参与社会疼痛传递等过程,但 ACC-AcbC 通路在 CPOP 中的作用及机制尚未明确,亟需深入研究以填补这一空白,为 CPOP 治疗提供新的理论依据。
动物模型:采用皮肤 / 肌肉切开牵拉(SMIR)法构建 CPOP 小鼠模型,假手术组仅暴露肌腱筋膜不牵拉,以雄性 C57BL/6J 小鼠和 CaMKIIα-ires-Cre 小鼠为研究对象。
行为学检测:通过 von Frey 试验检测 50% 足退缩阈值(PWT50)评估机械痛敏,Hargreaves 试验检测足退缩潜伏期(PWL)评估热痛敏,开放场试验(OFT)评估运动功能。
神经活性检测:免疫荧光染色检测 C-FOS 表达以反映神经元激活;在体电生理记录 AcbC 神经元自发放电频率;光纤 photometry 监测神经元钙信号(GCaMP6s 标记),评估对非伤害性(0.6g)和伤害性(2g)机械刺激的反应。
环路追踪:采用顺行、逆行病毒追踪技术(如 AAV2/9-EF1α-mCherry-DIO、AAV2/Retro-hSyn-mCherry-DIO),验证 ACC-CaMKII 神经元与 AcbC 神经元的连接。
调控实验:化学遗传学(hM4D (Gi) 抑制、hM3D (Gq) 激活)调控 AcbC 神经元或 ACC-CaMKII 神经元;光遗传学(eNpHR3.0 抑制、hChR2 激活)调控 ACC-CaMKII-AcbC 通路,观察疼痛行为变化。

SMIR 小鼠术后 1-14 天同侧后爪 PWT50 显著降低,仅表现为机械痛敏,无热痛敏,且运动功能不受影响;AcbC 区 C-FOS 阳性神经元数量显著增加,且对侧多于同侧,C-FOS 阳性细胞与 D1R-MSNs 共定位比例(52.97%±11.03%)高于 D2R-MSNs(37.52%±5.15%),电生理显示 AcbC 神经元放电频率升高。
光纤 photometry 证实,SMIR 小鼠 AcbC 神经元对 0.6g 和 2g 机械刺激的钙信号反应均显著增强,C-FOS 与 GCaMP 存在共定位。
病毒追踪显示,AcbC 神经元接收 ACC 区 CaMKII 阳性神经元的直接投射,尤其来自 ACC 的 Cg2 亚区。
化学遗传学抑制 AcbC 神经元可升高 SMIR 小鼠同侧 PWT50,激活则降低正常小鼠 PWT50 和 PWL;激活 ACC-CaMKII 神经元可增强 AcbC 神经元钙信号和放电频率,SMIR 小鼠 ACC-CaMKII-AcbC 通路对机械刺激的反应增强。
光遗传学抑制 ACC-CaMKII-AcbC 通路可缓解 SMIR 小鼠机械痛敏,激活则诱导正常小鼠出现机械痛敏和热痛敏,且不影响运动功能。
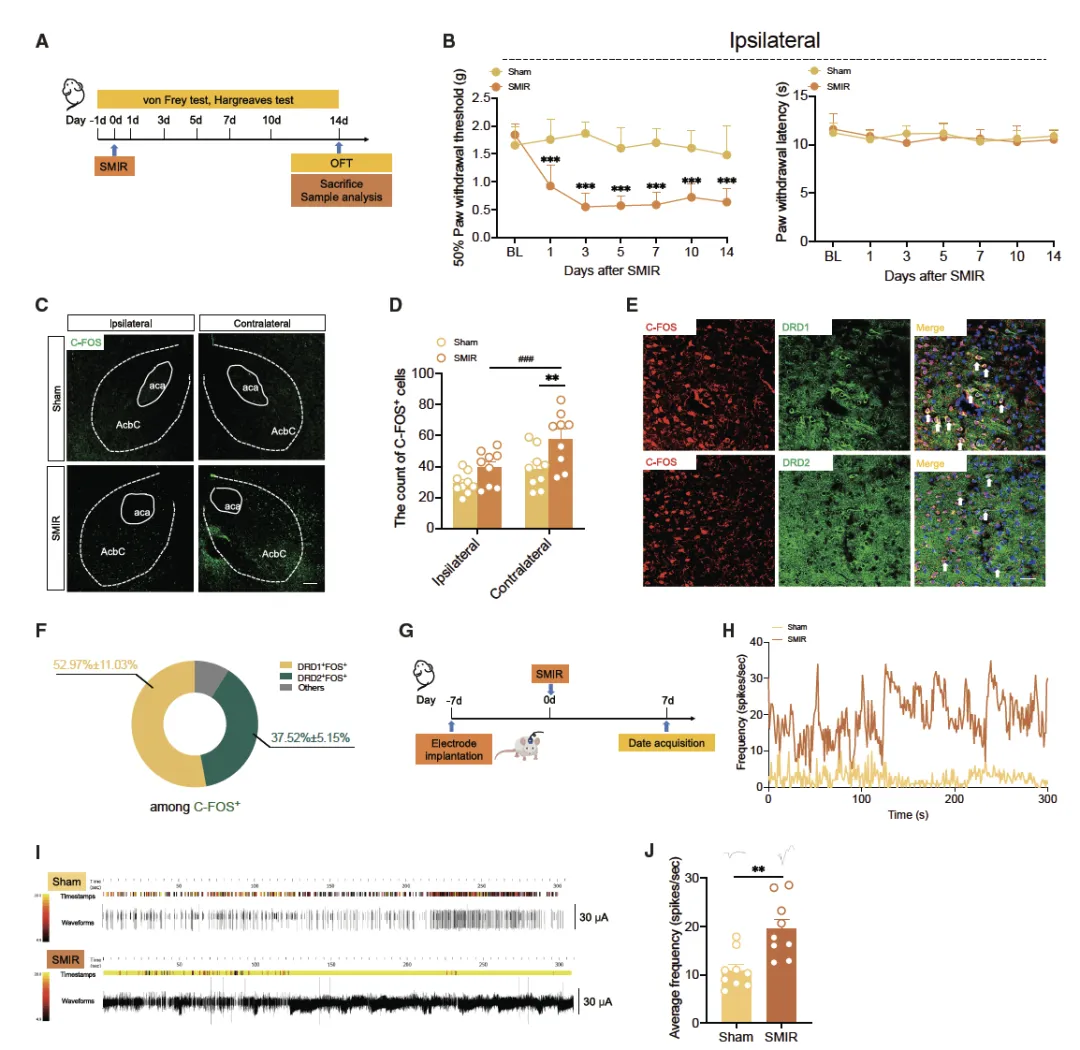
Figure 1:SMIR 小鼠伏隔核核心区(AcbC)神经元显著激活
该图通过一系列实验验证了皮肤 / 肌肉切开牵拉(SMIR)模型构建后,AcbC 神经元的激活状态。首先,行为学测试显示 SMIR 小鼠术后 1-14 天同侧后爪的 50% 足退缩阈值(PWT50)显著降低,仅表现为机械痛敏,而热痛敏(PWL)无明显变化,且开放场试验证明手术未影响小鼠运动功能。随后,免疫荧光染色发现 SMIR 小鼠 AcbC 区的 C-FOS 阳性神经元数量显著增加,且对侧 AcbC 的 C-FOS 阳性细胞密度高于同侧,提示神经损伤后存在偏侧化神经元激活模式,同时 C-FOS 阳性细胞与 D1R-MSNs 的共定位比例(52.97%±11.03%)高于 D2R-MSNs(37.52%±5.15%)。此外,在体电生理记录显示 SMIR 小鼠 AcbC 神经元的自发放电频率较假手术组显著升高,综合这些结果证实 SMIR 手术可诱导 AcbC 神经元异常激活,表现为细胞活性增强。
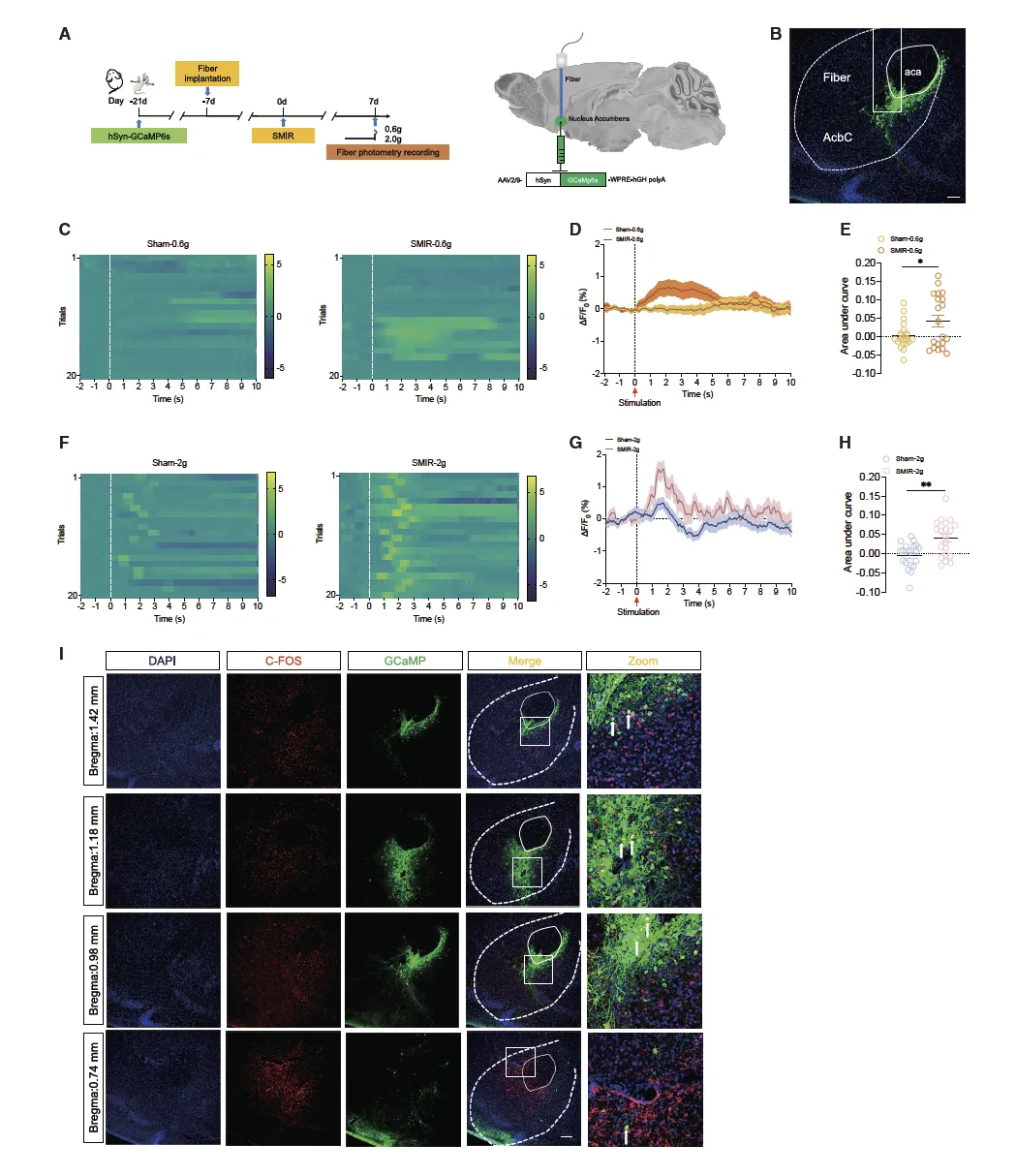
Figure 2:SMIR 小鼠 AcbC 神经元对非伤害性和伤害性刺激的反应增强
此图通过光纤 photometry 技术监测自由活动小鼠的 AcbC 神经元钙信号,探究其对不同机械刺激的响应特性。实验中向小鼠对侧 AcbC 注射 AAV2/9-hSyn-GCaMP6s 病毒并植入光纤,分别用 0.6g(非伤害性)和 2g(伤害性)von Frey 丝刺激后,结果显示假手术组中 0.6g 刺激仅引发 AcbC 神经元轻微钙瞬变,而 SMIR 小鼠的钙信号反应显著增强;2g 刺激下两组均出现钙活性升高,但 SMIR 组的反应幅度远大于假手术组。对曲线下面积(AUC)的定量分析进一步证实,SMIR 组在两种刺激下的钙信号强度均显著增加,且免疫组化结果显示 SMIR 组中 GCaMP 阳性神经元与 C-FOS 阳性细胞存在共定位,表明 SMIR 手术导致 AcbC 神经元处于过度兴奋状态,对非伤害性和伤害性机械刺激的反应性均显著提升。
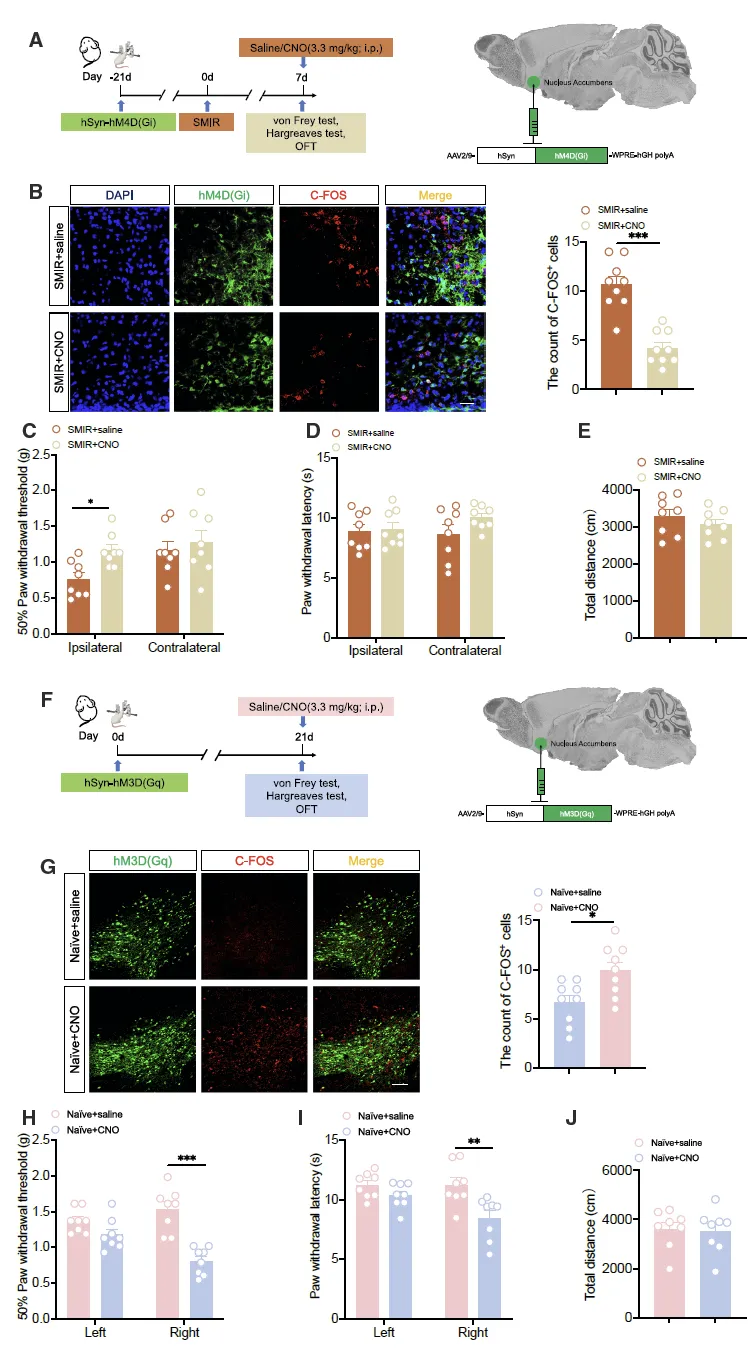
Figure 3:AcbC 神经元双向调控疼痛敏感性
该图借助化学遗传学技术(DREADDs)探究 AcbC 神经元在疼痛调节中的作用。在 SMIR 小鼠对侧 AcbC 注射 AAV2/9-hSyn-hM4D (Gi)-EGFP 病毒后,腹腔注射氯氮平 N - 氧化物(CNO)可有效抑制 AcbC 神经元活性(表现为 C-FOS 阳性细胞减少),并特异性升高 SMIR 小鼠同侧后爪的 PWT50,缓解机械痛敏,且不影响热痛敏和运动功能。反之,向正常小鼠左侧 AcbC 注射 AAV2/9-hSyn-hM3D (Gq)-EGFP 病毒后,CNO 激活 AcbC 神经元会显著降低正常小鼠右侧后爪的 PWT50 和 PWL,诱导疼痛表型,同时不影响运动表现。这些结果表明 AcbC 神经元具有双向疼痛调控作用,激活可诱导伤害性超敏反应,抑制则能减轻机械痛敏。
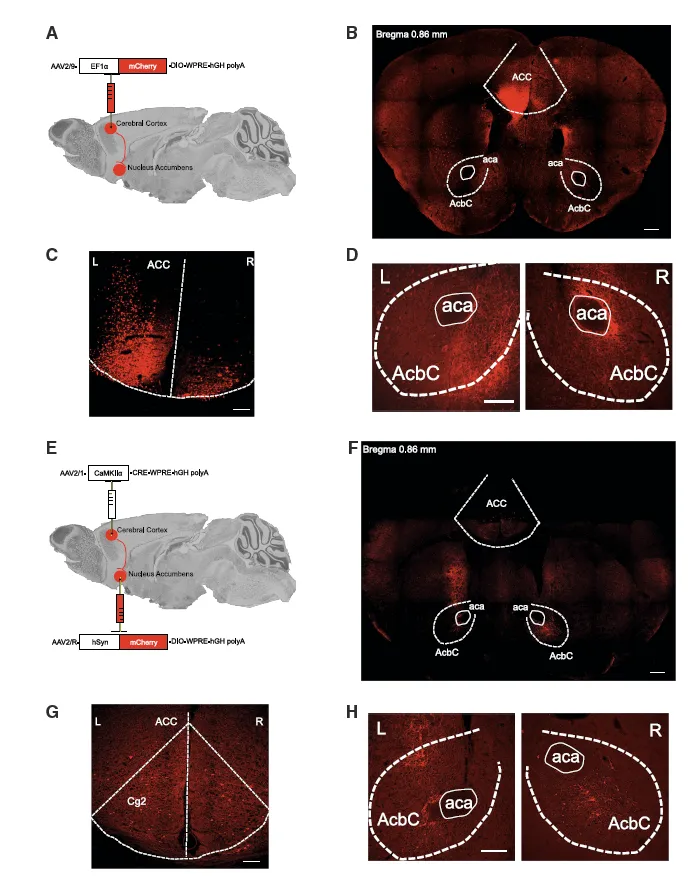
Figure 4:AcbC 神经元接收前扣带回皮层(ACC)CaMKII 阳性神经元的投射
此图通过病毒追踪技术明确了 ACC 与 AcbC 之间的神经连接。首先向 CaMKII-Cre 小鼠双侧 ACC 注射 AAV2/9-EF1α-mCherry-DIO 病毒,组织学分析发现 ACC 内出现 mCherry 阳性神经元胞体,且 AcbC 区存在 mCherry 标记的神经纤维,提示 AcbC 接收 ACC CaMKII 神经元的投射。为进一步验证直接连接,向双侧 ACC 注射 CRE 依赖的顺行跨突触病毒 AAV2/1-CaMKIIα-CRE,同时向 AcbC 注射 DIO 依赖的逆行追踪病毒 AAV2/Retro-hSyn-mCherry-DIO,结果显示 AcbC 内出现 mCherry 阳性轴突末梢和神经元胞体,且 ACC 内的 mCherry 阳性神经元主要定位于 Cg2 亚区。这些实验证实 AcbC 神经元可接收来自 ACC(尤其是 Cg2 亚区)CaMKII 阳性神经元的直接突触输入。
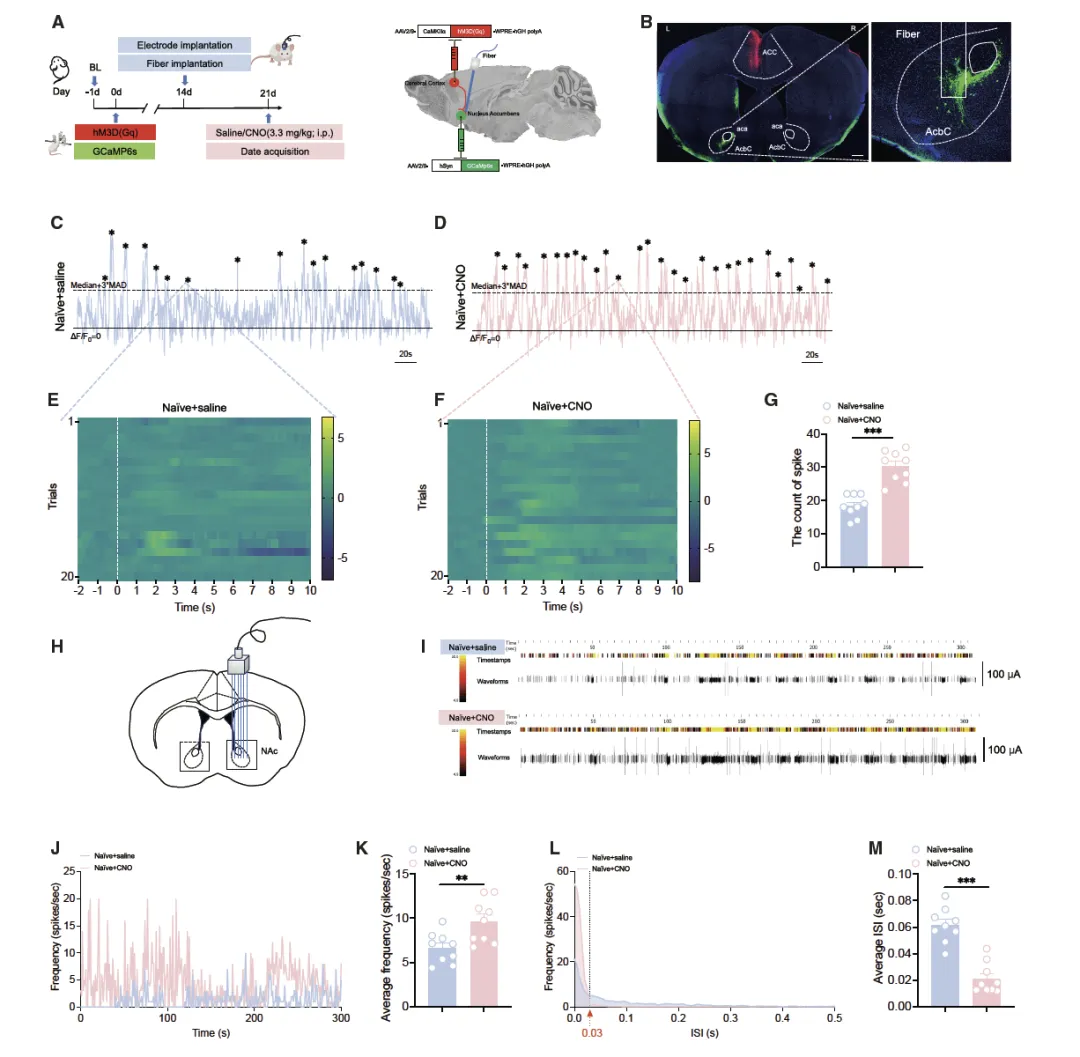
Figure 5:ACC CaMKII 阳性神经元对 AcbC 神经元起正向调控作用
该图结合化学遗传学与光纤 photometry、在体电生理技术,探究 ACC CaMKII 神经元对 AcbC 神经元活性的调控功能。向 ACC 注射 AAV2/9-CaMKIIα-hM3D (Gq)-mCherry 病毒,同时向同侧 AcbC 注射 AAV2/9-hSyn-GCaMP6s 病毒,CNO 激活 ACC CaMKII 神经元后,AcbC 神经元的钙信号峰值数量显著增加;在体电生理记录进一步显示,激活 ACC CaMKII 神经元可显著升高 AcbC 神经元的自发放电频率,且峰间间隔(ISI)显著缩短,多数 ISI 低于 0.03s。钙成像与电生理结果共同证实,ACC CaMKII 神经元通过直接的兴奋性投射,对 AcbC 神经元活性起到正向调控作用。
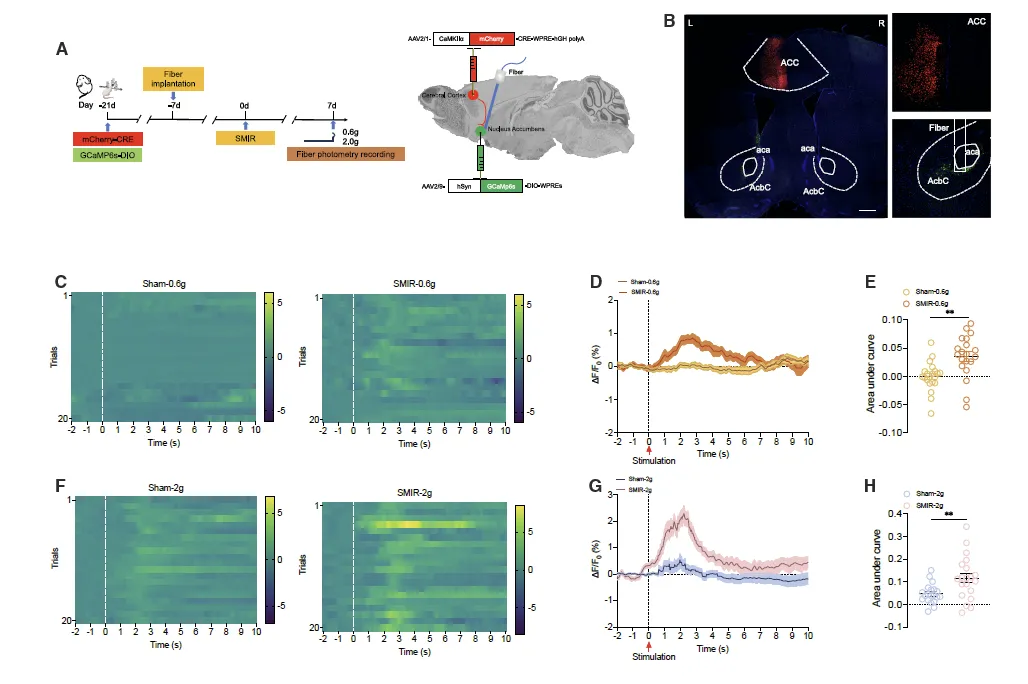
Figure 6:SMIR 手术增强 ACC CaMKII-AcbC 通路对机械刺激的反应
此图通过光纤 photometry 监测 SMIR 手术对 ACC CaMKII-AcbC 通路活性的影响。向 ACC 注射 AAV2/1-CaMKIIα-mCherry-CRE 顺行跨突触病毒,向同侧 AcbC 注射 AAV2/9-hSyn-GCaMP6s-DIO 病毒,使接收 ACC 投射的 AcbC 神经元表达 GCaMP6s,随后植入光纤记录钙信号。结果显示,0.6g von Frey 丝刺激下,SMIR 组接收 ACC 投射的 AcbC 神经元钙活性显著升高,而假手术组反应微弱;2g 刺激下两组均出现钙活性增加,但 SMIR 组的反应幅度显著大于假手术组。曲线下面积分析证实,SMIR 组在两种刺激下的钙信号强度均显著高于假手术组,表明 SMIR 手术可增强 ACC CaMKII-AcbC 通路对非伤害性和伤害性机械刺激的反应活性。
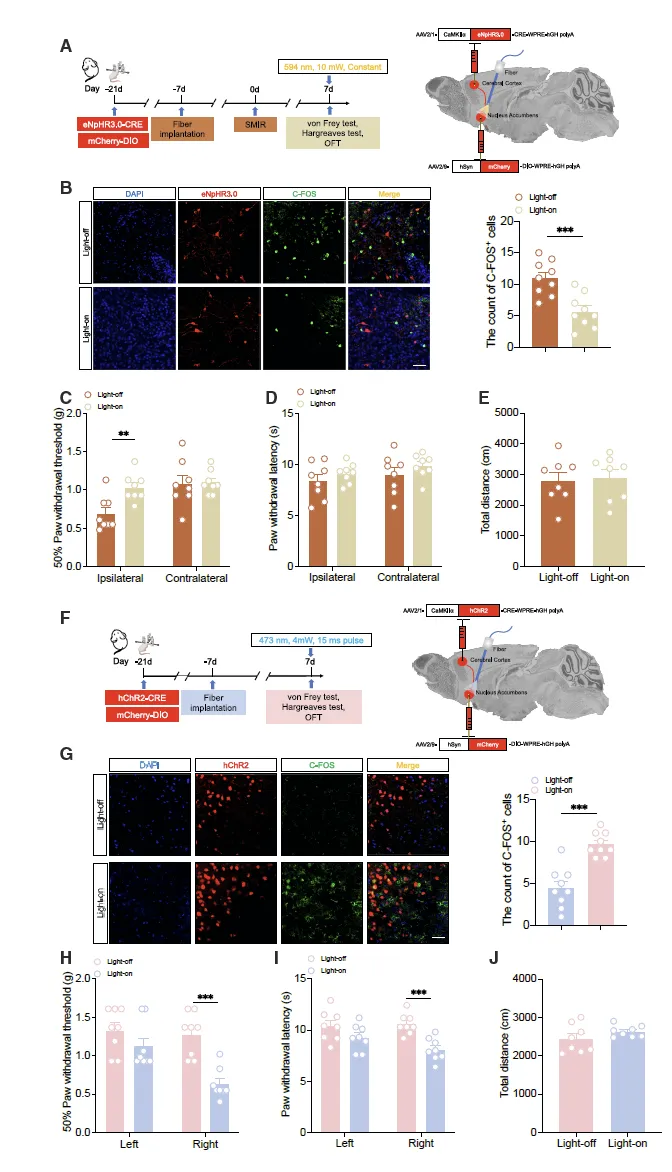 Figure 7:ACC CaMKII-AcbC 兴奋性通路双向调控疼痛
Figure 7:ACC CaMKII-AcbC 兴奋性通路双向调控疼痛
该图利用光遗传学技术明确 ACC CaMKII-AcbC 通路在疼痛调节中的作用。向 SMIR 小鼠对侧 ACC 注射 AAV2/1-CaMKIIα-eNpHR3.0-mCherry-CRE 病毒,向同侧 AcbC 注射 AAV2/9-hSyn-mCherry-DIO 病毒并植入光纤,594nm 光刺激可抑制该通路活性(表现为 C-FOS 阳性细胞减少),并特异性升高 SMIR 小鼠同侧后爪的 PWT50,缓解机械痛敏,且不影响热痛敏和运动功能。反之,向正常小鼠左侧 ACC 注射 AAV2/1-CaMKIIα-hChR2-mCherry-CRE 病毒,向同侧 AcbC 注射 AAV2/9-hSyn-mCherry-DIO 病毒,473nm 光刺激激活该通路后,正常小鼠右侧后爪的 PWT50 和 PWL 显著降低,诱导疼痛表型,且运动功能不受影响。这些结果表明 ACC CaMKII-AcbC 通路可双向调控疼痛敏感性,抑制通路能缓解 CPOP 相关机械痛敏,激活则可诱导正常小鼠出现疼痛反应。
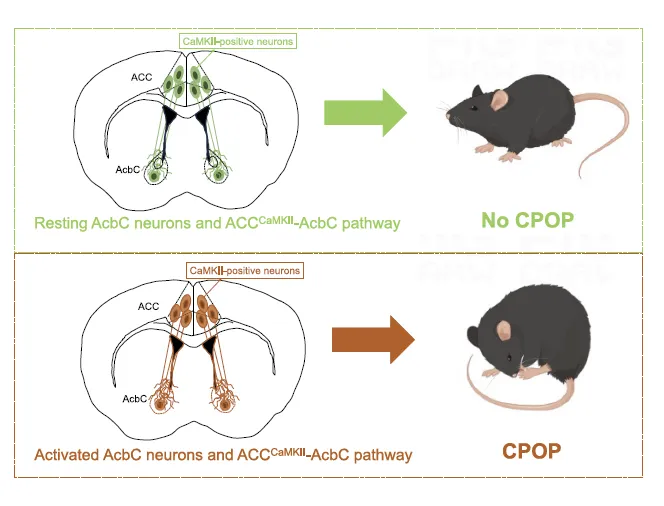 Figure 8:ACC CaMKII-AcbC 通路激活参与慢性术后痛(CPOP)的示意图
Figure 8:ACC CaMKII-AcbC 通路激活参与慢性术后痛(CPOP)的示意图
该图以示意图形式直观呈现了 ACC CaMKII-AcbC 通路在 CPOP 发生中的作用机制。在无 CPOP 状态下,AcbC 神经元和 ACC CaMKII-AcbC 通路处于静息状态,疼痛信号正常调控;而在 CPOP 状态下,SMIR 手术诱导 ACC CaMKII 神经元激活,通过兴奋性投射增强 AcbC 神经元的活性,进而引发机械痛敏等疼痛表型。该示意图清晰概括了研究核心结论:ACC CaMKII-AcbC 通路的激活是 CPOP 发生发展的关键机制,为理解 CPOP 的神经环路基础提供了直观参考。
本研究证实,伏隔核核心区(AcbC)神经元和前扣带回皮层(ACC)CaMKII 阳性神经元 - AcbC 通路在慢性术后痛(CPOP)的发生发展中起关键作用。SMIR 术后,AcbC 神经元兴奋性增强,对非伤害性和伤害性机械刺激的反应显著升高,且该神经元接收 ACC-CaMKII 阳性神经元的兴奋性投射,形成的 ACC-CaMKII-AcbC 通路术后活性增强。该通路和 AcbC 神经元可双向调控疼痛敏感性,抑制其活性能有效缓解 CPOP 小鼠的机械痛敏,激活则在正常小鼠中诱导疼痛表型。这些发现揭示了 CPOP 的神经环路机制,为术后疼痛的治疗提供了 AcbC 神经元及 ACC-CaMKII-AcbC 通路这两个潜在的特异性靶点,为开发精准靶向治疗策略奠定了基础。
局限性:仅评估了机械痛敏和热痛敏,未探究 CPOP 相关的焦虑、抑郁等情绪成分;实验仅使用雄性小鼠,未考虑性别差异对疼痛通路的影响;未明确 ACC 和 AcbC 内抑制性神经元的作用及 NAc 不同亚区的功能差异。
展望:未来需补充情绪相关行为检测,纳入雌性小鼠研究性别差异,深入分析抑制性神经元的作用及 NAc 亚区特异性机制,为临床转化提供更全面的理论支持。

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究