PNAS|郑州大学董子钢/王梅云/郭智萍等团队找到关键代谢开关,并发现它能预测化疗效果,胃癌细胞“吃草”是怎么变强抵抗化疗
- 2026-04-23 20:16:29




【期刊】Proceedings of the National Academy of Sciences of the United States of America
【影响因子】9.1
【doi】10.1073/pnas.2525213123


代谢重编程被认为是肿瘤发生发展的核心特征之一,它使肿瘤细胞能够在缺氧、营养匮乏及氧化应激等不利微环境中维持增殖与生存。近年来,氨基酸代谢作为这一过程的重要组成部分,逐渐被认为在肿瘤生长、免疫调控及治疗抵抗中发挥关键作用。其中,丝氨酸不仅参与核苷酸和脂质合成,还通过驱动谷胱甘肽(GSH)生成维持细胞氧化还原稳态,是连接代谢适应与抗氧化防御的关键枢纽。然而,丝氨酸代谢在胃癌中的具体致癌机制,以及其如何影响化疗反应,尤其是奥沙利铂敏感性,仍缺乏系统性阐释。
2026年3月25日,郑州大学董子钢、郭智萍、王梅云共同通讯在 PNAS(IF:9.1)在线发表题为“PHGDH phosphorylation mediated by WNK1 serves as a dual marker of metabolic vulnerability and responsiveness to oxaliplatin treatment”的研究,系统揭示了WNK1–PHGDH轴驱动的丝氨酸代谢重编程不仅促进肿瘤进展,同时赋予其化疗耐药能力。
研究首先通过整合代谢组学与^13C示踪的代谢通量分析发现,胃癌中丝氨酸合成通路显著激活,其核心驱动来源于限速酶PHGDH的异常上调。作为丝氨酸从头合成途径的关键节点,PHGDH的活性增强直接推动了代谢通量向丝氨酸及其下游产物的重分配。
进一步机制研究表明,WNK1可在Ser349和Ser371位点对PHGDH进行磷酸化修饰,通过抑制其泛素介导的降解,显著提升PHGDH的蛋白稳定性与酶活性。这一翻译后修饰机制揭示了PHGDH异常激活的上游调控来源,也为代谢酶功能调控提供了新的分子层面解释。
在体内功能验证中,WNK1缺失可显著降低胃部肿瘤负荷,同时伴随丝氨酸水平下降及细胞氧化还原平衡的破坏,进一步证明WNK1–PHGDH轴在肿瘤维持中的关键作用。这一结果从因果层面支持了该代谢通路的促肿瘤功能。
从代谢功能角度来看,PHGDH的磷酸化激活带来了一系列下游效应:增强的丝氨酸合成促进半胱氨酸及谷胱甘肽(GSH)生成,从而提升细胞清除活性氧(ROS)的能力,维持氧化还原稳态,并抑制氧化性细胞死亡(包括铁死亡)。这种代谢适应为肿瘤细胞在压力环境中的持续存活提供了关键支持。
值得关注的是,这一代谢重编程过程与化疗反应密切相关。临床数据分析显示,PHGDH活性升高、丝氨酸积累及GSH水平增加,与胃癌患者对奥沙利铂治疗反应不佳显著相关。这一发现提示,PHGDH不仅是代谢调控节点,更可作为预测化疗耐药的重要生物标志物。
综合来看,本研究构建了一条清晰的功能轴:WNK1介导PHGDH磷酸化→稳定并激活PHGDH→增强丝氨酸代谢→提升GSH依赖的抗氧化能力→维持氧化还原稳态并抑制细胞死亡→促进肿瘤生长与化疗耐受。这一机制不仅揭示了胃癌代谢适应的关键路径,也解释了肿瘤细胞获得“抗压生存优势”的分子基础。
更重要的是,PHGDH在该过程中同时具备“驱动因子”与“治疗脆弱性靶点”的双重属性。研究提示,通过抑制PHGDH活性或干预其磷酸化修饰,有望削弱肿瘤的抗氧化防御体系,从而提高其对奥沙利铂等化疗方案的敏感性。这为胃癌新辅助治疗策略的优化提供了明确的代谢干预方向。

Results
主要研究结果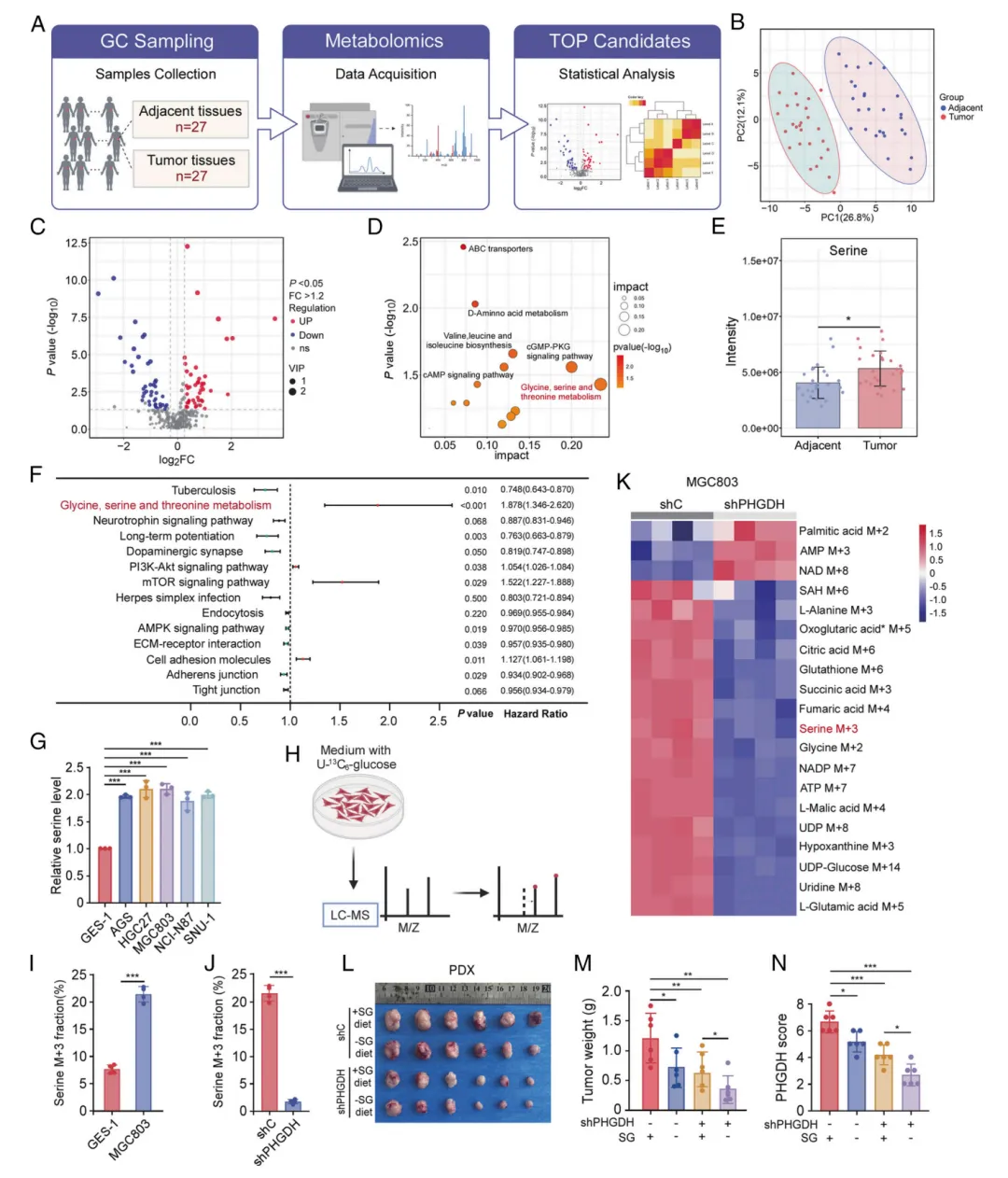
图1. 丝氨酸水平升高与 PHGDH 表达是癌症生长的必要条件。(A)人类胃癌组织及其配对邻近组织样本(n=27)的非靶向 UPLC -MS代谢组学分析流程图。(B)代谢组学数据的主成分分析。(C)人类胃癌组织相对于配对邻近正常组织的差异代谢物火山图(n=27样本,队列1)。(D)代谢物类别变化对通路的影响。(E)胃癌组织及其配对邻近正常组织中检测到的丝氨酸水平。(F) TCGA 数据库中胃癌患者(n=154)的单变量Cox回归分析显示与生存相关的通路。(G)人类胃黏膜上皮细胞(GES-1)及胃癌细胞(AGS、HGC27、MGC803、NCI-N87和SNU-1)中的丝氨酸水平。(H)细胞内U-[13C]-葡萄糖掺入丝氨酸的示意图。m/z,质荷比。(I)人类胃黏膜上皮细胞(GES-1)与胃癌细胞(MGC803)中丝氨酸13C掺入效应(n=4个生物学独立细胞样本)。(J) PHGDH 敲低(shPHGDH)与对照组(shC)相比对MGC803细胞中丝氨酸13C掺入(M+3)的影响(n=4个生物学独立细胞样本)。(K) PHGDH 敲低(shPHGDH)与对照组(shC)相比MGC803细胞中20种差异代谢物的热图(n=4个独立生物学细胞样本)。(L–N)肿瘤图像(L)、肿瘤重量(M)并基于 IHC 染色(N)呈现了 PHGDH 蛋白表达情况。
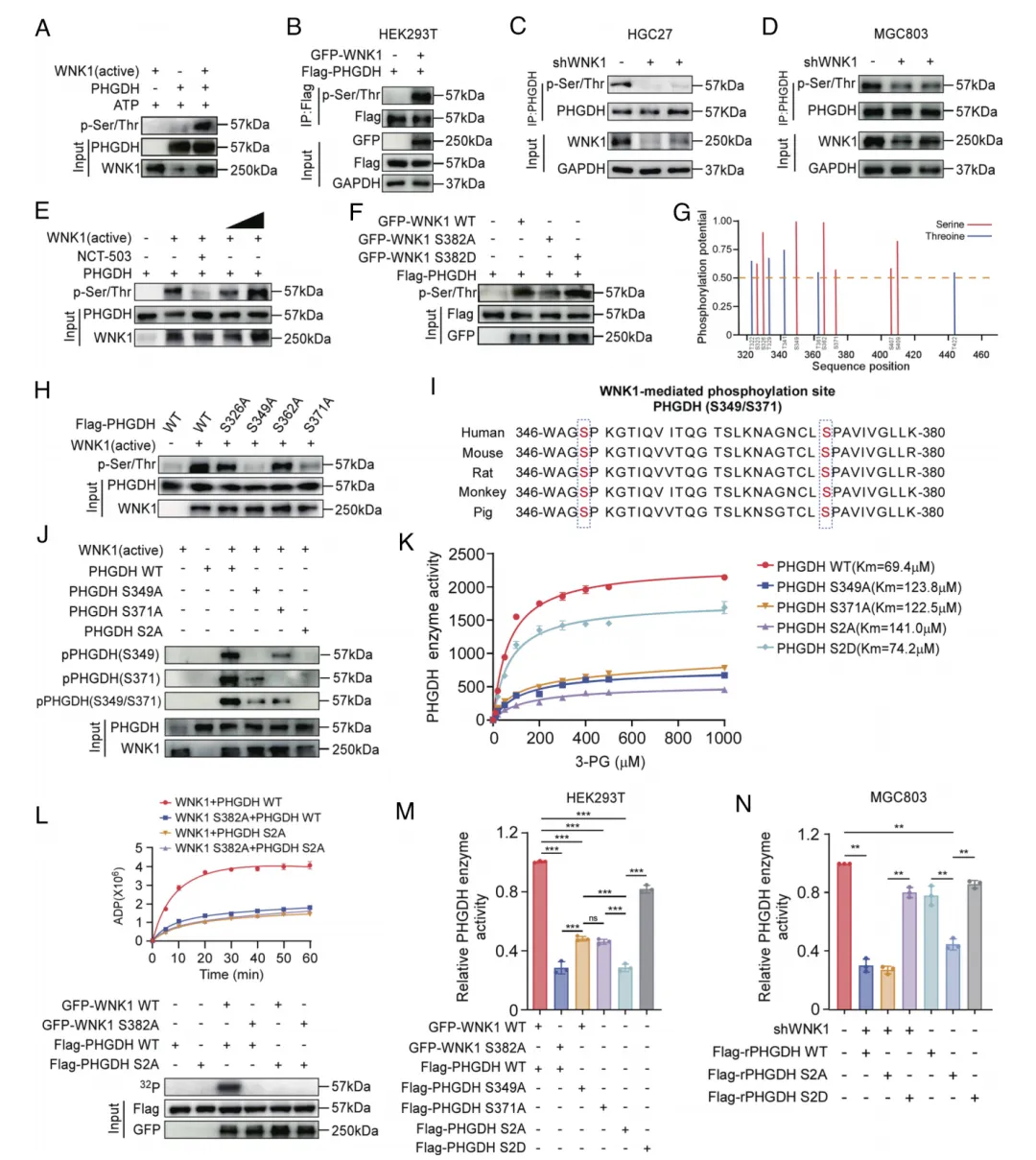
图2. WNK1通过磷酸化 PHGDH 蛋白的Ser349和Ser371位点来增强其酶活性。(A)采用泛磷酸化抗体进行蛋白质印迹分析,比较活性WNK1与失活 PHGDH 在体外激酶活性实验中的差异。(B)HEK293T细胞中共表达 GFP -WNK1与Flag- PHGDH 蛋白;Flag- PHGDH 经免疫沉淀后通过蛋白质印迹法(WB)分析磷酸化状态。(C和D)通过免疫沉淀(IP)和蛋白质印迹法分析WNK1敲低后HGC27和MGC803细胞中 PHGDH 磷酸化水平。(E)通过蛋白质印迹法分析WNK1诱导的 PHGDH 磷酸化呈剂量依赖性增加及NCT-503抑制作用。(F)采用具有激酶活性与失活突变体的WNK1进行体外激酶活性实验,并通过蛋白质印迹法验证。(G)运用NetPhos 3.0算法预测 PHGDH WNK1结合ASB结构域(残基323-455)中的磷酸化位点。(H)通过蛋白质印迹法分析WNK1与 PHGDH 突变体(S326A、S349A、S362A、S371A)的体外激酶活性实验。(I)不同物种间 PHGDH S349与S371氨基酸残基的序列比对。(J)使用磷酸化特异性抗体检测 PHGDH 野生型、单点突变体(S349A、S371A)及双突变体(S2A)与活性WNK1共孵育后的蛋白质印迹结果。(K)以3-PG为底物评估 PHGDH 野生型及突变体(S349A、S371A、S2A、S2D)的酶动力学特性。(L)在HEK293T细胞中进行[32P]-ATP标记实验,检测 PHGDH 野生型与S2A突变体与WNK1野生型或S382A突变体共表达时的ADP水平变化。(M和N)在WNK1过表达或敲低条件下,转染 PHGDH 野生型、S349A、S371A、S2A或S2D的HEK293T(M)与MGC803(N)细胞中进行 PHGDH 酶活性测定。
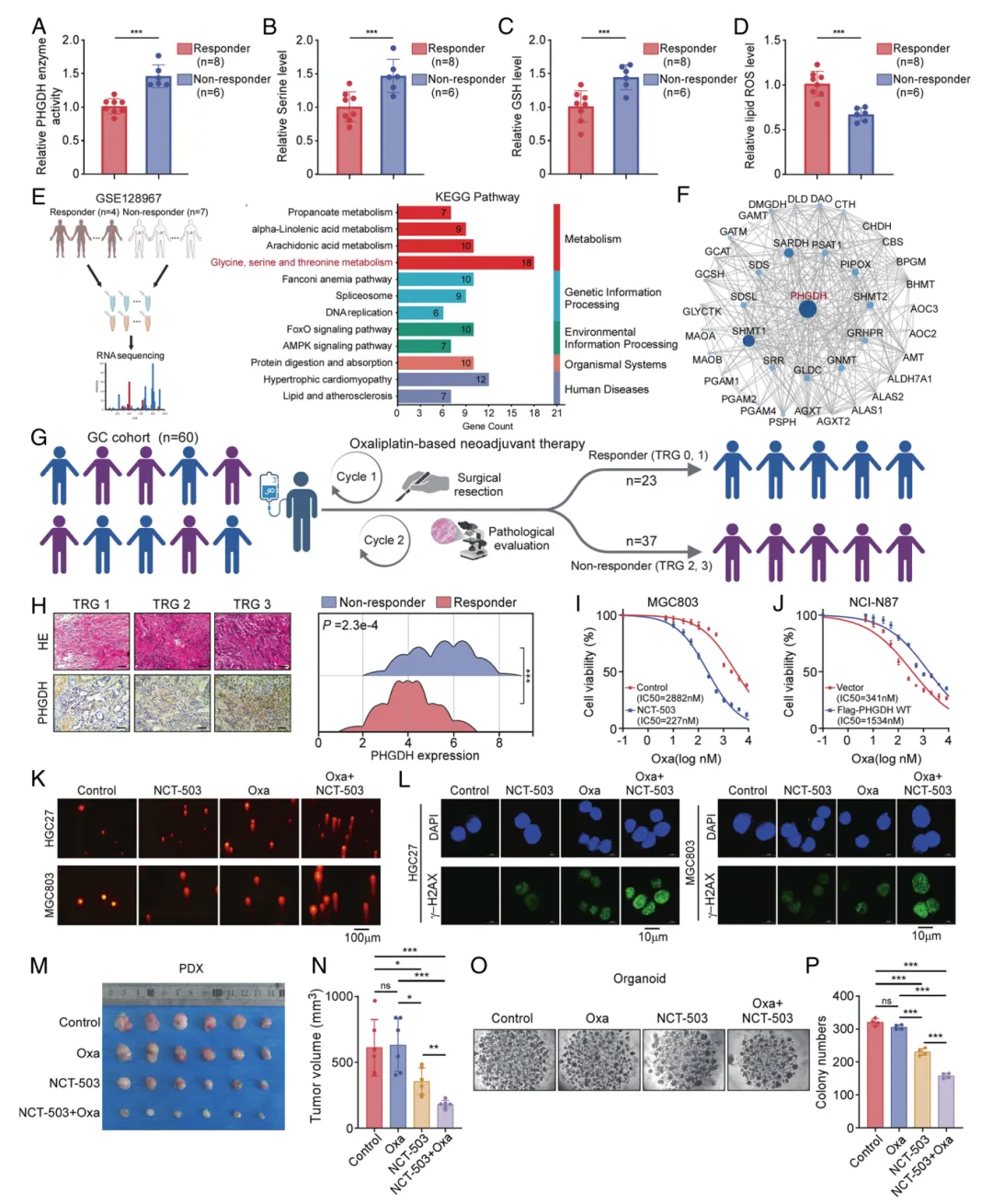
图3. PHGDH 表达与丝氨酸代谢与胃癌奥沙利铂耐药性相关性分析。(A–D) 通过酶活性测定或代谢物定量法检测奥沙利铂应答组(n=8)与无应答组(n=6)肿瘤组织中 PHGDH 酶活性相对水平(A)、细胞内丝氨酸(B)、 GSH (C)及脂质活性氧(D)的变化。(E) 基于GSE128967数据集(应答组n=4;无应答组n=7)进行应答组与无应答组差异基因表达的 KEGG 通路富集分析。(F) 以 PHGDH 为核心的蛋白质相互作用网络图(采用STRING数据库构建),显示甘氨酸、丝氨酸及苏氨酸代谢相关酶群。(G) 接受奥沙利铂新辅助化疗临床队列示意图(n=60例样本,队列2)。病理评估将患者分为应答组(TRG 0-1,n=23)与无应答组(TRG 2-3,n=37)。(H) 不同 TRG 评分患者肿瘤样本的H&E染色与 PHGDH IHC 染色代表性结果,及应答组与无应答组 PHGDH 表达分布对比。(I-J) MGC803(I)与NCI-N87(J)细胞经奥沙利铂处理72小时后的剂量-效应曲线,分别显示 PHGDH 抑制剂(NCT-503)与 PHGDH 过表达条件下的实验结果。细胞活力通过 MTT 法进行评估。(K) 显示经奥沙利铂、NCT-503或其联合治疗后HGC27和MGC803细胞DNA损伤加剧的彗星实验结果。(L) 经奥沙利铂、NCT-503或其联合处理细胞中 γ -H2AX(绿色)与 DAPI(蓝色)的免疫荧光染色结果。(M) 各治疗组切除 PDX 肿瘤的代表性图像。(N) 各组肿瘤体积定量分析(每组n=6只小鼠)。(O) 不同处理条件下类器官培养的代表性图像。各组别分别展示对照组、奥沙利铂组(Oxa)、NCT-503组及奥沙利铂+NCT-503联合组的类器官形态学特征。(P) 类器官培养物中集落数量的定量分析。
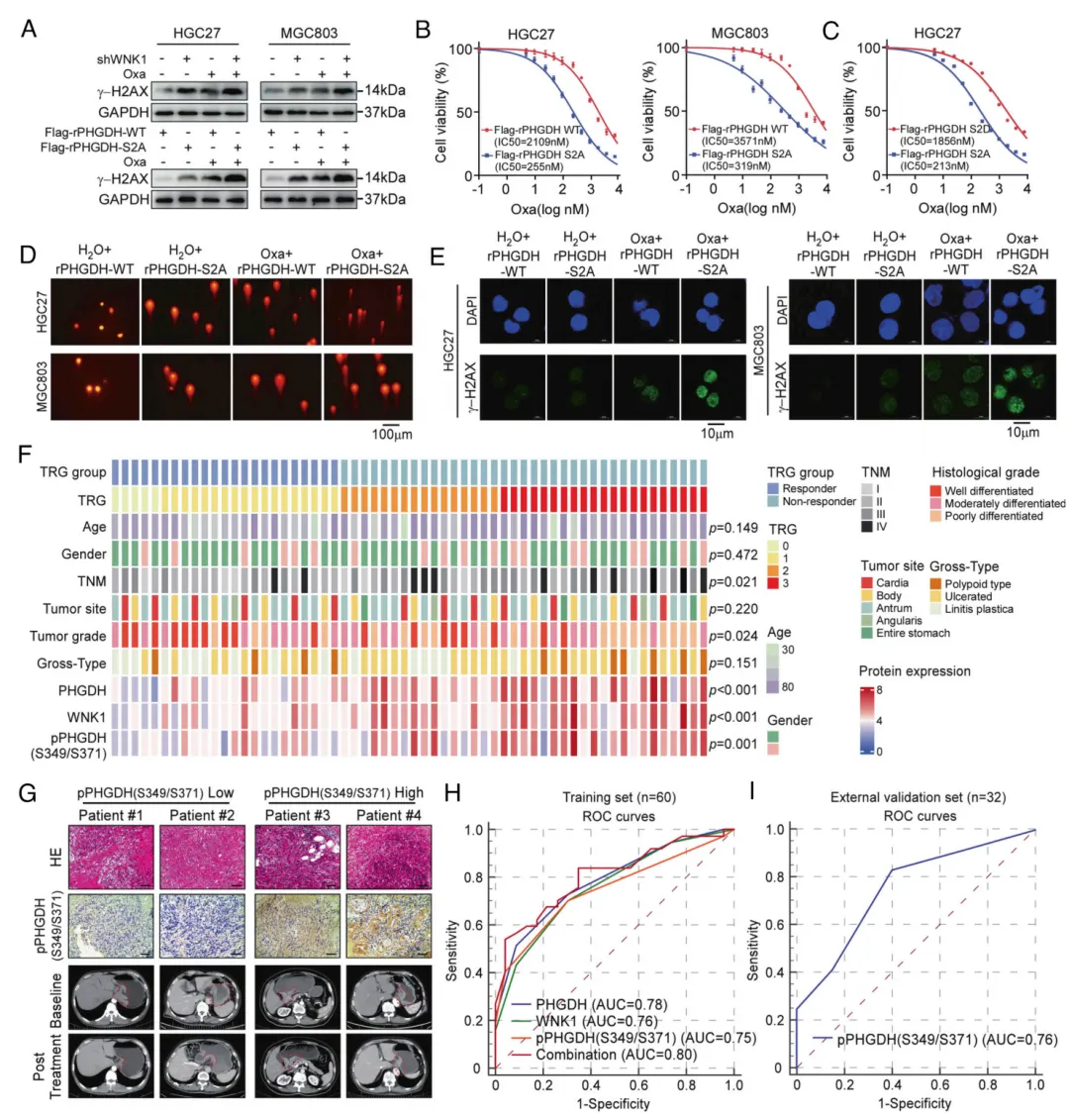
图4. Ser349/Ser371位点 PHGDH 磷酸化调控DNA损伤反应及奥沙利铂敏感性,可作为胃癌潜在预测生物标志物。(A) 指定条件下HGC27与MGC803细胞中 γ -H2AX水平的蛋白质印迹分析。(上)shWNK1细胞经奥沙利铂处理。(下)用rPHGDH-WT或磷酸化缺陷突变体rPHGDH-S2A重建的 PHGDH 敲除细胞。(B和C) 表达rPHGDH-WT或rPHGDH-S2A的HGC27与MGC803(B)细胞经奥沙利铂处理72小时后的剂量-反应曲线。细胞活力通过 MTT 法测定。(D) 显示过氧化氢或奥沙利铂(Oxa)处理后,用rPHGDH-WT或rPHGDH-S2A重建的HGC27与MGC803细胞中DNA损伤的彗星实验。(E) (D)组处理细胞中 γ -H2AX焦点(绿色)的免疫荧光检测;细胞核用 DAPI(蓝色)复染。(F) 热图显示按肿瘤消退分级(TRG 组)分层患者的临床、病理及蛋白表达特征。 PHGDH 、WNK1及pPHGDH(S349/S371)表达水平采用颜色编码。(G) 低 PHGDH 磷酸化水平与高 PHGDH 磷酸化水平患者pPHGDH(S349/S371)的代表性H&E染色、 IHC 染色及治疗前后CT图像对比。(H) ROC曲线显示训练集(n=60)中 PHGDH 、WNK1及pPHGDH(S349/S371)对奥沙利铂反应的预测价值。(I) ROC曲线显示外部验证集(n=32)中pPHGDH(S349/S371)对奥沙利铂反应的预测价值。
以上内容均来自期刊官网、Pubmed平台,本公众号仅做整理分享。
推荐阅读:
Nature Cancer | 西湖大学高晓飞/浙江省人民医院杨柳/浙江大学梁廷波/冯宇雄团队等开发首款红细胞抗体偶联药物,安全有效治疗晚期癌症
Adv Sci|复旦大学附属眼耳鼻喉科医院陈健/吴海涛团队揭示人源化和电荷优化的CSPG4特异性CAR-T细胞对头颈部鳞状细胞癌显示出增强的疗效
Gut|复旦大学附属中山医院周俭院士和杨欣荣教授团队发表CD177+中性粒细胞能够驱动肝再生最新研究结果

文献PDF请识别下方二维码直接下载
PHGDH phosphorylation mediated by WNK1 serves as a dual marker of metabolic vulnerability and responsiveness to oxaliplatin treatment.pdf

近期如有需要发表SCI可以咨询,留下您的研究方向,可辅导!!
