郑州大学第三附属医院 | 栗河舟教授团队:胎儿部分性胼胝体缺失超声特征及相关畸形分析
- 2026-05-14 01:38:22



作者
靳留杰1,周昌荣1,王新霞1,王蒙蒙1,栗河舟1*,陆林2,刘灵3
本文引用格式
[1]靳留杰,周昌荣,王新霞,等.胎儿部分性胼胝体缺失超声特征及相关畸形分析[J].中国医学影像学杂志,2026,34(3):319-323 .DOI:10.3969/j.issn.1005-5185.2026.03.012.
目的
总结胎儿部分性胼胝体缺失的超声特征及合并相关畸形,并分析其与遗传学异常的关系。
资料与方法
回顾性纳入2018年8月—2023年11月在郑州大学第三附属医院诊断的51例部分性胼胝体缺失胎儿,分析其超声特征、合并相关畸形以及遗传学结果。
结果
颅脑横切面显示透明隔腔异常41例、侧脑室扩张21例、第三脑室扩张上抬15例、大脑纵裂池增宽21例。单纯性部分性胼胝体缺失17例,复杂性部分性胼胝体缺失34例;34例复杂性病例中,合并颅内畸形21例、颅外畸形9例、颅内及颅外畸形4例;颅内畸形中最常见的是大脑皮质发育不良,共7例,颅外畸形最常见的是心内结构异常,共8例。27例行遗传学检测,11例存在结果异常。19例行染色体微阵列或拷贝数变异测序检查,其中14例为阴性,5例发现致病性(3例致病性拷贝数缺失,2例致病性片段重复);8例行全外显子组检测分析,2例为阴性,5例检测出新发变异致病基因,1例意义不明的半合子变异位点。
结论
胎儿部分性胼胝体缺失最重要的超声征象为透明隔腔异常,易合并颅内、颅外畸形及遗传学异常,产前超声可为临床诊断及鉴别诊断提供参考。

胼胝体是颅内最大的白质结构,包含2亿个轴突,作为人类脑神经系统最主要的连接通路,主要负责协调、传递和整合两侧大脑半球间信息。Salomon等[1]研究显示胼胝体于12~13周开始发育,由前向后生长,从膝部开始到压部,最后形成嘴部。由于胼胝体在胚胎第18周发育形成,因此18周前通常不能诊断胎儿胼胝体缺如[2]。在胼胝体发育过程中,受遗传因素(染色体异常或基因突变)和外源性因素(出血、感染)的影响,会造成胼胝体发育不全,是最常见的先天性大脑畸形之一,其形态学分为完全性胼胝体缺失、部分性胼胝体缺失(partial agenesis of corpus callosum,PACC)以及胼胝体发育不良[3];根据是否合并其他畸形,分为单纯性和复杂性[4]。PACC胎儿预后与完全性胼胝体缺失胎儿预后相似,但产前超声征象不如后者典型,可能会导致PACC漏诊或误诊[5]。产前超声诊断胼胝体缺失是通过二维或三维成像在正中矢状切面或冠状切面直接观察有无胼胝体[6],但颅脑矢状切面及冠状切面对胎儿体位及医师操作手法要求较高,难以作为常规筛查切面[7],因此可以通过观察颅脑横切面部分超声间接征象,以提高对PACC的筛查率。本研究拟探讨产前诊断为PACC胎儿的超声特征及合并相关畸形,并分析其与遗传学异常的关系,为准确产前咨询和临床处理提供依据。
1.1 研究对象
回顾性纳入2018年8月—2023年11月郑州大学第三附属医院超声科疑诊为PACC的51例胎儿。纳入标准:①月经规律,末次月经明确。②产前超声提示PACC,并经MRI证实。排除完全性胼胝体缺失。孕妇年龄19~37岁,平均(29.22±4.51)岁;孕周21+1~34+1周,平均(25.76±2.00)周。本研究经郑州大学第三附属医院伦理委员会审核通过(2024-128-01),所有孕妇均签署知情同意书。
1.2 仪器与方法
使用GE Voluson E8 Expert、Voluson E10、Samsung W10超声诊断仪,C1-5、RAB4-8D、RAB2-5D、CV1~8 A探头,探头频率分别为1~5 MHz、4~8 MHz、2~5 MHz、1~8 MHz。检查时孕妇取仰卧位,按照产科系统检查规范[8]对胎儿进行筛查。可疑胼胝体发育异常时,对胎儿进行神经系统超声检查[9],从颅脑横切面[其中,侧脑室扩张分为轻度(10~12 mm)、中度(13~15 mm)和重度(>15 mm)[10]、冠状切面和正中矢状切面观察胼胝体形态。根据合并颅内畸形类型分为脑皮质发育异常、脑中线异常、后颅窝结构异常、其他异常。
采用Siemens skyra 3.0T MR成像仪,8通道相控阵表面线圈,孕妇取仰卧位,必要时取侧卧位,头先进,先行中下腹、盆腔定位扫描,然后对胎儿头部进行轴位、冠状位及矢状位3个方位扫描,T2WI采用半傅立叶单激励快速自旋回波序列,Haete:TR 720 ms,TE 65 ms,翻转角120°。
1.3 遗传学检查
超声科疑诊为PACC并经产前MRI证实的胎儿,孕妇行染色体微阵列或拷贝数变异测序及全外显子测序检测。
2.1 PACC产前超声间接声像图特征
颅脑横切面(图1、2):①透明隔腔(cavum septum pellucidum,CSP)异常41例,其中CSP狭小8例,CSP形态异常18例,CSP缺失15例。②侧脑室扩张21例,单侧侧脑室扩张6例(左侧侧脑室扩张2例,右侧侧脑室扩张4例),双侧侧脑室扩张15例;轻度8例、中度10例、重度3例。③第三脑室扩张上抬15例。④大脑纵裂池增宽21例。
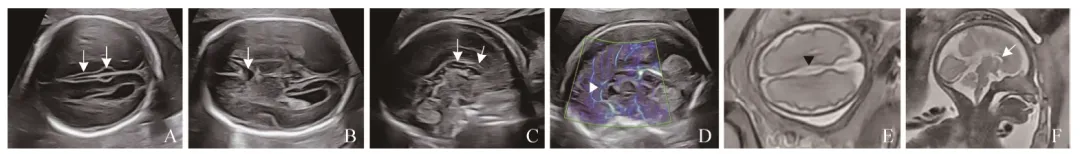
图1 女,35岁,孕周25周,胎儿PACC。A.大脑纵裂池增宽呈三线征(箭);B. CSP形态异常,前后径与左右径比值约0.66(<1.5)(箭);C.二维超声颅脑正中矢状切面胼胝体部分显示,体部后部分及压部未显示(箭);D.颅脑正中矢状切面胼周动脉走行短(箭头);E. MRI横断面显示大脑纵裂池增宽(箭头);F. MRI矢状面显示胎儿胼胝体部分显示(箭)。PACC为部分性胼胝体缺失,CSP为透明隔腔
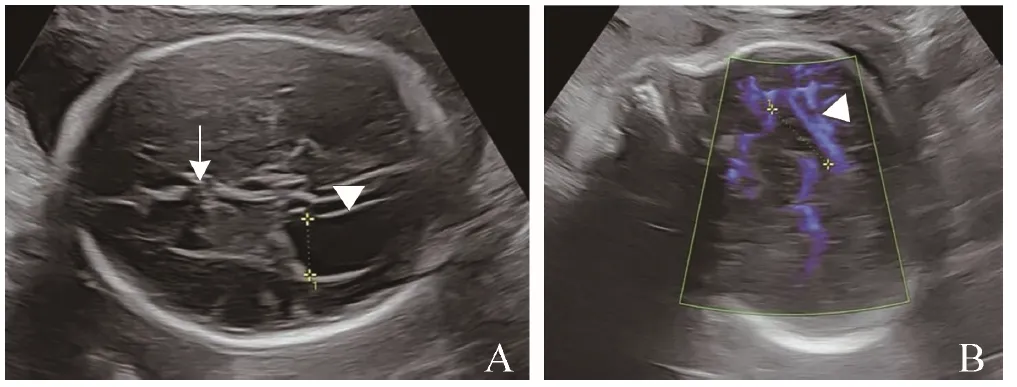
图2 女,31岁,孕周29+4周,胎儿PACC。A. CSP缺失(箭),左侧侧脑室扩张,宽约13.4 mm(箭头);B.颅脑正中矢状切面胼胝体部分显示,体部后部分及压部未显示,胼周动脉走行短(箭头)。PACC为部分性胼胝体缺失,CSP为透明隔腔
51例中,4例存在上述全部4种间接征象;20例存在2种间接征象,CSP异常+大脑纵裂池增宽10例,CSP异常+侧脑室扩张6例,CSP异常+第三脑室扩张上抬4例;10例存在3种间接征象,CSP异常+第三脑室扩张上抬+大脑纵裂池增宽3例,CSP异常+第三脑室扩张上抬+侧脑室扩张4例,CSP异常+侧脑室扩张+大脑纵裂池增宽3例;17例仅存在1种间接征象,CSP异常9例(CSP狭小2例,CSP形态异常5例,CSP缺失2例),侧脑室扩张6例(双侧侧脑室扩张4例、右侧侧脑室扩张1例、左侧侧脑室扩张1例),第三脑室扩张上抬1例,大脑纵裂池增宽1例。
2.2 PACC产前超声直接声像图特征
颅脑正中矢状切面:以胼胝体后半部分缺失最常见,多为体部后部分和压部缺失,或仅有压部缺失。
2.3 PACC合并其他畸形特征
51例中,单纯性PACC 17例;复杂性PACC 34例,包括合并颅内畸形21例、颅外畸形9例、颅内及颅外畸形4例。本组颅内畸形以脑皮质发育异常较常见,共12例,包括大脑皮质发育不良7例、小头畸形4例、脑裂畸形1例。脑中线异常6例,包括蛛网膜囊肿4例、脑中线脂肪瘤2例。后颅窝结构异常8例,包括小脑蚓部发育不良3例、Dandy-walker畸形2例、Black囊肿1例、后颅窝池增宽1例、Joubert综合征1例。其他异常6例,包括脉络从囊肿2例、脑室出血2例、脑穿通畸形2例。颅外畸形主要包括心内结构异常8例,泌尿系统发育异常5例,四肢发育异常4例,其他发育异常13例。
2.4 PACC产前遗传学检测
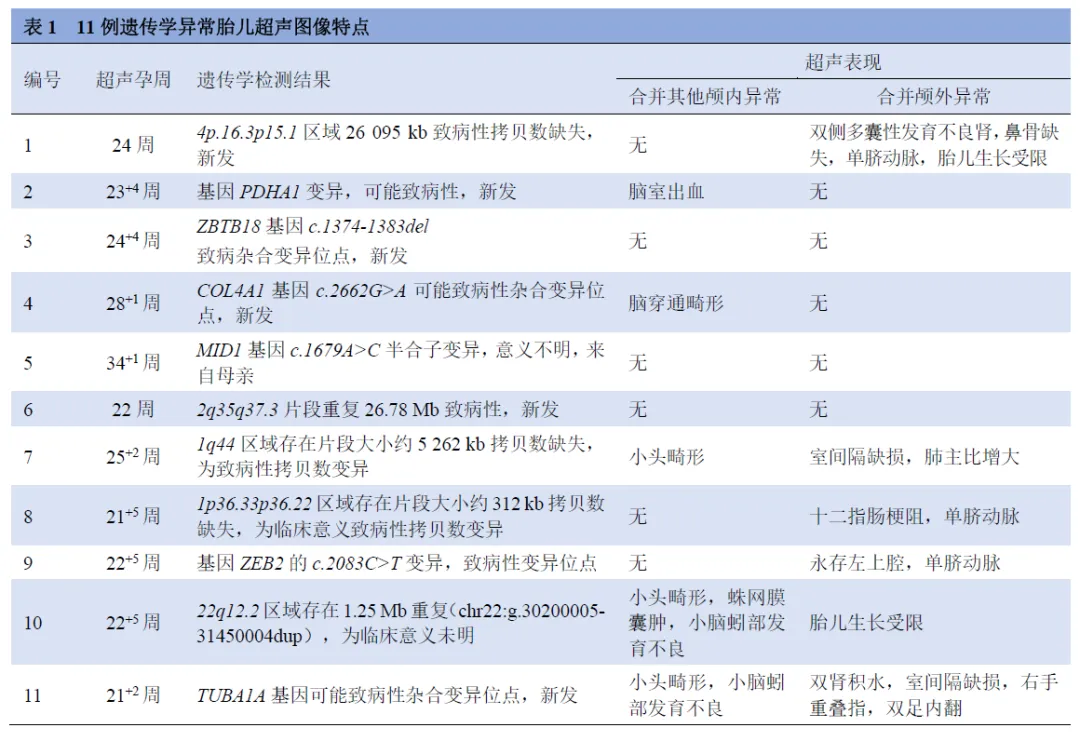
27例行遗传学检测,11例结果异常。其中19例行染色体微阵列或拷贝数变异测序检查,14例为阴性,5例发现致病性(单纯性1例,复杂性4例):3例染色体部分片段存在拷贝数缺失,2例存在染色体片段重复;8例行全外显子组检测分析,2例为阴性,5例检测出新发变异致病基因,1例意义不明的半合子变异位点,其中单纯性2例,复杂性4例。11例遗传学异常胎儿超声图像特点见表1。
本研究中,PACC胎儿颅脑横切面显示CSP异常、侧脑室扩张、第三脑室扩张上抬、大脑纵裂池增宽,以CSP形态异常最常见。本研究显示PACC胎儿易合并颅内结构畸形,并且复杂性PACC更易合并遗传学异常。
3.1 PACC的产前超声特征
CSP是位于两侧透明隔小叶中间的液体腔隙,起源于胚胎前联合板[11]。CSP与胼胝体有共同的胚胎起源,CSP异常提示胼胝体及其他结构可能存在异常;侧脑室中央部是从室间孔至胼胝体压部之间的部分,又称侧脑室体部(顶部),当胼胝体发育异常时,侧脑室及第三脑室形态会发生改变[12];胼胝体位于大脑纵裂底部,其发育异常,大脑纵裂池可能会呈梭形扩张。通常CSP宽度2~9 mm,<2 mm考虑CSP狭小;未见CSP显示考虑缺失;CSP前后径/左右径<1.5考虑形态异常[13]。本研究PACC间接征象中,以CSP异常最常见,主要表现为CSP狭小、缺失及形态异常,其中以CSP形态异常最常见,与Zhao等[14]报道一致。曾晴等[15]研究发现,在胼胝体异常间接征象中不到1/4病例会出现所有间接征象,本研究PACC胎儿中4例存在所有间接征象,17例仅有1种间接征象。de Koning等[16]报道中枢神经系统胚胎发育在产前存在一些难以解释的变异,使得某些神经系统畸形难以通过产前超声检测。胼胝体在神经系统中发育较晚,其发育始于胚胎阶段,并且在出生后漫长时间内持续发育,因此胼胝体的发育比其他结构需要更长时间[17],这使产前对胼胝体异常的诊断带来很大困难。而颅脑横切面是常规筛查切面,产前超声筛查更容易发现CSP、侧脑室、第三脑室、大脑纵裂池等结构异常,因此当发现以上任何1种间接征象时,应提高警惕,扫查颅脑正中矢状切面观察胼胝体发育情况,从而降低胼胝体缺失的漏诊率。
3.2 PACC合并其他畸形特征
单纯性PACC 17例,复杂性34例。合并颅内畸形21例、颅外畸形9例、颅内及颅外畸形4例。本研究中,PACC合并颅内畸形,以脑皮质发育异常较多见,与Glatter等[18]报道一致。脑皮质发育异常是胚胎期大脑皮质正常发育过程受到干扰,导致多种不同种类皮质发育障碍的一组疾病,包括小头畸形、大头畸形、无脑回、巨脑回、室周灰质异位、脑裂畸形、结节性硬化症等。本研究中脑皮质发育异常类型包括小头畸形、脑裂畸形、脑回、脑沟异常等。本研究颅外畸形常见的是心内结构异常和泌尿系统发育异常,与Monteagudo等[19]报道一致。产前筛查发现胼胝体发育异常时,应仔细筛查颅内及颅外结构,排除相关畸形,避免漏诊其他结构异常影响其预后评估。
3.3 PACC遗传学结果特征分析
随着遗传学检测技术提高,越来越多的研究显示,胎儿胼胝体缺失与染色体数目或结构异常、染色体微缺失或微重复以及基因突变等有关[20]。Mellis等[21]报道当羊水穿刺显示染色体微阵列或拷贝数变异测序检测正常时,进一步行全外显子测序检测可能会提高基因异常的诊断率。本研究11例遗传学异常胎儿中,5例在拷贝数变异测序检测时未见异常,进一步行全外显子测序检测,均发现致病基因;3例行全外显子测序检测:2例发现致病基因及1例意义不明的半合子变异;3例行拷贝数变异测序或染色体微阵列检测:2例拷贝数缺失,1例染色体片段重复。本研究中,无论是单纯性PACC或复杂性PACC,均可能合并遗传学异常,但以复杂性PACC相对常见,由此推测复杂性PACC胎儿染色体或基因异常的风险更高。通过染色体微阵列、拷贝数变异测序和全外显子测序等遗传学检测方法可能会增加病例中潜在病因的检出。
3.4 本研究的局限性
本研究未随访妊娠结局,无法评估新生儿神经发育结果,未来需要扩充临床研究样本,同时随访PACC胎儿妊娠结局等相关情况。
胎儿PACC最重要的超声征象为CSP异常,易合并颅内、颅外畸形及遗传学异常,产前超声可为临床诊断及鉴别诊断提供参考。
利益冲突 所有作者均声明不存在利益冲突
[1]Salomon LJ, Paladini D. Fetal corpus callosal anomalies: from disease of classification to classification of disease[J]. Ultrasound Obstet Gynecol, 2024, 64(2): 151-154. DOI: 10.1002/uog.27564.
[2]Héron D, Gerasimenko A, Frugère L, et al. A large cohort study of prenatal exome sequencing redefines diagnosis in fetal corpus callosum anomalies[J]. Brain, 2025, 148(12): 4253-4258. DOI: 10.1093/brain/awaf311.
[3]Sun H, Li K, Wang L, et al. Fetal agenesis of the corpus callosum: clinical and genetic analysis in a series of 40 patients[J]. Eur J Obstet Gynecol Reprod Biol, 2024, 298: 146-152. DOI: 10.1016/j.ejogrb.2024.05.005.
[4]Min A, Zou L. Application of prenatal ultrasonography and magnetic resonance imaging on fetal agenesis of corpus callosum[J]. Ginekol Pol, 2020, 91(3): 132-136. DOI: 10.5603/GP.2020.0029.
[5]Shwe WH, Schlatterer SD, Williams J, et al. Outcome of agenesis of the corpus callosum diagnosed by fetal MRI[J]. Pediatr Neurol, 2022, 135: 44-51. DOI: 10.1016/j. pediatrneurol.2022.07.007.
[6]Zhou C, Li H, Han R, et al. Partial agenesis of the corpus callosum: prenatal ultrasound characteristics, associations, and outcome[J]. Acta Obstet Gynecol Scand, 2025, 104(7): 1304-1317. DOI: 10.1111/aogs.15121.
[7]尹春林, 肖菊花, 郭梦兰, 等. 胎儿胼枕径筛查部分型胼胝体发育不全[J]. 中国医学影像学杂志, 2025, 33(4): 403-406. DOI: 10.3969/j.issn.1005-5185.2025.04.012.
[8]中华医学会超声医学分会妇产超声学组, 国家卫生健康委妇幼司全国产前诊断专家组医学影像组. 超声产前筛查指南[J]. 中华超声影像学杂志, 2022, 31(1): 1-12. DOI: 10.3760/cma.j.cn131148-20211110-00821.
[9]Paladini D, Malinger G, Birnbaum R, et al. ISUOG practice guidelines (updated): sonographic examination of the fetal central nervous system. Part 2: performance of targeted neurosonography[J]. Ultrasound Obstet Gynecol, 2021, 57(4): 661-671. DOI: 10.1002/uog.23616.
[10]Fox NS, Monteagudo A, Kuller JA, et al. Mild fetal ventriculomegaly: diagnosis, evaluation, and management[J]. Am J Obstet Gynecol, 2018, 219(1): B2-B9. DOI: 10.1016/ j.ajog.2018.04.039.
[11]李洁, 王晨静, 李涵, 等. 产前超声提示孤立性透明隔腔宽度异常的临床意义[J]. 中国医学影像学杂志, 2021, 29(7): 726-729. DOI: 10.3969/j.issn.1005-5185.2021.07.017.
[12]冯芳芳, 栗河舟. 产前超声间接征象在部分型胼胝体发育不全诊断中的价值[J]. 中国临床医学影像杂志, 2022, 33(6): 425-429. DOI: 10.12117/jccmi.2022.06.010.
[13]中华医学会超声医学分会妇产超声学组. 胎儿透明隔腔超声检查专家共识[J]. 中华超声影像学杂志, 2021, 30(1): 1-4. DOI: 10.3760/cma.j.cn131148- 20201012-00803.
[14]Zhao D, Wang B, Cai A. Utility of indirect sonographic signs (including cavum septum pellucidum ratio) in midgestational screening for partial agenesis of corpus callosum[J]. J Clin Ultrasound, 2019, 47(7): 394-398. DOI: 10.1002/jcu.22722.
[15]曾晴, 文华轩, 袁鹰, 等. 二维横切面新方法对胎儿胼胝体结构异常的诊断价值[J]. 中华医学超声杂志(电子版), 2022, 19(9): 899-907. DOI: 10.3877/cma.j.issn.1672-6448. 2022.09.006.
[16]de Koning MA, Hoffer MJV, Nibbeling EAR, et al. Prenatal exome sequencing: a useful tool for the fetal neurologist[J]. Clin Genet, 2022, 101(1): 65-77. DOI: 10.1111/cge.14070.
[17]De León Reyes NS, Bragg-Gonzalo L, Nieto M. Development and plasticity of the corpus callosum[J]. Development, 2020, 147(18): dev189738. DOI: 10.1242/dev.189738.
[18]Glatter S, Kasprian G, Bettelheim D, et al. Beyond isolated and associated: a novel fetal MR imaging-based scoring system helps in the prenatal prognostication of callosal agenesis[J]. Am J Neuroradiol, 2021, 42(4): 782-786. DOI: 10.3174/ajnr.A7064.
[19]Monteagudo A, Kuller JA, Craigo S, et al. SMFM fetal anomalies consult series #3: intracranial anomalies[J]. Am J Obstet Gynecol, 2020, 223(6): B2-B50. DOI: 10.1016/ j.ajog.2020.08.041.
[20]佘芹, 甄理, 符芳, 等. 孤立性胼胝体发育异常胎儿的系列遗传学诊断研究[J]. 中华妇产科杂志, 2022, 57(9): 671-677. DOI: 10.3760/cma.j.cn112141-20220428-00281.
[21]Mellis R, Oprych K, Scotchman E, et al. Diagnostic yield of exome sequencing for prenatal diagnosis of fetal structural anomalies: a systematic review and meta-analysis[J]. Prenat Diagn, 2022, 42(6): 662-685. DOI: 10.1002/pd.6115.
向下滑动查看更多参考文献
本文为《中国医学影像学杂志》原创文章。若您需要转载本文,请通过公众号联系本刊编辑部获得授权,并在醒目位置注明“原文刊发于《中国医学影像学杂志》,卷(期):起止页码”,期待与您的合作!


杂志微信公众号 | zgyxyxx
本刊官网 | http://zyyz.cbpt.cnki.net
编辑部电话 | 010-64012981转5200;15110102619

