伤口早好了,为啥还疼?郑州大学张伟/李治松团队揭示慢性术后疼痛的新中枢机制
- 2026-03-27 23:27:43



很多人以为疼痛只是“伤口在痛”,但其实慢性术后疼痛(比如手术几个月后还持续疼痛)更多是大脑“记住了痛”。
基于此,郑州大学第一附属医院麻醉科张伟教授&郑州大学第二附属医院麻醉与围术期医学部李治松教授研究团队在《iScience》杂志发表了“The neurons in NAc core receiving ACC excitatory afferents contribute to chronic postoperative pain”揭示了接收前扣带皮层(ACC)兴奋性传入的伏隔核(NAc)核心神经元参与慢性术后疼痛。

在此,作者发现伏隔核核心(AcbC)接收来自前扣带皮层(ACC)中CaMKII阳性神经元的兴奋性投射并在CPOP的发生发展中发挥重要作用。作者证实,在皮肤/肌肉切开与牵拉后,AcbC神经元对伤害性及非伤害性刺激的反应均显著增强。此外,光纤记录和电生理记录进一步表明,术后ACCCaMKII–AcbC通路的活动也明显升高。抑制AcbC神经元或ACCCaMKII–AcbC通路可缓解CPOP小鼠的痛觉超敏,而激活该通路则可在正常小鼠中诱发疼痛表型。这些结果揭示了AcbC神经元及ACCCaMKII–AcbC通路在CPOP发病机制中的关键作用,为术后疼痛的治疗提供了潜在的干预靶点。
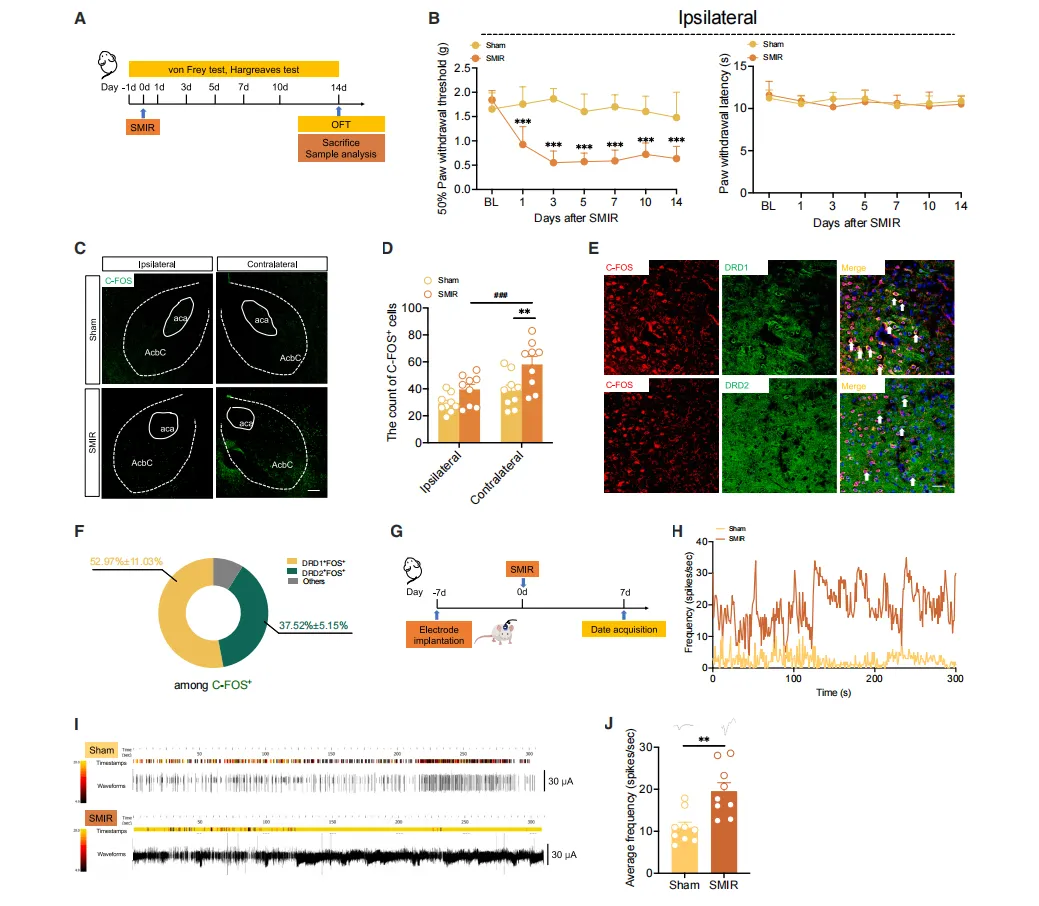
图一 在SMIR小鼠中,AcbC的神经元被显著激活
为了探究慢性术后疼痛(CPOP)的病理机制,作者建立了SMIR啮齿类动物模型。通过Von Frey实验测量50%缩足阈值以量化机械性异常性疼痛,通过Hargreaves实验测量缩足潜伏期以量化热痛觉过敏。
定量分析显示,SMIR小鼠术后第1天至第14天,手术侧后爪的50%缩足阈值(上海欣软)显著降低,而非手术侧后爪则未受影响。然而,在SMIR组和假手术组中,手术侧与非手术侧后爪的缩足潜伏期均无统计学显著差异。这些结果表明,SMIR诱导的慢性术后疼痛特异性表现为机械性异常性疼痛,而不影响热敏感性。
此外,为评估SMIR手术后是否存在运动功能障碍,对SMIR组和假手术组进行了旷场实验(VisuTrack,上海欣软)。术后第14天的运动活性定量评估显示,两组小鼠的总移动距离相当,表明该手术操作未对整体运动能力产生显著影响。研究发现,SMIR小鼠的伏隔核核心在非手术侧(即未受伤的一侧大脑)中,C-FOS阳性神经元数量明显增多且密度显著高于手术侧,表明神经损伤后大脑激活呈现“偏侧化”特征。
进一步分析显示:这些被激活的神经元中,约53%属于D1受体型中型多棘神经元(D1R-MSNs),约38%属于D2受体型(D2R-MSNs),说明两类主要神经元均参与其中。
为验证功能变化,作者在自由活动小鼠的非手术侧NAc核心植入电极进行记录,发现SMIR小鼠的神经元放电频率显著高于假手术组。
综合来看,SMIR模型通过激活伏隔核核心(尤其是非手术侧)的神经元,增强其电活动和即刻早期基因表达,揭示了该脑区在慢性术后疼痛中的关键作用。
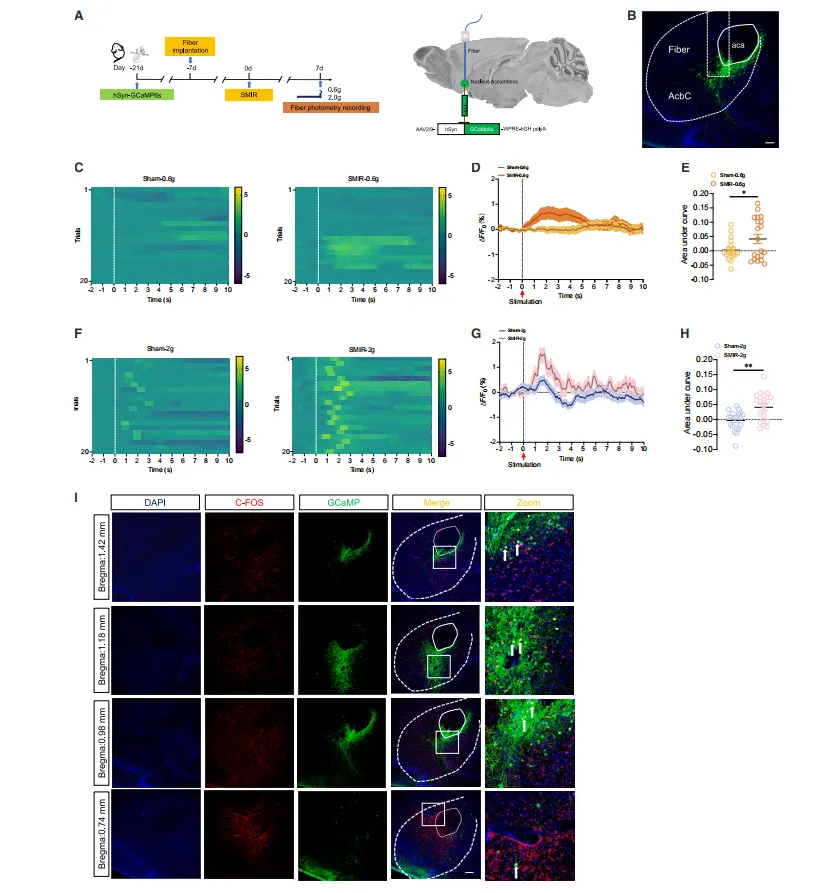
图二 SMIR小鼠的伏隔核核心神经元对非伤害性刺激和伤害性刺激均表现出增强的反应
为动态监测神经元活动,作者在小鼠伏隔核核心注射钙指示剂GCaMP6s并植入光纤,通过光纤记录自由活动状态下对机械刺激的反应。
使用0.6克(非伤害性)和2克(伤害性)Von Frey纤维丝刺激后发现:假手术组对0.6克刺激仅有微弱反应,而SMIR小鼠(慢性术后疼痛模型)则表现出显著增强的钙信号;在2克刺激下,两组均有反应,但SMIR组明显更强;
定量分析(曲线下面积)证实,SMIR组在两种刺激下的神经元活动均显著升高。
此外,GCaMP阳性神经元与C-FOS(神经激活标志物)存在共标,进一步验证了其高活性状态。
综上,SMIR导致伏隔核核心神经元处于“超敏”状态,不仅对痛觉刺激反应更强,甚至对原本无害的轻触也产生过度反应,这可能是慢性术后疼痛的重要机制之一。
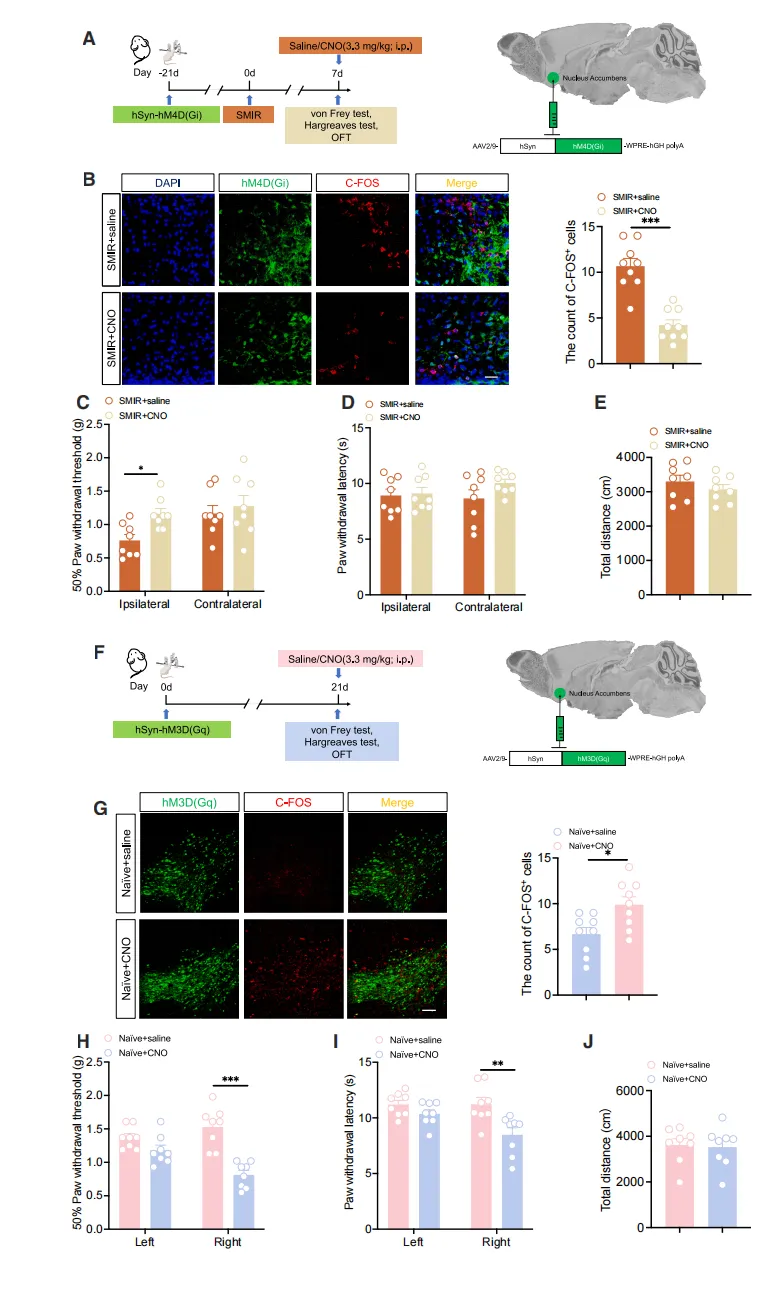
图三 NAc核心神经元参与疼痛的双向调控
为探究NAc核心神经元在SMIR诱导的慢性术后疼痛中的作用,作者采用化学遗传学进行双向调控。
在SMIR小鼠对侧NAc核心注射抑制型受体,激活后显著减少C-FOS表达,有效抑制神经元活性并特异性缓解手术侧后爪的机械性异常性疼痛(50%缩足阈值升高),而对侧痛觉和运动功能不受影响。
反之,在正常小鼠单侧NAc核心注射激活型受体hM3D(Gq),激活后可诱发对侧后爪痛觉超敏(缩足阈值降低、潜伏期缩短),同样不损害运动能力。
这些结果表明,NAc核心神经元具有双向调控疼痛的能力:其激活足以引发痛觉过敏,而抑制则能有效缓解慢性术后疼痛,凸显该脑区在疼痛调控中的关键作用。
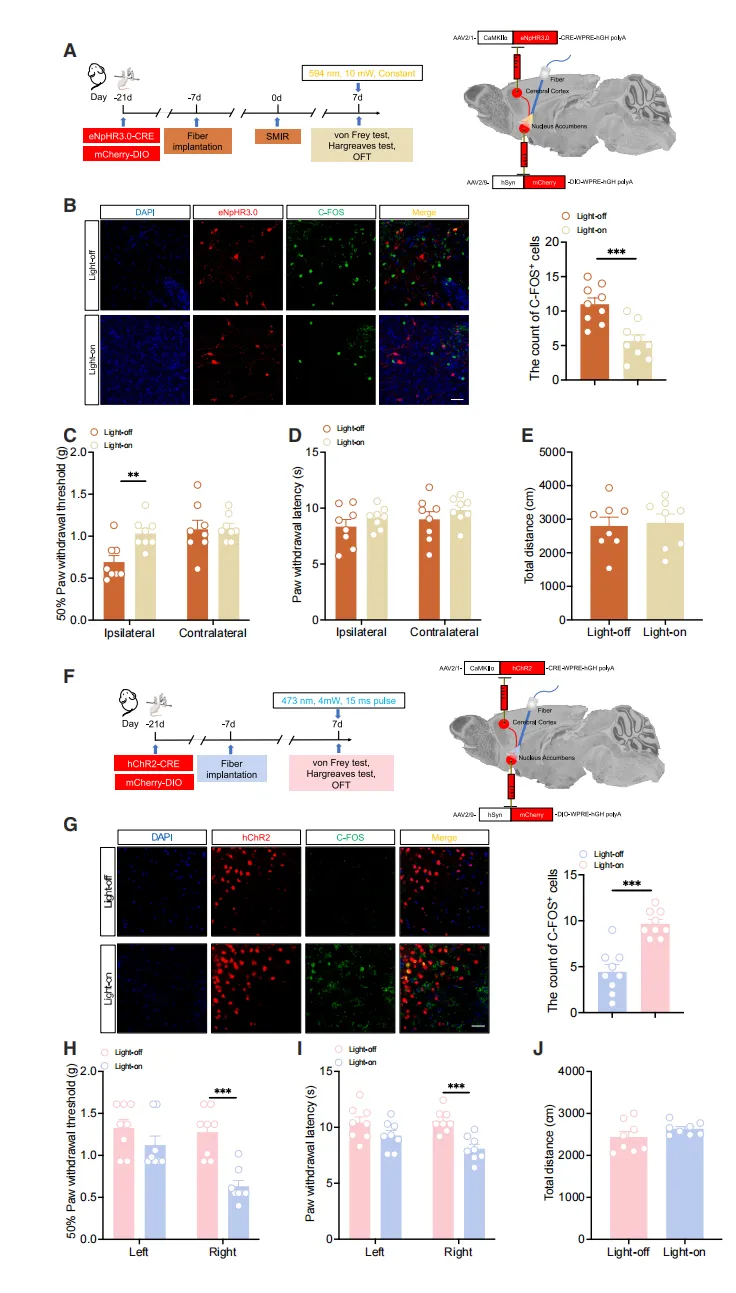
图四 ACCCaMKII–AcbC通路参与疼痛的双向调控
为探究前扣带皮层CaMKII神经元到ACCCaMKII→AcbC这一兴奋性通路在慢性术后疼痛中的作用,作者采用光遗传学进行双向调控。
首先,在SMIR小鼠中抑制该通路:通过跨突触病毒在ACC表达抑制型光敏蛋白eNpHR3.0并在AcbC植入光纤。594 nm光照后,ACC投射神经元活性下降(C-FOS减少),显著提高手术侧后爪的机械痛阈(即疼痛缓解),而对侧痛觉和运动功能不受影响。
接着,在正常小鼠中激活该通路:光刺激后,对侧后爪出现明显痛觉超敏:缩足阈值降低、反应更快,但运动能力正常。
这些结果表明:ACCCaMKII→AcbC通路能双向调控疼痛,激活它可诱发痛觉过敏,抑制它则能缓解慢性术后疼痛,说明该通路在伤害性信息处理中扮演关键角色。
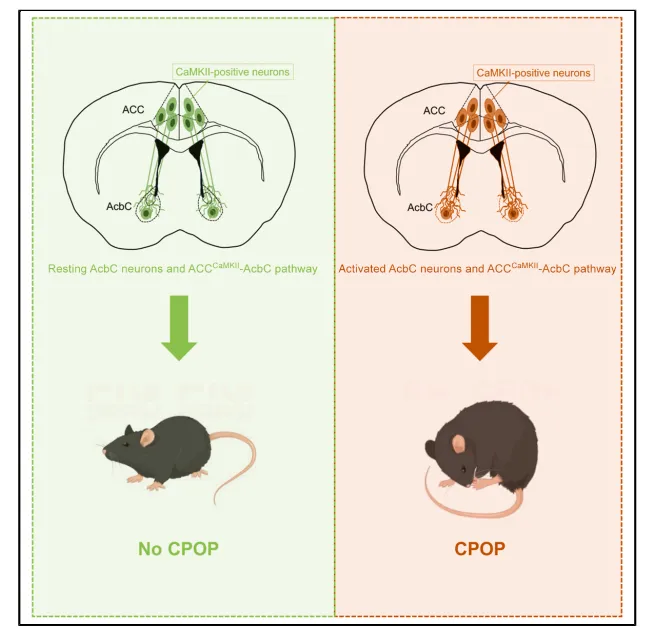
图五 全文摘要图
总结
本研究揭示了AcbC神经元及其上游ACCCaMKII-AcbC通路在CPOP中的关键作用:抑制该通路可有效缓解疼痛,激活则诱发痛觉超敏且均不影响运动功能。这些发现不仅阐明了CPOP的环路机制,也为未来基于精准神经调控(如深部脑刺激、经颅磁刺激等)的术后疼痛干预提供了新的靶点和理论依据。
文章来源:
https://doi.org/10.1016/j.isci.2025.113921
欣软产品应用






欢迎转发分享
